
【題目】下列元素中,屬于第三周期的是( )
A. 鋰
B. 氟
C. 磷
D. 鐵
科目:高中化學 來源: 題型:
【題目】鹵代烴分子里的鹵素原子與活潑金屬或其陽離子結合,發生下列反應(X表示鹵素原子):
R—X+2Na+X—R′![]() R—R′+2NaX
R—R′+2NaX
R—X+NaCN![]() R—CN+NaX
R—CN+NaX
根據下列各物質的轉化關系填空:

(1)E的結構簡式是______________。
(2)B→D的化學方程式是________________________。
(3)C→F的化學方程式是________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】TiCl4是由鈦精礦(主要成分為TiO2)制備鈦(Ti)的重要中間產物,制備純TiCl4的流程示意圖如下:
![]()
資料:TiCl4及所含雜質氯化物的性質
化合物 | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
沸點/℃ | 58 | 136 | 181(升華) | 316 | 1412 |
熔點/℃ | 69 | 25 | 193 | 304 | 714 |
在TiCl4中的溶解性 | 互溶 | —— | 微溶 | 難溶 | |
(1)氯化過程:TiO2與Cl2難以直接反應,加碳生成CO和CO2可使反應得以進行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ΔH1=+175.4 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220.9 kJ·mol-1
① 沸騰爐中加碳氯化生成TiCl4(g)和CO(g)的熱化學方程式:____________________。
② 氯化過程中CO和CO2可以相互轉化,根據如圖判斷:CO2生成CO反應的ΔH_____0(填“>”“<”或“=”),判斷依據:_______________。
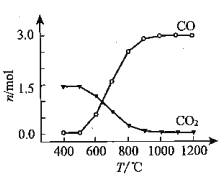
③ 氯化反應的尾氣須處理后排放,尾氣中的HCl和Cl2經吸收可得粗鹽酸、FeCl3溶液,則尾氣的吸收液依次是__________________________。
④ 氯化產物冷卻至室溫,經過濾得到粗TiCl4混合液,則濾渣中含有_____________。
(2)精制過程:粗TiCl4經兩步蒸餾得純TiCl4。示意圖如下:
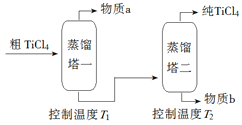
物質a是______________,T2應控制在_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生活密切相關。下列說法正確的是
A. 植物油的主要成分是不飽和高級脂肪酸甘油酯
B. 尼龍繩、宣紙均可由合成纖維制造
C. 淀粉和纖維素都是人體中能量的重要來源
D. 酶是生物體內重要的催化劑,僅由碳、氫、氧三種元素組成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1.76克銅鎂合金完全溶解于50mL、密度為1.400g/cm3、質量分數為63%的濃硝酸中,得到NO2氣體1792mL(標準狀況),向反應后的溶液中加入適量的1.0mol/LNaOH溶液,恰使溶液中的金屬離子全部沉淀。下列說法不正確的是( )
A. 該濃硝酸中HNO3的物質的量濃度是14.0mol/L
B. 加入NaOH溶液的體積是50mL
C. 濃硝酸在與合金反應中起了酸性和氧化性的雙重作用,且起氧化性的硝酸的物質的量為0.08 mol
D. 得到的金屬氫氧化物的沉淀為3.12克
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知反應: MnO2 +4HCl(濃) ![]() MnCl2 + Cl2↑+ 2H2O。將一定質量的二氧化錳溶解在過量的濃鹽酸中,反應一段時間后生成標準狀況下氯氣4.48 L (假設反應前后溶液體積不變)。試回答下列問題:
MnCl2 + Cl2↑+ 2H2O。將一定質量的二氧化錳溶解在過量的濃鹽酸中,反應一段時間后生成標準狀況下氯氣4.48 L (假設反應前后溶液體積不變)。試回答下列問題:
(1)用單線橋法標明該反應中電子轉移的方向和數目:______
MnO2 +4HCl(濃) ![]() MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(2)計算反應消耗的MnO2的質量______ ;
(3)計算被氧化的HCl物質的量______ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】漢黃芩素是傳統中草藥黃芩的有效成分之一,對腫瘤細胞的殺傷有獨特作用。下列有關漢黃芩素的敘述正確的是()。

A. 漢黃芩素的分子式為C16H13O5
B. 該物質遇FeCl3溶液顯色
C. 1 mol該物質與溴水反應,最多消耗1 mol Br2
D. 與足量H2發生加成反應后,該分子中官能團的種類減少1種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于一些重要的化學概念有下列說法,其中正確的是
①Fe(OH)3膠體和CuSO4溶液都是混合物
②BaSO4是一種難溶于水的強電解質
③冰醋酸、純堿、小蘇打分別屬于酸、堿、鹽
④煤的干餾、煤的汽化和液化都屬于化學變化
⑤置換反應都屬于離子反應
A. ①②⑤ B. ①②④ C. ②③④ D. ③④⑤
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com