
(1)硫元素有多種化合價,可形成多種化合物。填寫下表中的空白:
| 化合價 | -2 | -1 | 0 | +2 | +4 | +6 | +7 |
| 代表物的化學式 | | FeS2 | S | Na2S2O3 | | SO3或H2SO4或Na2SO4 | Na2S2O8 |

(1)(2分)化合價 -2 -1 0 +2 +4 +6 +7 代表物的化學式 Na2S或H2S等 SO2或Na2SO3
(2)HSO3- H++SO32-、HSO3-+H2O
H++SO32-、HSO3-+H2O H2SO3+OH-、H2O
H2SO3+OH-、H2O H++OH-;(3分,每個方程式1分)
H++OH-;(3分,每個方程式1分)
(3)c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)(2分);減小(1分);2SO32-+O2=2SO42-,SO32-被氧化生成SO42-,SO32-的濃度減小,水解產生的OH-濃度減小,溶液pH減小;(2分,只要敘述合理,不寫方程式也得分)
(4)還原;具有氧化性、沉淀性(或能與陽離子結合產生沉淀)、絡合性(或能形成絡合物)、能發生歧化反應(或既具有氧化性又具有還原性)。(答對一條1分,共3分,錯誤不得分,只要合理即可得分)
解析試題分析:(1)硫元素表現-2價,有硫化鈉等,硫元素表現+4價,有二氧化硫、亞硫酸鹽等,故答案為:Na2S等;SO2等;
(2)溶液中存在水的電離平衡、亞硫酸氫根的電離平衡與水解平衡,平衡反應的離子方程式分別為HSO3- H++SO32-、HSO3-+H2O
H++SO32-、HSO3-+H2O H2SO3+OH-、H2O
H2SO3+OH-、H2O H++OH-,
H++OH-,
(3)Na2SO3溶液亞硫酸根水解得到亞硫酸氫根,溶液呈堿性,亞硫酸根氫根水解得到亞硫酸,同時存在水的電離,故溶液中氫氧根離子的濃度大于亞硫酸氫根離子,堿性條件下,氫離子濃度原小于亞硫酸氫根離子濃度,水解程度不大,亞硫酸根濃度大于氫氧根離子濃度,故溶液中離子濃度大小關系為:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+),
Na2SO3溶液放置于空氣中一段時間后,SO32-被氧化生成SO42-,SO32-的濃度減小,水解產生的OH-濃度減小,溶液pH減小,
(4)Na2S2O3溶液與氯化鋇溶液混合后,沒有明顯現象,加入氯水,有白色沉淀生成,該沉淀為硫酸鋇,反應中硫元素的化合價升高,Na2S2O3表現還原性;
Na2S2O3中硫元素的化合價處于中間價態,具有氧化性、還原性,可能發生歧化反應等.
考點:本題考查硫元素化合物的性質、常用化學用語、鹽類水解、離子濃度比較等。


 陽光課堂課時作業系列答案
陽光課堂課時作業系列答案科目:高中化學 來源: 題型:填空題
硅酸鈉是一種重要的無機功能材料,某研究性學習小組設計的利用海邊的石英砂(含氯化鈉、氧化鐵等雜質)制備硅酸鈉的流程如下: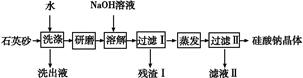
(1)石英砂加水洗滌的目的是 。
研磨后加入NaOH溶液溶解的離子方程式是 。
(2)實驗室進行蒸發操作要用到的儀器有鐵架臺(含鐵圈)、 和 。
(3)殘渣Ⅰ的成分是 (填化學式)。將殘渣Ⅰ溶于鹽酸,再加入NaOH溶液得到沉淀,將該沉淀加入到NaClO和NaOH混合溶液中可制得一種優質凈水劑,完成反應的離子方程式: + ClO-+ OH- + Cl-+ H2O
+ Cl-+ H2O
(4)按上述流程制得的硅酸鈉晶體可表示為Na2O·nSiO2,若石英砂的質量為10.0 g,其中含SiO2的質量分數為90%,最終得到硅酸鈉晶體15.2 g,則n= 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氯水具有多種性質,根據新制氯水分別與如圖五種物質發生的反應填空(氯水足量):
(1)a、b、c中反應的離子方程式為: 。
e中的化學反應方程式為 。上述反應中發生了氧化還原反應的是: (填“a”、“b”、“c”或“e”)。
(2)能證明氯水具有漂白性的現象是____________________________。
(3)久置的氯水變為________,用化學反應方程式表示為__________。
(4)實驗室保存飽和氯水的方法是_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
為了探究三種氣態氧化物(SO2、NO2、CO2)的性質,某同學設計了一組實驗:
實驗一:探究三種氣體在水中的溶解性,用三支相同的試管收集滿三種氣體,倒置在盛滿水的燒杯中,一段時間后,觀察到的現象如圖A、B、C所示。
(1)在相同條件下,三種氣體在水中溶解度最大的是________(寫化學式)寫出A燒杯中發生反應的化學方程式:____ 。如果在三只燒杯中分別滴幾滴紫色石蕊試液,可觀察到的現象是_____________________ 。
實驗二:用三只集氣瓶收集滿二氧化硫、二氧化氮氣體,然后將其倒置在水槽中。分別緩慢通入適量O2或Cl2,如圖D、E、F所示。一段時間后,D、E裝置的集氣瓶中充滿溶液,F裝置的集氣瓶中還有氣體剩余。
(2)實驗二中裝置D的集氣瓶最終充滿溶液(假設瓶內液體不擴散):
①寫出裝置D中總反應的化學方程式:
_______________________________________________。
②假設該實驗條件下,氣體摩爾體積為a L·mol-1。則裝置D的集氣瓶中所得溶液溶質的物質的量濃度為____________________。
(3) 寫出實驗F通入氧氣后,發生反應的化學方程式:____________________________。
(4)溶液充滿集氣瓶后,在E裝置的水槽里滴加硝酸鋇溶液,可能觀察到的現象為________,用有關的離子方程式解釋原因:________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氨在國民經濟中占有重要地位。
(1)NH3的電子式為
(2)實驗室中制取氨氣的化學方程式為 ,生成的氣體可以用蘸有濃鹽酸的玻璃棒來檢驗,將產物溶于水,溶液呈酸性,用離子方程式表示原因 ;
溶液中離子濃度由大到小的順序為
(3)欲快速制取氨氣,可將濃氨水滴入固體氫氧化鈉中,其裝置如圖,請結合化學用語從化學平衡的角度解釋: 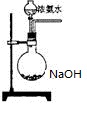
(4)將SO2氣體通入氯化鋇溶液,未見有沉淀生成,繼續通入NH3,則出現白色沉淀,請寫出反應的離子方程式 ;若將SO2氣體通入酸化的硝酸鋇溶液,也產生白色沉淀,用離子方程式加以說明
(5)氨和肼(N2H4)是氮的兩種常見化合物,在科學技術和生產中有重要的應用。
肼——空氣燃料電池是一種堿性電池,該電池放電時,負極的反應式 。
(6)氮氧化物的排放會對空氣造成污染,利用氧化法除去煙氣中的氮氧化物。首先向氮氧化物中補充氧氣,然后將混合氣體通入石灰乳中,使之轉化為硝酸鈣。已知某氮氧化物由NO和NO2組成,且n(NO):n(NO2)=1:3.寫出氧化吸收法除去氮氧化物的化學方程式___________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
化學實驗的微型化可有效地減少污染,實現化學實驗綠色化的要求。某學生按下列操作做一個實驗:在一塊下襯白紙的玻璃片的不同位置分別滴加濃度為0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每種液滴彼此分開,圍成半徑小于表面皿的圓形(如下圖所示),在圓心e處放置2粒芝麻粒大小的KMnO4晶體,向KMnO4晶體上滴加一滴濃鹽酸,再立即將表面皿蓋好。(已知:2KMnO4+16HCl(濃)=2KCl+2MnCl2+5Cl2↑+8H2O)
(1)e處反應的離子方程式為_____________________,該反應中發生反應的氧化劑和還原劑的物質的量之比為 。
(2)b處的實驗現象為________________,d處的實驗現象為___________________。
(3)c處反應的化學方程式為_______________________ ______,標準狀況下,當有0.224 L Cl2被NaOH溶液吸收后,轉移電子的物質的量為 mol。
(4)通過該實驗能否比較Cl2、FeCl3、KMnO4三種物質氧化性的強弱? (填“能”或“不能”),若能,其氧化性由強到弱的順序是 。(若不能,此空不填)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業生產硝酸的尾氣中含有氮氧化物NOx(NO和NO2的混合物,假設不含N2O4),對生態環境和人類健康帶來較大的威脅。
(1)工業上可用氨催化吸收法處理NOx,反應原理為:
 。某化學興趣小組模擬該處理過程的實驗裝置如下(夾持裝置已略去):
。某化學興趣小組模擬該處理過程的實驗裝置如下(夾持裝置已略去):
①裝置A中發生反應的化學方程式為 。
②裝置D中堿石灰的作用是 。
(2)工業上也常用Na2CO3溶液吸收法處理NOx。已知:NO不能與Na2CO3溶液反應,
NO+ NO2+Na2CO3=2NaNO2+ CO2;2NO2+Na2CO3= NaNO2+ NaNO3+CO2.
①當NOx被Na2CO3溶液完全吸收時,x的值不可能是 (填字母)。
A.1.3 B.1.6 C.1.8
②將1 mol NOx通入Na2CO3溶液中,被完全吸收時,溶液中生成的NO—3、NO—2兩種離子的物質的量隨x變化關系如圖所示:
圖中線段a表示 離子隨x值變化的關系;若用溶質質量分數為21.2%的Na2CO3溶液吸收,則需要Na2CO3溶液至少 g。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
研究NO2、SO2、CO等大氣污染氣體的處理及利用的方法具有重要意義。
⑴一定條件下,NO2與SO2反應生成SO3和NO兩種氣體。將體積比為1∶2的NO2、SO2氣體置于密閉容器中發生上述反應,下列能說明反應達到平衡狀態的是________(填字母)。
a.體系壓強保持不變 b.混合氣體顏色保持不變
c.體系中SO3的體積分數保持不變 d.每消耗1 mol SO2的同時生成1 mol NO
測得上述反應平衡時NO2與SO2體積比為1∶6,則平衡常數K=________。
⑵新型氨法煙氣脫硫技術的化學原理是采用氨水吸收煙氣中的SO2,再用一定量的磷酸與上述吸收產物反應。該技術的優點除了能回收利用SO2外,還能得到一種復合肥料,該復合肥料可能的化學式為________(寫出一種即可)。
⑶右圖是MCFC燃料電池,它是以水煤氣(CO、H2)為燃料,一定比例Li2CO3和Na2CO3低熔混合物為電解質。A為電池的________(填“正”或“負”)極,寫出B極電極反應式:________________________。
⑷工業上常用Na2CO3溶液吸收法處理氮的氧化物(以NO和NO2的混合物為例)。
已知:NO不能與Na2CO3溶液反應。
NO+NO2+Na2CO3=2NaNO2+CO2
2NO2+Na2CO3=NaNO2+NaNO3+CO2
①用足量的Na2CO3溶液完全吸收NO和NO2的混合物,每產生22.4 L(標準狀況)CO2(全部逸出)時,吸收液質量就增加44 g,則混合氣體中NO和NO2的體積比為
____________。
②用Na2CO3溶液吸收法處理氮的氧化物存在的缺點是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
以黃鐵礦為原料生產硫酸的工藝流程圖如下:
(1)已知: (已折算為標況下)SO3氣體與H2O化合時放出的熱量為 (保留兩位有效數字)。
(已折算為標況下)SO3氣體與H2O化合時放出的熱量為 (保留兩位有效數字)。
(2)沸騰爐中發生反應的化學方程式為 。
(3)依據工藝流程圖判斷下列說法正確的是(選填序號字母) 。
a.沸騰爐排出的礦渣可供煉鐵
b.過量空氣能提高SO2的轉化率
c.使用催化劑能提高SO2的反應速率和轉化率
d.為使黃鐵礦充分燃燒,需將其粉碎
(4)在吸收塔吸收SO3不用水或稀硫酸的原因 。
(5)吸收塔排出的尾氣先用氨水吸收,再用濃硫酸處理,得到較高濃度的SO2和銨鹽。
①SO2既可作為生產硫酸的原料循環再利用,也可用于工業制溴過程中吸收潮濕空氣中的Br2。SO2吸收Br2的離子方程式是 。
②為測定該銨鹽中氮元素的質量分數,將不同質量的銨鹽分別加入到50.00mL相同濃度的NaOH溶液中,沸水浴加熱至氣體全部逸出(此溫度下銨鹽不分解)。該氣體經干燥后用濃硫酸吸收完全,測定濃硫酸增加的質量。部分測定結果如下表(a>0): 
計算:該銨鹽中氮元素的質量分數是 %;若銨鹽質量為15.00g,濃硫酸增加的質量為 。(計算結果保留兩位小數)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com