

| A.鐵粉 | B.鈉 | C.氯化鋇溶液 | D.銀粉 |
| 序號 | 不合理的原因 | 誤差 (偏低或偏高) | 改變措施 |
| 方案① | | | |
| 方案② | | | |
| 方案序號 | 不合理的原因 | 誤差(偏低或偏高) | 改變措施 |
| 方案① | 高錳酸鉀溶液中含有硫酸,與氯化鋇反應,使生成的沉淀增多 | 偏低 | 將硫酸酸化的高錳酸鉀溶液換成溴水或碘水或硝酸溶液 |
| 方案② | -- | -- | -- |
 CuSO4+SO2↑+2H2O。隨著反應的進行。硫酸逐漸變稀。稀硫酸與銅片不發生反應。反應后的溶液中含有CuSO4、H2O及過量的H2SO4。要證明反應結束后的燒瓶中確有余酸,A.加入Fe粉會發生反應:CuSO4+Fe= FeSO4+Cu; H2SO4+Fe= FeSO4+H2↑.會有氣體產生,因此會冒出氣泡。正確。B.由于溶液中含有大量的水,無論酸是否有剩余,都會發生反應:2Na+2H2O=2NaOH+H2↑。因此不能證明酸剩余。錯誤。C.溶液中含有CuSO4,一定會發生反應:Ba2++SO42-=BaSO4↓。不能證明酸剩余。錯誤。D.在金屬活動性順序表中Ag位于H后面,不能把酸中的氫置換出來。錯誤。因此選項為A。(3)I、方案①中KMnO4溶液酸化是用的硫酸,因此在高錳酸鉀溶液中的SO42-包括SO2氧化產生的和外加的兩部分,這樣產生的硫酸鋇沉淀就偏多,導致剩余的硫酸偏少(或偏低)。改變的措施是采用其它的氧化劑如溴水或碘水或硝酸溶液等氧化SO2,使其轉化為硫酸,再用氯化鋇溶液減小滴定。方案②設計合理、操作無誤。Ⅱ、用標準NaOH溶液滴定剩余硫酸時,由于在溶液中含有CuSO4,用酚酞作指示劑,變色點為8,但氫氧化銅開始沉淀的pH約為5。Cu2+也會與堿反應生成沉淀,不能達到滴定終點。無法準確測定剩余硫酸的物質的量的多少。(4)其他可行的用來測定余酸的物質的量濃度實驗方案可以是方案一:①取反應后溶液,向其中加入足量鋅;②收集并測定氫氣的體積;③通過H2量計算剩余硫酸的物質的量濃度。方案二:反應結束后將燒瓶中的銅片取出,洗凈、在N2的環境中烘干,稱其質量即可。方案三:反應結束后將燒瓶中的銅片取出,然后向溶液中加入足量氯化鋇溶液,過濾出沉淀,洗凈、干燥后稱量。根據反應消耗的Cu的質量科確定由CuSO4產生的沉淀的質量。進而計算出剩余酸的物質的量。在這三種方案中第三種方案可操作性更強,誤差更小。第二種方法中要在惰性氣體或N2的環境中進行不容易進行。而第一種方法H2的體積測量容易引起誤差,而且不容易換算為標準狀況下。容易產生誤差。
CuSO4+SO2↑+2H2O。隨著反應的進行。硫酸逐漸變稀。稀硫酸與銅片不發生反應。反應后的溶液中含有CuSO4、H2O及過量的H2SO4。要證明反應結束后的燒瓶中確有余酸,A.加入Fe粉會發生反應:CuSO4+Fe= FeSO4+Cu; H2SO4+Fe= FeSO4+H2↑.會有氣體產生,因此會冒出氣泡。正確。B.由于溶液中含有大量的水,無論酸是否有剩余,都會發生反應:2Na+2H2O=2NaOH+H2↑。因此不能證明酸剩余。錯誤。C.溶液中含有CuSO4,一定會發生反應:Ba2++SO42-=BaSO4↓。不能證明酸剩余。錯誤。D.在金屬活動性順序表中Ag位于H后面,不能把酸中的氫置換出來。錯誤。因此選項為A。(3)I、方案①中KMnO4溶液酸化是用的硫酸,因此在高錳酸鉀溶液中的SO42-包括SO2氧化產生的和外加的兩部分,這樣產生的硫酸鋇沉淀就偏多,導致剩余的硫酸偏少(或偏低)。改變的措施是采用其它的氧化劑如溴水或碘水或硝酸溶液等氧化SO2,使其轉化為硫酸,再用氯化鋇溶液減小滴定。方案②設計合理、操作無誤。Ⅱ、用標準NaOH溶液滴定剩余硫酸時,由于在溶液中含有CuSO4,用酚酞作指示劑,變色點為8,但氫氧化銅開始沉淀的pH約為5。Cu2+也會與堿反應生成沉淀,不能達到滴定終點。無法準確測定剩余硫酸的物質的量的多少。(4)其他可行的用來測定余酸的物質的量濃度實驗方案可以是方案一:①取反應后溶液,向其中加入足量鋅;②收集并測定氫氣的體積;③通過H2量計算剩余硫酸的物質的量濃度。方案二:反應結束后將燒瓶中的銅片取出,洗凈、在N2的環境中烘干,稱其質量即可。方案三:反應結束后將燒瓶中的銅片取出,然后向溶液中加入足量氯化鋇溶液,過濾出沉淀,洗凈、干燥后稱量。根據反應消耗的Cu的質量科確定由CuSO4產生的沉淀的質量。進而計算出剩余酸的物質的量。在這三種方案中第三種方案可操作性更強,誤差更小。第二種方法中要在惰性氣體或N2的環境中進行不容易進行。而第一種方法H2的體積測量容易引起誤差,而且不容易換算為標準狀況下。容易產生誤差。

 寒假創新型自主學習第三學期寒假銜接系列答案
寒假創新型自主學習第三學期寒假銜接系列答案科目:高中化學 來源:不詳 題型:單選題
| A.測pH值 | B.測導電性大小 | C.測密度 | D.進行中和滴定 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.根據元素分析結果推測該粉末為純凈物 |
| B.將該粉末溶于水,加入氯化鋇,有白色沉淀生成,證明該粉末中含有K2SO4 |
| C.將該粉末加入鹽酸中,產生氣泡,證明該粉末是K2SO3粉末 |
| D.將該粉末溶于水,加入氯化鋇和過量的鹽酸,有白色沉淀和氣泡生成,證明該粉末是K2SO4和K2SO3的混合物 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.消除硫酸廠尾氣排放:SO2+2NH3 = (NH4)2SO3 |
| B.消除制硝酸工業尾氣排放:NO2+NO+2NaOH =2NaNO2+H2O |
| C.制CuSO4:Cu+2H2SO4(濃) = CuSO4+SO2↑+2H2O |
| D.制CuSO4:2Cu+O2= 2CuO CuO+H2SO4(稀) = CuSO4+H2O |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
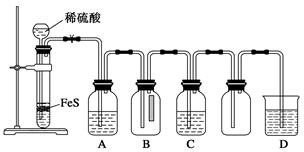
| | 實驗操作 | 實驗現象 |
| 實驗1 | 將等濃度的Na2S和Na2SO3溶液按體積比2∶1混合 | 無明顯現象 |
| 實驗2 | 將H2S通入Na2SO3溶液中 | 未見明顯沉淀,再加入少量稀硫酸,立即產生大量淺黃色沉淀 |
| 實驗3 | 將SO2通入Na2S溶液中 | 有淺黃色沉淀產生 |
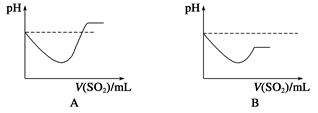
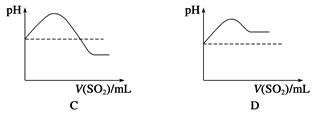
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| A.7.32 L | B.6.72 L | C.20.16 L | D.30.24 L |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
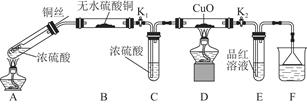
| 硫酸/mol·L-1 | 黑色物質出現的溫度/℃ | 黑色物質消失的溫度/℃ |
| 15 | 約150 | 約236 |
| 16 | 約140 | 約250 |
| 18 | 約120 | 不消失 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
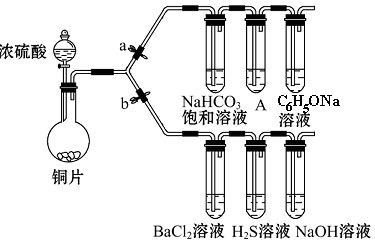
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com