CO2可轉(zhuǎn)化成有機物實現(xiàn)碳循環(huán)。
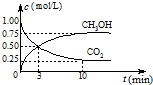
(1)在體積為1 L的密閉容器中,充入1 mol CO2和3 mol H2,一定條件下發(fā)生反應(yīng): CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 mol·L-1, 測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
CH3OH(g)+H2O(g) ΔH=-49.0 mol·L-1, 測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。

①從0 min到10 min,v(H2)= mol·(L·min)-1。
②能說明上述反應(yīng)達到平衡狀態(tài)的是 (選填編號)。
A.反應(yīng)中CO2與CH3OH的物質(zhì)的量濃度之比為1︰1(即圖中交叉點)
B.容器內(nèi)氣體的壓強不隨時間的變化而變化
C.單位時間內(nèi)每消耗3 mol H2,同時生成1 mol H2O
D.CO2的體積分數(shù)在混合氣體中保持不變
③下列措施中能使n (CH3OH)/n (CO2)增大的是 (選填編號)。
A.將H2O(g)從體系中分離 B.恒溫恒容充入He
C.恒溫恒壓充入He D.恒溫恒容再充入1 mol CO2和3 mol H2
(2)據(jù)報道,一定條件下由二氧化碳和氫氣合成二甲醚已成為現(xiàn)實。
2CO2(g)+6H2(g) 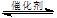 CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
在一定壓強下,測得反應(yīng)的實驗數(shù)據(jù)如下表。
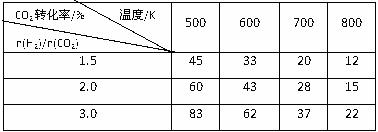
分析表中數(shù)據(jù)回答下列問題:
①反應(yīng)的溫度升高,K值 (填“增大”、“減小”或“不變”)。
②提高氫碳比[n(H2)/n(CO2)], K值 (填“增大”、“減小”或“不變”)。
(3)800℃時,C(s)+CO2(g) 2CO(g)的平衡常數(shù)K=1.64,相同條件下測得c(CO)=0.20 mol·L-1、c(CO2)=0.05 mol·L-1,此時反應(yīng)向 (填“正”或“逆”)方向進行。
2CO(g)的平衡常數(shù)K=1.64,相同條件下測得c(CO)=0.20 mol·L-1、c(CO2)=0.05 mol·L-1,此時反應(yīng)向 (填“正”或“逆”)方向進行。
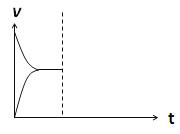
(4)在密閉容器中通入1mol H2和1mol CO2發(fā)生H2(g)+CO2(g)  CO(g)+H2O(g) △H> 0反應(yīng),當(dāng)反應(yīng)達到平衡后,在其他條件不變時,若升高溫度,請在下圖中畫出正(v正)、逆(v逆)反應(yīng)速率隨時間t變化的示意圖。
CO(g)+H2O(g) △H> 0反應(yīng),當(dāng)反應(yīng)達到平衡后,在其他條件不變時,若升高溫度,請在下圖中畫出正(v正)、逆(v逆)反應(yīng)速率隨時間t變化的示意圖。

![]() CH3OH(g)+H2O(g) ΔH=-49.0 mol·L-1, 測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
CH3OH(g)+H2O(g) ΔH=-49.0 mol·L-1, 測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
![]() CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g) 
![]() 2CO(g)的平衡常數(shù)K=1.64,相同條件下測得c(CO)=0.20 mol·L-1、c(CO2)=0.05 mol·L-1,此時反應(yīng)向 (填“正”或“逆”)方向進行。
2CO(g)的平衡常數(shù)K=1.64,相同條件下測得c(CO)=0.20 mol·L-1、c(CO2)=0.05 mol·L-1,此時反應(yīng)向 (填“正”或“逆”)方向進行。![]() CO(g)+H2O(g) △H> 0反應(yīng),當(dāng)反應(yīng)達到平衡后,在其他條件不變時,若升高溫度,請在下圖中畫出正(v正)、逆(v逆)反應(yīng)速率隨時間t變化的示意圖。
CO(g)+H2O(g) △H> 0反應(yīng),當(dāng)反應(yīng)達到平衡后,在其他條件不變時,若升高溫度,請在下圖中畫出正(v正)、逆(v逆)反應(yīng)速率隨時間t變化的示意圖。
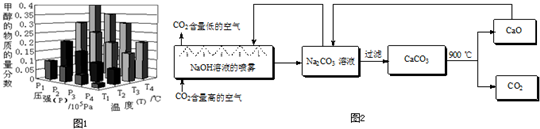

 CO2、SO2、NOx是對環(huán)境影響較大的氣體,控制和治理CO2、SO2、NOx是解決溫室效應(yīng)、減少酸雨和光化學(xué)煙霧的有效途徑.
CO2、SO2、NOx是對環(huán)境影響較大的氣體,控制和治理CO2、SO2、NOx是解決溫室效應(yīng)、減少酸雨和光化學(xué)煙霧的有效途徑. CO+3H2
CO+3H2 CH3OH(g)+H2O(g)△H=-49.0kJ/mol,測得CO2和CH3OH(g)的濃度隨時間變化如上左圖所示.
CH3OH(g)+H2O(g)△H=-49.0kJ/mol,測得CO2和CH3OH(g)的濃度隨時間變化如上左圖所示.