
【題目】Ⅰ.用化學用語回答下列問題:
(1)寫出二氧化碳分子的電子式:_____________;
(2)寫出氮氣分子的結構式____________。
Ⅱ.下列物質:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩HBr。
含有極性鍵和非極性鍵的是_______;
含有非極性鍵的離子化合物是_____。(填序號,下同)
Ⅲ.下列變化中:①干冰氣化;②硝酸鉀熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解;⑦碘升華;⑧溴蒸氣被木炭吸附。
(1)未破壞化學鍵的是_____________;
(2)僅離子鍵被破壞的是_____________;
(3)僅共價鍵被破壞的是_____________。
Ⅳ.下列物質:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④14N、14C
(1)互為同位素的是:______;
(2)互為同素異形體的是:______;
氫的三種原子1H、2H、3H 與氯的兩種原子35Cl、37Cl相互結合為氯化氫,可得分子中相對分子質量不同的有________種。
【答案】 ![]() N≡N ⑧ ⑤ ①⑤⑦⑧ ②③ ④⑥ ① ③ 【答題空10】⑤
N≡N ⑧ ⑤ ①⑤⑦⑧ ②③ ④⑥ ① ③ 【答題空10】⑤
【解析】Ⅰ.(1)寫出二氧化碳分子的電子式:![]() ;
;
(2)寫出氮氣分子的結構式N≡N。
Ⅱ.同種元素的原子之間形成的共價鍵是非極性鍵,不同種元素的原子之間形成的共價鍵是極性鍵。雙氧水中含氫氧鍵和氧氧鍵,所以含有極性鍵和非極性鍵的是⑧;過氧化鈉中含鈉離子和過氧根,兩個氧原子之間形成的是非極性鍵,所以含有非極性鍵的離子化合物是⑤。
Ⅲ. (1)分子晶體的三態變化中,變化的是分子間的距離,分子內的化學鍵沒有變化;木炭吸附溴蒸氣的作用力是分子間作用力,兩者的化學鍵都沒有變化。干冰、蔗糖、碘和溴都是分子晶體,所以未破壞化學鍵的是①⑤⑦⑧;
(2)離子鍵僅存于離子晶體,離子晶體在熔化時僅破壞離子鍵,硝酸鉀和硫酸氫鉀都屬于離子晶體,所以僅離子鍵被破壞的是②③;
(3)分子晶體只含共價鍵。屬于電解質的分子晶體在溶于時,共價鍵會被破壞,分子晶體在發生分解時,共價鍵被破壞,硫酸和碘化氫都能形成分子晶體,所以僅共價鍵被破壞的是④⑥。
Ⅳ. (1)同種元素的不同原子互稱同位素,所以互為同位素的是:①;
(2)同種元素形成的不同單質互稱為同素異形體,所以互為同素異形體的是:③;
氫的三種原子1H、2H、3H 與氯的兩種原子35Cl、37Cl相互結合為氯化氫,可得到6種分子,但是相對分子質量只有5種,分別是36、37、38、39、40.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】(1)已知常溫時,0.1mol/L某一元酸HA在水中有0.1%發生電離,則該溶液的pH= ,此酸的電離平衡常數K= ,由HA電離出的H+的濃度約為水電離出的H+的濃度的 倍。
(2)含有弱酸HA和其鈉鹽NaA的混合溶液,在化學上用作緩沖溶劑。向其中加入少量酸或堿時,溶液的酸堿性變化不大。
①向該溶液中加入少量鹽酸時,發生反應的離子方程式是 ,向其中加入少量KOH溶液時,發生反應的離子方程式是 。
②現將0.04mol﹒L-1HA溶液和0.02mol﹒L-1NaOH溶液等體積混合,得到緩沖溶液。
a、若HA為HCN,該溶液顯堿性,則溶液中c(Na+) c(CN-)(填“<”、“=”或“>”)。
b、若HA為CH3COOH,該溶液顯酸性,溶液中所有的離子按濃度由大到小排列的順序是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I、煤制天然氣的工藝流程簡圖如下:

⑴反應I:C(s) + H2O(g)![]() CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧氣會與部分碳發生燃燒反應。請利用能量轉化及平衡移動原理說明通入氧氣的作用:___________________________。
CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧氣會與部分碳發生燃燒反應。請利用能量轉化及平衡移動原理說明通入氧氣的作用:___________________________。
⑵反應II:CO(g) + H2O(g) ![]() CO2(g) + H2(g) ΔH = 41 kJ·mol-1。如圖表示不同溫度條件下,煤氣化反應I發生后的汽氣比(水蒸氣與CO物質的量之比)與CO平衡轉化率的變化關系。
CO2(g) + H2(g) ΔH = 41 kJ·mol-1。如圖表示不同溫度條件下,煤氣化反應I發生后的汽氣比(水蒸氣與CO物質的量之比)與CO平衡轉化率的變化關系。

① 判斷T1、T2和T3的大小關系:______________。(從小到大的順序)
② 若煤氣化反應I發生后的汽氣比為0.8,經煤氣化反應I和水氣變換反應II后,得到CO與H2的物質的量之比為1:3,則反應II應選擇的溫度是_______(填“T1”或“T2”或“T3”)。
⑶① 甲烷化反應IV發生之前需要進行脫酸反應III。煤經反應I和II后的氣體中含有兩種酸性氣體,分別是H2S和_______。
② 工業上常用熱碳酸鉀溶液脫除H2S氣體得到兩種酸式鹽,該反應的離子方程式是_______。
II、利用甲烷超干重整CO2技術可得到富含CO的氣體,將甲烷和二氧化碳轉化為可利用的化學品,其能源和環境上的雙重意義重大。該技術中的化學反應為:
CH4 (g)+3CO2 (g)![]() 2H2O(g)+4CO(g)
2H2O(g)+4CO(g) ![]() H>0
H>0
CH4超干重整CO2的催化轉化原理示意如圖:

⑷過程II,實現了含氫物種與含碳物種的分離。生成H2O(g)的化學方程式是______________。
⑸假設過程I和過程II中的各步均轉化完全,下列說法正確的是_______。((填序號)
a.過程I和過程II中均含有氧化還原反應
b.過程II中使用的催化劑為Fe3O4 和CaCO3
c.若過程I投料![]() ,可導致過程II中催化劑失效
,可導致過程II中催化劑失效
(6)一定條件下,向體積為2L的恒容密閉容器中充入1.2 mol CH4(g)和4.8 mol CO2(g),發生反應CH4 (g)+3CO2 (g)![]() 2H2O(g)+4CO(g)
2H2O(g)+4CO(g) ![]() H>0,實驗測得,反應吸收的能量和甲烷的體積分數隨時間變化的曲線圖像如圖。計算該條件下,此反應的
H>0,實驗測得,反應吸收的能量和甲烷的體積分數隨時間變化的曲線圖像如圖。計算該條件下,此反應的![]() H=________________。
H=________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高聚物的合成與結構修飾是制備具有特殊功能材料的重要過程。下圖是合成具有特殊功能高分子材料W(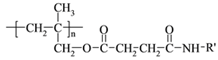 )的流程:
)的流程:
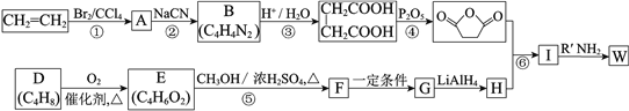
已知:(R、R1、R2代表烴基)
I、![]()
![]() RCH2OH
RCH2OH
II、![]()
⑴反應①的反應類型是_______________。
⑵反應②是取代反應,其化學方程式是___________________________________________。
⑶D的核磁共振氫譜中有兩組峰且面積之比是1:3,不存在順反異構。D的結構簡式是______。
⑷反應⑤的化學方程式是__________________________________________________。
⑸G的結構簡式是__________________。
⑹反應⑥的化學方程式是__________________________________________________。
⑺工業上也可用![]() 合成E。由上述①~④的合成路線中獲取信息,完成下列合成路線(箭頭上注明試劑和反應條件,
合成E。由上述①~④的合成路線中獲取信息,完成下列合成路線(箭頭上注明試劑和反應條件,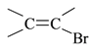 不易發生取代反應)__________________
不易發生取代反應)__________________
![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲、乙兩溶液中,分別含有大量的Cu2+、K+、H+、Cl-、CO32—、OH-6種離子中的3種,已知甲溶液呈藍色,則乙溶液中大量存在的離子是( )
A.K+、OH-、CO32— B.Cu2+、H+、Cl- C.K+、H+、Cl- D.CO32—、OH-、Cl-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用CaSO4代替O2與燃料CO反應,既可以提高燃燒效率,又能得到高純CO2,是一種高效、清潔、經濟的新型燃燒技術,反應①為主反應,反應②和③為副反應。
①1/4CaSO4(s)+CO(g)![]() 1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
②CaSO4(s)+CO(g)![]() CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
③CO(g)![]() 1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol
1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol
(1)反應2 CaSO4(s)+7CO(g)![]() CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H= (用△H1△H2△H3表示)。
CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H= (用△H1△H2△H3表示)。
(2)反應①~③的平衡常數的對數lgK隨反應溫度T的變化曲線見圖18.結合各反應的△H,歸納lgK~T曲線變化規律:
a)
b)

(3)向盛有CaSO4的真空恒容容器中充入CO,反應①于900 C達到平衡,c平衡(CO)=8.0×10-5mol·L-1,計算CO的轉化率(忽略副反應,結果保留2位有效數字)。
(4)為減少副產物,獲得更純凈的CO2,可在初始燃料中適量加入 。
(5)以反應①中生成的CaS為原料,在一定條件下經原子利用率100%的高溫反應,可再生成CaSO4,該反應的化學方程式為 ;在一定條件下CO2可與對二甲苯反應,在其苯環上引入一個羧基,產物的結構簡式為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com