
在實驗室模擬工業生產碳酸鈉:一定溫度下,往一定量飽和NaCl溶液中通入氨氣達到飽和后,再不斷通入CO2,一段時間后,出現沉淀,過濾得到NaHCO3晶體。
(1)該過程的化學方程式: 。
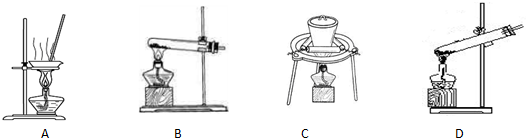
(2)加熱NaHCO3得到純堿制品,實驗室可進行此操作的裝置是 。

A B C D
(3)得到的純堿制品含有少量NaHCO3和NaCl,設計實驗驗證樣品中各種組分。試劑和儀器限選用:試管、膠頭滴管、過濾裝置、Ba(NO3)2溶液、NaOH溶液、AgNO3溶液、澄清石灰水、稀硫酸、稀鹽酸、稀硝酸。
|
步驟一:取少量制品于試管中,加少量蒸餾水,振蕩,溶解。往試管中加入 振蕩,觀察 |
現象:溶液中產生大量白色沉淀;
結論: 。 |
|
步驟二:將步驟一的濁液過濾,取濾液于試管中B中,加入 , 振蕩,觀察 |
現象: ; 結論:樣品中含有NaHCO3 。 |
|
步驟三:將步驟二的濁液過濾,取濾液于試管C中, 振蕩,觀察 |
現象: ; 結論: 。 |
(4)用碘量法測量自來水中殘留的Cl2的濃度:
① 在大錐形瓶中放置過量的KI,加一定量的冰醋酸,準確取水樣200mL加入瓶中,迅速塞上瓶塞搖動,水樣呈淡黃色,發生反應:Cl2+2I-=2Cl-+ I2。
② 加少許淀粉溶液,用c mol/L Na2S2O3溶液滴定,發生反應:I2+2S2O32-=2I-+S4O62-,當 ,達到滴定終點。
③ 重復操作3次,平均讀數為V mL,則該樣品中殘留Cl2的濃度: mg/L(Cl的相對原子質量:35.5)
(16分)
(1) NaCl + NH3 + CO2 + H2O = NaHCO3 ↓+ NH4Cl (2分,沒有沉淀符號扣1分)
(2)BC (2分)
(3)
|
步驟一:取少量制品于試管中,加入少量蒸餾水,振蕩,溶解:往試管中加入 過量的Ba(NO3)2溶液,振蕩,觀察 (2分) |
現象:溶液中產生大量白色沉淀; 結論:試樣中含有Na2CO3 。(1分) |
|
步驟二:將步驟一的濁液過濾:取濾液于試管B中,加入 適量的NaOH溶液, 振蕩,觀察(1分) |
現象:有少量白色沉淀生成 ;(1分) 結論:試樣中含有NaHCO3 。 |
|
步驟三: 將步驟二的濁液過濾后,取濾液于試管C中,先加入足量的稀硝酸,再加入少許AgNO3溶液,振蕩,觀察(2分) |
現象:有少量白色沉淀生成 ; 結論:試樣中含有NaCl 。(1分) |
(8分)檢驗出Na2CO3 得3分;檢驗出NaHCO3 得2分(若用硝酸檢驗得1分),
檢驗出NaCl得3分(未加過量硝酸不得分)。三種物質檢驗不誅連。
(4)② 最后一滴溶液滴入,錐形瓶內的液體恰好從藍色變成無色,且半分鐘不變化 (2分)
③ 177.5 cV (即:0.5×c×V×10-3×71×1000/0.2)(2分)
【解析】
試題分析:(1)氨氣易溶于飽和食鹽水,且NH3+H2O=NH3•H2O,得到氯化鈉、氨水溶液;一水合氨是弱堿,二氧化碳是酸性氧化物,不斷通入二氧化碳氣體時,NH3•H2O+CO2=NH4HCO3;由于碳酸氫鈉的溶解度比氯化鈉、碳酸氫銨都小,碳酸氫鈉最先達到飽和,則碳酸氫銨與氯化鈉容易反應,生成碳酸氫鈉晶體和氯化銨溶液,即NH4HCO3+NaCl=NaHCO3↓+NH4Cl;上述幾步反應加起來可得:NaCl + NH3 + CO2 + H2O = NaHCO3 ↓+ NH4Cl;(2)碳酸氫鈉是固體,加熱固體樣品應該選擇試管或坩堝,故BC正確;A項,屬于蒸發裝置,加熱鹽溶液,分離和鹽和水,故A錯;未了防止冷凝水回流時,導致熱的試管底突然遇冷炸裂,試管底應該略低于試管口,故D錯;(3)制品是碳酸鈉、碳酸氫鈉和氯化鈉組成的混合物,它們都是可溶性鹽,根據實驗步驟一、二、三的操作及預期現象和結論綜合推斷,步驟I加入的試劑是過量或足量Ba(NO3)2溶液,振蕩,因為硝酸鋇只能與碳酸鈉反應,生成碳酸鋇沉淀和硝酸鈉,可以檢驗制品中含有碳酸鈉,并且除去其中的碳酸鈉,防止碳酸鈉對碳酸氫鈉、氯化鈉的檢驗產生干擾;由于碳酸氫鈉與硝酸鋇不能反應,但是碳酸氫鈉與足量或過量氫氧化鈉能發生反應,生成水和碳酸鈉,生成物中的碳酸鈉與步驟一中加入的過量或足量的硝酸鋇反應,濾液中又產生少量的白色沉淀,說明制品中含有少量碳酸氫鈉;檢驗制品中的氯化鈉可以用硝酸銀溶液檢驗,但是碳酸鈉也能與硝酸銀反應,都產生白色沉淀,因此需要除去制品中的碳酸鈉,由于步驟二的濾液中含有過量氫氧化鈉,氫氧化鈉也能與硝酸銀反應,產生白色沉淀,對氯化鈉的檢驗造成干擾,則步驟三必須先用過量或足量稀硝酸酸化,中和氫氧化鈉之后,再向步驟二的濾液中滴入少量或幾滴AgNO3溶液,產生少量的白色沉淀,說明制品中含有氯化鈉;(4)實驗①中發生的反應為Cl2+2I-=2Cl-+ I2,則錐形瓶內溶液中的碘離子被自來水中的氯氣氧化為單質碘;單質碘遇淀粉變藍,則實驗②中發生的反應為I2+2S2O32-=2I-+S4O62-,碘離子遇淀粉不變色,則錐形瓶內溶液的顏色由藍色變為無色,說以滴定終點的現象為:最后一滴Na2S2O3溶液溶液滴入,錐形瓶內的液體恰好從藍色變成無色,且半分鐘不變化;先根據c•V=n求Na2S2O3溶液中溶質的物質的量,即n(Na2S2O3)=cmol/L×V×10-3L= c×V×10-3mol;由于Na2S2O3是強電解質,完全電離出鈉離子和硫代硫酸根離子,且n(S2O32-)= n(Na2S2O3)= c×V×10-3mol;由于I2+2S2O32-=2I-+S4O62-中I2與S2O32-的物質的量之比等于系數之比,則單質的物質的量為c×V×10-3mol×1/2;由于Cl2+2I-=2Cl-+ I2中Cl2與I2的物質的量之比等于系數之比,則自來水中氯氣的物質的量為c×V×10-3mol×1/2×1/1; 氯氣的相對分子質量為71,然后根據n•M=m求自來水中所含氯氣的質量,則m(Cl2)= c×V×10-3mol×1/2×1/1×71g/mol;200mL=0.2L,最后根據n/V=c求自來水中所含氯氣的濃度,則c(Cl2)= c×V×10-3mol×1/2×1/1×71g/mol÷0.2L=0.5×c×V×10-3×71/0.2g/L=0.5×c×V×10-3×71×1000/0.2mg/L= 177.5 cV mg/L,因為1g=1000mg。
考點:考查探究實驗,涉及碳酸鈉工業制法的化學方程式、加熱固體的方法及使用的儀器、設計實驗方案檢驗制品中的碳酸鈉、設計實驗方案檢驗制品中的碳酸氫鈉、設計實驗方案檢驗制品中的氯化鈉、定量檢測自來水中所含氯氣的原理、滴定終點的現象、物質的量在電離或離子方程式中的應用、物質的量濃度、消耗標準溶液的體積、摩爾質量、質量、指定情況下的濃度等。


科目:高中化學 來源: 題型:閱讀理解

查看答案和解析>>
科目:高中化學 來源: 題型:

| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
| 步驟一:取少量制品于試管中,加少量蒸餾水,振蕩,溶解.往試管中加入 |
現象:溶液中產生大量白色沉淀; 結論: |
| 步驟二:將步驟一的濁液過濾,取濾液于試管中B中,加入 振蕩,觀察 |
現象: 結論:樣品中含有NaHCO3. |
| 步驟三:將步驟二的濁液過濾,取濾液于試管C中, 振蕩,觀察 |
現象: 結論: |
查看答案和解析>>
科目:高中化學 來源: 題型:
(14分)KCIO3在農業上用作除草劑,超細CaCO3廣泛用于生產牙膏、無炭復寫紙等。某同學在實驗室模擬工業生產,利用制乙炔產生的殘渣制備上述兩種物質,過程如下:
I.殘渣中主要成分是Ca(OH)2和 。
II.將I中的部分灰漿配成濁液,通入Cl2在一定的溫度下只得到Ca(ClO3)2與CaCl2兩種溶質,該反應的化學方程式是 。
Ⅲ、向II所得溶液中加入KCl,發生復分解反應,經蒸發濃縮,冷卻結晶,過濾得49.0克KClO3晶體,則理論上至少需要標準狀況下Cl2 升。
Ⅳ、將I中的殘渣溶于NH4Cl溶液,加熱,收集揮發出的氣體再利用。向所得CaCl2溶液中依次通入NH3、CO2,便可獲得超細CaCO3,過程如下:
①根據沉淀溶解平衡原理,解釋殘渣中難溶鹽的溶解原因 。
②CaCl2溶液中通入兩種氣體后,生成超細CaCO3的化學方程式是 。
③圖示的溶液A可循環使用,其主要成分的化學式是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com