
【題目】 “侯氏制堿法”是我國化工行業歷史長河中一顆璀璨明珠。
Ⅰ..純堿的制備:用下圖裝置制取碳酸氫鈉,再間接制得純堿。

(1)裝置乙的作用是 _________________,其中水可以用_______________代替;
(2)裝置丙中反應的化學方程式為_____________________________________;
(3)用裝置丙中產生的碳酸氫鈉制取純堿時,需要的實驗操作有:_____________。
(4)定量分析:測定純堿樣品純度
提供藥品:酚酞、甲基橙、0.1mol/LHCl溶液
實驗步驟:
①稱取樣品mg,溶于水形成100mL溶液;
②向溶液中滴加少量___________作指示劑,再向其中滴加鹽酸溶液至終點,消耗鹽酸_________VmL;
③計算:純堿樣品純度=__________________。
Ⅱ.某小組同學在0.1mol/LNaHCO3溶液中滴加酚酞溶液1滴,溶液沒有什么變化,但加熱后顯淡紅色,加熱較長時間后冷卻,紅色不褪去。為探究原因,進行了下列實驗:加熱0.1mol/LNaHCO3溶液,測得溶液pH隨溫度變化的曲線:

當溫度恢復到10℃,測得溶液 pH=11.5。
(5)依據圖像信息對下列問題做出合理猜測:
①AB段pH上升原因:____________________________________________________,
②BC段pH上升原因:____________________________________________________;
(6)設計實驗對BC段pH上升的合理猜測進行驗證(藥品任意選擇):__________________________。
【答案】
(1)除去二氧化碳中混有的氯化氫氣體 飽和碳酸氫鈉溶液 ;
(2)NH3·H2O+CO2+NaCl=NaHCO3↓+NH4Cl
(3)過濾、洗滌、灼燒
(4)酚酞 0.0106V/m (或甲基橙,(0.0084V-m)/62m)
(5)①HCO3-+H2O![]() H2CO3+OH-,△H>0;升溫促進水解平衡正向移動,pH上升
H2CO3+OH-,△H>0;升溫促進水解平衡正向移動,pH上升
②2NaHCO3![]() Na2CO3+CO2↑+H2O,溫度較高時,使得碳酸氫鈉受熱分解為碳酸鈉,溶液堿性增強
Na2CO3+CO2↑+H2O,溫度較高時,使得碳酸氫鈉受熱分解為碳酸鈉,溶液堿性增強
(6)取回復至室溫的溶液少許,向其中滴加氯化鋇溶液,產生白色沉淀,說明猜測合理。
【解析】
試題分析:Ⅰ.(1)鹽酸有揮發性,制得的CO2中混有少量HCl,故乙裝置的作用是除去二氧化碳中混有的氯化氫氣體,可以用飽和碳酸氫鈉溶液代替水吸收HCl;
(2)裝置丙是侯氏制堿原理,發生的反應方程式為NH3·H2O+CO2+NaCl=NaHCO3↓+NH4Cl;
(3)從反應后的混合物中提出不溶物需要過濾并洗滌,最后加熱灼燒使之完全分解得到純堿,具體需要的實驗操作有過濾、洗滌、灼燒;
(4)②用鹽酸滴定純堿溶液選擇酚酞作指示劑;
③滴定過程發生的反應為Na2CO3+HCl=NaHCO3+H2O,n(Na2CO3)=n(HCl)=0.1V×10-3mol,樣品的純度為![]() ×100%=0.0106V/m;
×100%=0.0106V/m;
Ⅱ.(5)①AB段pH上升原因是溶液里存在HCO3-+H2O![]() H2CO3+OH-,△H>0;升溫促進水解平衡正向移動,pH上升;
H2CO3+OH-,△H>0;升溫促進水解平衡正向移動,pH上升;
②BC段pH上升原因是碳酸氫鈉不穩定,受熱分解生成碳酸鈉,碳酸鈉的水解程度大于碳酸氫鈉,溶液堿性增強;
(6)結合碳酸鈉與碳酸氫鈉的性質差異,取回復至室溫的溶液少許,向其中滴加氯化鋇溶液,產生白色沉淀,說明溶液里含有碳酸鈉,猜測合理。


 提分百分百檢測卷系列答案
提分百分百檢測卷系列答案 寶貝計劃期末沖刺奪100分系列答案
寶貝計劃期末沖刺奪100分系列答案 能考試全能100分系列答案
能考試全能100分系列答案科目:高中化學 來源: 題型:
【題目】氯化銅、氯化亞銅是重要的化工原料,廣泛用作有機合催化劑。
已知:氯化銅容易潮解.

I.實驗室用如圖所示裝置,用還原銅粉和氯氣來制備氯化銅。
(1)石棉絨的作用是 ;B裝置中的試劑是 。E和F裝置及試劑可用_______ 替換(填裝置及所裝試劑)。
(2)當Cl2排盡空氣后,加熱D。則D中發生反應的化學方程式為 。
(3) 若實驗測得CuCl2質量分數為90.0%,則其中可能含有的雜質是 (一種即可)。
Ⅱ.另取純凈CuC l2固體用于制備CuCl。

(4)溶解時加入HCl溶液的目的主要是 (結合離子方程式回答)。
(5)若接上述操作用10. 0mol/L的HCl代替0.2mol/L HCl,通人SO2后,200. 00mL黃綠色溶液顏色褪去,但無白色沉淀。對此現象:
甲同學提出假設:c(H+)過大。
為驗證此假設,可取75.00g CuCl2固體與100mL0.2mol/LHCl及 mL9. 8mol/LH2SO4配制成200. 00mL溶液再按上述操作進行實驗。
乙同學查閱資料:體系中存在平衡2Cl-(aq)+CuCl(s)=CuCl32-(aq)。則出現此現象另一可能的原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】0.2 mol某烴A在氧氣中充分燃燒后,生成化合物B,C各1.2 mol。試回答:
(1)烴A的分子式為_____________.
(2)若取一定量的烴A完全燃燒后,生成B、C各3 mol,則有________g烴A參加了反應,燃燒時消耗標準狀況下的氧氣_____________L.
(3)若烴A不能使溴水褪色,但在一定條件下,能與氯氣發生取代反應,其一氯代物只有
一種,則烴A的結構簡式為______________.
(4)若烴A能使溴水褪色,在催化劑作用下,與H2加成,其加成產物經測定分子中含有4個甲基,烴A可能有的結構________種,任寫出其中一種烴A的結構簡式____________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海水淡化及海水資源的提取利用是當今化工行業重要課題。
回答下列問題:
(1)下列屬于海水淡化常見工藝的是________(填序號)。
①電滲析法 ②蒸餾法 ③離子交換法 ④沉淀法
(2)采用“空氣吹出法”從濃海水中吹出Br2,并用純堿吸收。堿吸收溴的主要反應是 Br2+Na2CO3+H2O→ NaBr+NaBrO3+NaHCO3,吸收1 mol Br2時,轉移的電子為________mol。
(3)海水提鎂的一段工藝流程如下圖:

濃海水的主要成分如下:

該工藝過程中,脫硫階段主要反應的離子方程式為____________________________________________,產品2 的化學式為________,1 L 濃海水最多可得到產品2 的質量為________g。
(4)采用石墨陽極、不銹鋼陰極電解熔融的氯化鎂,發生反應的化學方程式為:_______________。電解時,若有少量水存在會造成產品鎂的消耗,寫出有關反應的化學方程式:__________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用KMnO4氧化溶質質量分數為36.5%的鹽酸。反應方程式如下:
2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
(1)若此鹽酸的密度為1.2g/cm3,其物質的量濃度為_________________________;
(2)用雙線橋表示電子的得失_________________________;
(3)此反應中氧化劑是_________,氧化產物____________;
(4)若有xmolKMnO4參加反應,則轉移電子的物質的量為____________;
(5)15.8gKMnO4完全反應,產生標準狀況下Cl2的體積為_________,同時有________molHCl被氧化。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】次磷酸(H3PO2)是一種精細化工產品,具有較強還原性,回答下列問題:
(1)H3PO2是一元中強酸,寫出其電離方程式:___________。
(2)H3PO2及NaH2PO2均可將溶液中的銀離子還原為銀單質,從而可用于化學鍍銀.
①(H3PO2)中,磷元素的化合價為___________。
②利用(H3PO2)進行化學鍍銀反應中,氧化劑與還原劑的物質的量之比為4:1,則氧化產物為:___________(填化學式);
③NaH2PO2是 正鹽還是酸式鹽?___________,其溶液顯___________性(填“弱酸性”、“中性”、或者“弱堿性”)。
(3)H3PO2的工業制法是:將白磷(P4)與氫氧化鋇溶液反應生成PH3氣體和Ba(H2PO2)2,后者再與硫酸反應,寫出白磷與氫氧化鋇溶液反應的化學方程式___________。
(4)(H3PO2)也可以通過電解的方法制備.工作原理如圖所示(陽膜和陰膜分別只允許陽離子、陰離子通過):

①寫出陽極的電極反應式___________;
②分析產品室可得到H3PO2的原因___________;
③早期采用“三室電滲析法”制備H3PO2,將“四室電滲析法”中陽極室的稀硫酸用H3PO2稀溶液代替,并撤去陽極室與產品室之間的陽膜,從而合并了陽極室與產品室,其缺點是___________雜質。該雜質產生的原因是___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有A、B、C三種烴,其球棍模型下圖:

(1)等質量的以上物質完全燃燒時耗去O2的量最多的是___________(填對應字母,下同);
(2)同狀況、同體積的以上三種物質完全燃燒時耗去O2的量最多的是___________;
(3)等質量的以上三種物質燃燒時,生成二氧化碳最多的是__________________;
(4)在120℃、1.01×l05Pa下時,有兩種氣態烴和足量的氧氣混合點燃,相同條件下測得反應前后氣體體積沒有發生變化,這兩種氣體是___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】綠原酸是金銀花的主要抗菌、抗病毒有效藥理成分之一。
Ⅰ.已知綠原酸X的結構簡式為
(1)X中含氧原子的官能團的名稱為____ _。
(2)下列敘述正確的是 _。
①X的分子式為C16O20O9
②1molX最多能與4mol H2發生加成反應
③X能與碳酸氫鈉溶液反應,且能使酸性高錳酸鉀褪色
④1molX最多能與5mol NaOH反應
⑤綠原酸水解后所得兩產物碳原子數之差為2
Ⅱ.綠原酸在一定條件下可合成D和對羥基苯甲酸兩種醫藥中間體,其合成路線如下(部分反應條件未注明):

已知:R—![]() —R
—R![]() 2R—CHO
2R—CHO
(1) D是一種芳香族化合物,D的結構簡式為 ;
(2)A→C的反應類型是 ;
(3)由B生成E的化學方程式為 ;
(4)F與E互為同分異構體,且F同時滿足下列條件:
①遇氯化鐵溶液顯紫色
②能發生銀鏡反應
③核磁共振氫譜為4組峰,且面積比為2:2:1:1,則F的結構共有 種(不考慮立體異構),結構簡式為 (任寫一種)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】丁烷催化裂解生成烷烴和烯烴,可按下列兩種方式進行:C4H10→C2H4+C2H6;C4H10→C H4+C3H6某化學興趣小組為了測定丁烷裂解氣中CH4和C2H6的比例關系,設計實驗如下圖所示:
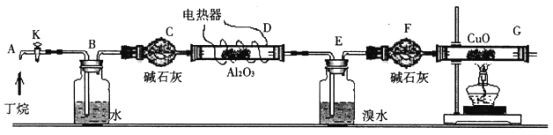
如圖連接好裝置后,需進行的操作有:①給D、G裝置加熱;②檢查整套裝置的氣密性;③排出裝置中的空氣等……
注:CuO能將烴氧化成CO2和H2O;Al2O3是烷烴裂解的催化劑;G后面裝置已省略。
(1)這三步操作的先后順序是_________(填序號)
(2)簡要敘述證明空氣已排盡的操作方法______________________。
(3)假定丁烷完全裂解,且流經各裝置中的氣體能完全反應。當裝置E和F的總質量比反應前增加了0.7g,G裝置中固體質量比反應前減少了1.76g,則在丁烷的裂解產物中CH4和C2H6的物質的量之比n(CH4):n(C2H6)=______________。
(4)若對實驗后E裝置中的混合物再按以下流程進行實驗:

![]()
①分離操作I、Ⅱ的名稱分別是:I、_____________,Ⅱ、____________。
②Na2SO3溶液的作用是______________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com