
SO2和NOx在化學(xué)工業(yè)上有重要用途,也是大氣污染的主要來源,開發(fā)和利用并重,預(yù)防和治理并舉是當(dāng)前工業(yè)上和環(huán)境保護(hù)領(lǐng)域研究的主要課題之一。
(1)在接觸法制硫酸的過程中,發(fā)生2SO2(g)+O2(g)  2SO3(g) △H<0反應(yīng),某溫度下,SO2的平衡轉(zhuǎn)化率(α)與體系總壓強(qiáng)(p)的關(guān)系如下圖所示,根據(jù)圖示回答下列問題:
2SO3(g) △H<0反應(yīng),某溫度下,SO2的平衡轉(zhuǎn)化率(α)與體系總壓強(qiáng)(p)的關(guān)系如下圖所示,根據(jù)圖示回答下列問題: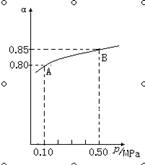
①平衡狀態(tài)由A到B時,平衡常數(shù)K(A) K(B)(填“>”、“<”或“=”);
②將2.0molSO2和1.0molO2置于10L的密閉容器中,若40s后反應(yīng)達(dá)到平衡,此時體系總壓強(qiáng)為0.10MPa,這一段時間內(nèi)SO2的平均反應(yīng)速率為 。
該反應(yīng)的平衡常數(shù)為 。
(2)用CH4催化還原NOx可消除氮的氧化物的污染,例如:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol—1
取標(biāo)準(zhǔn)狀況下4.48LCH4并使之完全反應(yīng):
①若將NO2還原至N2,整個過程中轉(zhuǎn)移電子的物質(zhì)的量為 ;
②若還原NO2和NO的混合物,放出的總熱量Q的取值范圍是 。
(1)①=;(1分)②0.0040mol·L-1·s-1,800L·mol-1;(共4分,各2分,無單位或錯誤扣1分)(2)①1.6mol(2分,無單位扣1分)②173.4kJ<Q<232kJ(3分)
解析試題分析:(1)平衡常數(shù)只受溫度的影響,溫度不變,則壓強(qiáng)不變,平衡狀態(tài)由A變到B時,則k(A)=k(B);(2)由圖象知,體系總壓強(qiáng)為0.10MPa時SO2的平衡轉(zhuǎn)化率為0.8,則
2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
起始:2.0mol 1.0mol 0
轉(zhuǎn)化:1.6mol 0.8mol 1.6mol
平衡:0.4mol 0.2mol 1.6mol
則平衡時:c(SO2)=0.04mol/L,c(O2)=0.02mol/L,c(SO3)=0.16mol/L,SO2的平均反應(yīng)速率為1.6mol/10L/40s=0.0040mol·L-1·s-1,K=c(SO3)2/c(SO2)2·c(O2)=(0.16)2/(0.04)2×0.02=800;(2)①CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H="-1160kJ/mol" 利用蓋斯定律將①+②/2可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=-867kJ/moln(CH4)=4.48L/22.4L/mol=0.2mol,整個過程中轉(zhuǎn)移的電子總數(shù)為:0.20mol×8=1.60mol,放出的熱量為:0.2mol×867kJ/mol=173.4kJ。②上述可知,若反應(yīng)物中全部是為二氧化氮,放出的熱量為173.4kJ。根據(jù)蓋斯定律可據(jù)算出若全部為一氧化氮放出熱量為232kJ,故放出的熱量范圍是173.4kJ<Q<232kJ。
考點(diǎn):蓋斯定律,化學(xué)平衡常數(shù),化學(xué)平衡。



| 年級 | 高中課程 | 年級 | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:填空題
應(yīng)用化學(xué)反應(yīng)原理知識解決下列問題
(1)某溫度下純水中c (H+) = 2.0×10-7 mol·L-1,則此純水中的c (OH-) = 。
(2)將某CH3COOH溶液稀釋10倍,則稀釋后的溶液中c(H+) 原來的十分之一(填“大于”、“小于”或“等于”)。
(3)0.1 mol·L-1的下列溶液①HCl、②CH3COOH、③CH3COONa、④FeCl3、⑤NaOH,其中pH最大的是 (填序號);實(shí)驗(yàn)室配制的氯化鐵溶液顯弱酸性的原因: (用離子方程式表示)。
(4)一定條件下22g二氧化碳?xì)怏w與足量氫氣反應(yīng)生成氣態(tài)甲醇(CH3OH)和水蒸氣時,放出247.5kJ熱量,其反應(yīng)的熱化學(xué)方程式為 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
工業(yè)上用CO生產(chǎn)燃料甲醇。一定溫度和容積條件下發(fā)生反應(yīng):CO(g)+2H2(g) CH3OH(g)。圖1表示反應(yīng)中的能量變化;圖2表示一定溫度下,在體積為1L的密閉容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的濃度隨時間變化。
CH3OH(g)。圖1表示反應(yīng)中的能量變化;圖2表示一定溫度下,在體積為1L的密閉容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的濃度隨時間變化。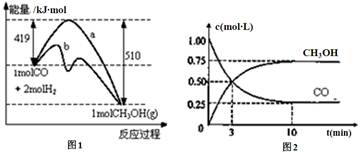
請回答下列問題:
(1)在“圖1”中,曲線 (填“a”或“b”)表示使用了催化劑;沒有使用催化劑時,在該溫度和壓強(qiáng)條件下反應(yīng)CO(g)+2H2(g) CH3OH(g)的△H= 。
CH3OH(g)的△H= 。
(2)下列說法正確的是
A.起始充入的CO的物質(zhì)的量為1mol
B.增加CO的濃度,H2的轉(zhuǎn)化率會增大
C.容器中壓強(qiáng)恒定時,反應(yīng)達(dá)到平衡狀態(tài)
(3)從反應(yīng)開始到建立平衡,v(CO)= ;達(dá)到平衡時,c(H2)= ,該溫度下CO(g)+2H2(g)  CH3OH(g)的化學(xué)平衡常數(shù)為 。達(dá)到平衡后若保持其它條件不變,將容器體積壓縮為0.5L,則平衡 移動 (填“正向”、“逆向”或“不”)。
CH3OH(g)的化學(xué)平衡常數(shù)為 。達(dá)到平衡后若保持其它條件不變,將容器體積壓縮為0.5L,則平衡 移動 (填“正向”、“逆向”或“不”)。
(4)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g);ΔH=-193kJ/mol
又知H2O(l)= H2O(g);ΔH=+44 kJ/mol,請寫出32g的CH3OH(g)完全燃燒生成液態(tài)水的熱化學(xué)方程式 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
霧霾已經(jīng)嚴(yán)重影響我們的生存環(huán)境。火力發(fā)電廠釋放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等氣體會造成環(huán)境污染。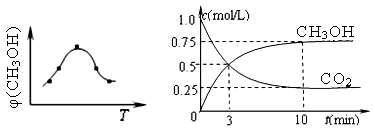
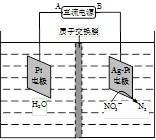
圖22-1 圖22-2 圖22-3
(1)利用甲烷催化還原NOx:
①CH4(g) + 4NO2(g) =" 4NO(g)" + CO2(g) + 2H2O(g) △H1=-574kJ?mol-1
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) △H2=-1160kJ?mol-1
甲烷直接將NO2還原為N2的熱化學(xué)方程式為 。
(2)將CO2轉(zhuǎn)化為甲醇的熱化學(xué)方程式為:
CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) △H3
①取五份等體積CO2和H2的混合氣體(物質(zhì)的量之比均為1∶3),分別加入溫度不同、容積相同的恒容密閉容器中,發(fā)生上述反應(yīng),反應(yīng)相同時間后,測得甲醇的體積分?jǐn)?shù)φ(CH3OH) 與反應(yīng)溫度T的關(guān)系曲線(見圖22-1),則上述CO2轉(zhuǎn)化為甲醇反應(yīng)的△H3 0(填“>”、“<”或“=”)。
②在一恒溫恒容密閉容器中充入1mol CO2和3mol H2,進(jìn)行上述反應(yīng)。測得CO2和CH3OH(g)的濃度隨時間變化如圖22-2所示。
下列說法正確的是 (填字母代號)。
| A.第10min后,向該容器中再充入1molCO2和3molH2,則再次達(dá)到平衡時c(CH3OH) ="1.5" mol/L |
| B.達(dá)到平衡時,氫氣的轉(zhuǎn)化率為0.75 |
| C.0~10分鐘內(nèi),氫氣的平均反應(yīng)速率為0.075mol/(L?min) |
| D.該溫度下,反應(yīng)的平衡常數(shù)的值為3/16 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
生物質(zhì)能是一種潔凈、可再生能源。生物質(zhì)氣(主要成分為 CO、CO2、H2等)與H2混合,催化合成甲醇和二甲醚(CH3OCH3)及許多烴類物質(zhì)等,是生物質(zhì)能利用的方法之一.
(1)已知碳的氣化反應(yīng)在不同溫度下平衡常數(shù)的對數(shù)值(lgK)如下表: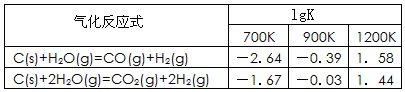
反應(yīng):CO(g)+H2O(g)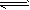 CO2(g)+H2(g),該反應(yīng)的△H________0(選填:“>”、“<”、“=”);在900K時,該反應(yīng)平衡常數(shù)的對數(shù)值(lgK)=_____________.
CO2(g)+H2(g),該反應(yīng)的△H________0(選填:“>”、“<”、“=”);在900K時,該反應(yīng)平衡常數(shù)的對數(shù)值(lgK)=_____________.
(2)甲醇是一種重要的能源和化工原料,工業(yè)上合成甲醇的反應(yīng)為:CO+2H2?CH3OH.現(xiàn)已知:H2(g)、CO(g)、CH3OH(l)的燃燒熱ΔH分別為-285.8KJ/mol、-283.0KJ/mol和-726.5KJ/mol。則:CH3OH不完全燃燒生成CO和液態(tài)H2O的熱化學(xué)反應(yīng)方程式 .
(3)在一定溫度、壓強(qiáng)和催化條件下,工業(yè)上用CO和H2反應(yīng)生成二甲醚,同時產(chǎn)生一種參與大氣循環(huán)的無機(jī)物。則該反應(yīng)的化學(xué)反應(yīng)方程式為: .
(4)下圖左為綠色電源“二甲醚燃料電池”的工作原理示意圖.a(chǎn)電極上發(fā)生反應(yīng)的電極反應(yīng)式為 .
(5)連接下圖右裝置的電源為(4)問中的二甲醚燃料電池。接通電源一段時間后,觀察到裝置中電解質(zhì)溶液顏色由無色變?yōu)樗{(lán)色,并逐漸加深。則該裝置中的Cu電極應(yīng)與二甲醚燃料電池中 電極(填a或b)相連。通電時發(fā)生反應(yīng)的總的離子反應(yīng)方程式為: .
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(1)在298K時,1mol C2H6 在氧氣中完全燃燒生成CO2和液態(tài)水,放出熱量1558.3kJ。寫出該反應(yīng)的熱化學(xué)方程式 。
(2)利用該反應(yīng)設(shè)計一個燃料電池:用KOH溶液作電解質(zhì)溶液,多孔石墨作電極,在電極上分別通入乙烷和氧氣。通入乙烷氣體的電極應(yīng)為 極(填“正”或“負(fù)”),該電極上發(fā)生的電極反應(yīng)式為 。
(3)在右圖所示實(shí)驗(yàn)裝置中,石墨棒上的電極反應(yīng)式為 。如果起始時盛有1L pH=5的CuSO4溶液(25℃,CuSO4足量),一段時間后溶液的pH變?yōu)?,此時可觀察到的現(xiàn)象是 。若要使溶液恢復(fù)到起始濃度(溫度不變,忽略溶液體積的變化),可向溶液中加入 (填物質(zhì)名稱),其質(zhì)量約為 。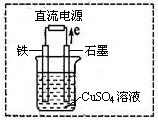
(4)將普通碳鋼釘放入“84消毒液”(NaClO溶液)中浸泡一段時間。預(yù)期的實(shí)驗(yàn)現(xiàn)象是 。
(5)為了進(jìn)一步探究碳鋼釘在該消毒液(NaClO)中的腐蝕原理,某同學(xué)設(shè)計了如圖所示實(shí)驗(yàn)裝置,寫出碳(C)極上發(fā)生的電極反應(yīng)式 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
常溫常壓下,斷裂1mol(理想)氣體分子化學(xué)鍵所吸收的能量或形成1mol(理想)氣體分子化學(xué)鍵所放出的能量稱為鍵能(單位為kJ.mol-1)下表是一些鍵能數(shù)據(jù)(kJ·mol-1)
| 化學(xué)鍵 | 鍵能 | 化學(xué)鍵 | 鍵能 | 化學(xué)鍵 | 鍵能 |
| C-F | 427 | C-Cl | 330 | C-I | 218 |
| H-H | 436 | S=S | 255 | H-S | 339 |
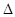 H1=" +1175.7" kJ·mol-1
H1=" +1175.7" kJ·mol-1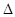 H2= —771.1 kJ·mol-1
H2= —771.1 kJ·mol-1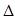 H3=" +482.2" kJ·mol-1
H3=" +482.2" kJ·mol-1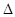 H="_____________" kJ·mol-1。
H="_____________" kJ·mol-1。查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
把煤作為燃料可通過下列兩種途徑:
途徑I:C(s) +O2 (g)=CO2(g) △H1<0 ①
途徑II:先制成水煤氣:C(s) +H2O(g)=CO(g)+H2(g) △H2>0 ②
再燃燒水煤氣:2CO(g)+O2 (g)=2CO2(g) △H3<0 ③
2H2(g)+O2 (g)=2H2O(g) △H4<0 ④
請回答下列問題:
(1)途徑I放出的熱量 ( 填“大于”“等于”或“小于”) 途徑II放出的熱量,原因是 。
(2)△H1、△H2、△H3、△H4的數(shù)學(xué)關(guān)系式是 。
(3)12g炭粉在氧氣中不完全燃燒生成一氧化碳,放出110.35kJ熱量。其熱化學(xué)方程式為 。
(4)煤炭作為燃料采用途徑II的優(yōu)點(diǎn)有
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
據(jù)報道,一定條件下由二氧化碳和氫氣合成乙醇已成為現(xiàn)實(shí)。
已知:①CH3CH2OH(l)+3 O2 (g)=2CO2(g)+3H2O(l) △H="-1366.8" kJ/mol
②2H2 (g)+O2 (g)=2H2O(l) △H="-571.6" kJ/mol
(1)寫出由CO2和H2 反應(yīng)合成CH3CH2OH (l)和H2O(l)的熱化學(xué)方程式 。
(2)堿性乙醇燃料電池易儲存,易推廣,對環(huán)境污染小,具有非常廣闊的發(fā)展前景。該燃料電池中,使用鉑作電極,KOH溶液做電解質(zhì)溶液。通入乙醇燃?xì)獾囊粯O為 極,該極上的電極反應(yīng)式為 。
(3)用乙醇燃料電池電解400 mL 飽和食鹽水裝置可簡單表示如下圖: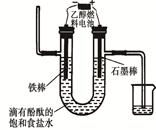
該裝置中發(fā)生電解反應(yīng)的方程式為 ;在鐵棒附近觀察到的現(xiàn)象是 ;當(dāng)陰極產(chǎn)生448 mL氣體(體積在標(biāo)準(zhǔn)狀況下測得)時,停止電解,將電解后的溶液混合均勻,溶液的pH為 。(不考慮氣體的溶解及溶液體積的變化)
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com