(2011?南平二模)火力發(fā)電廠釋放出大量的氮氧化物(NO
x)、二氧化硫和二氧化碳等氣體會(huì)造成環(huán)境污染.對(duì)燃煤廢氣進(jìn)行脫硝、脫硫和脫碳等處理,可實(shí)現(xiàn)綠色環(huán)保、節(jié)能減排、廢物利用等目的.
(1)脫硝.利用甲烷催化還原NO
x:
CH
4(g)+4NO
2(g)=4NO(g)+CO
2(g)+2H
2O(g)
△H
1=-574kJ?mol
-1CH
4(g)+4NO(g)=2N
2(g)+CO
2(g)+2H
2O(g)
△H
2=-1160kJ?mol
-1甲烷直接將NO
2還原為N
2的熱化學(xué)方程式為
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
.
(2)脫碳.將CO
2轉(zhuǎn)化為甲醇的熱化學(xué)方程式為:CO
2(g)+3H
2(g)?CH
3OH(g)+H
2O(g)△H
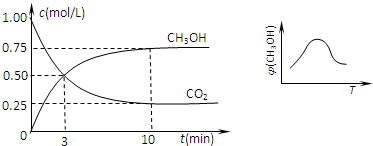
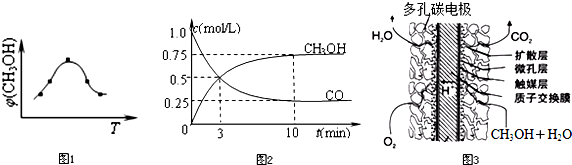
3①取五份等體積CO
2和H
2的混合氣體(物質(zhì)的量之比均為1:3),分別加入溫度不同、容積相同的恒容密閉容器中,發(fā)生上述反應(yīng),反應(yīng)相同時(shí)間后,測(cè)得甲醇的體積分?jǐn)?shù)φ(CH
3OH) 與反應(yīng)溫度T的關(guān)系曲線如圖所示,則φ(CH3OH)T上述CO
2轉(zhuǎn)化為甲醇的反應(yīng)的△H
3<
<
0(填“>”、“<”或“=”).
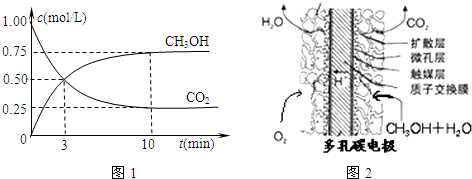
②在一恒溫恒容密閉容器中充入1mol CO
2和3mol H
2,進(jìn)行上述反應(yīng).測(cè)得CO
2和CH
3OH(g)的濃度隨時(shí)間變化如下圖所示.下列說法正確的是
CE
CE
(填字母代號(hào)).
A.第10min后,向該容器中再充入1mol CO
2和3mol H
2,則再次達(dá)到平衡時(shí)c(CH
3OH)=1.5mol?L
-1B.0~10min內(nèi),氫氣的平均反應(yīng)速率為0.075mol/(L?min)
C.達(dá)到平衡時(shí),氫氣的轉(zhuǎn)化率為0.75
D.該溫度下,反應(yīng)的平衡常數(shù)的值為3/16
E.升高溫度將使n(CH
3OH)/n(CO
2)減小
③甲醇燃料電池結(jié)構(gòu)如下圖所示.其工作時(shí)正極的電極反應(yīng)式可表示為
O2+4e-+4H+=2H2O
O2+4e-+4H+=2H2O
.
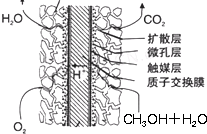
多孔碳電極
(3)脫硫.某種脫硫工藝中將廢氣經(jīng)處理后,與一定量的氨氣、空氣反應(yīng),生成硫酸銨和硝酸銨的混合物作為副產(chǎn)品化肥.設(shè)煙氣中的SO
2、NO
2的物質(zhì)的量之比為1:1,則該反應(yīng)的化學(xué)方程式為
12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3
12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3
.
(4)硫酸銨和硝酸銨的水溶液的pH<7,其中原因可用一個(gè)離子方程式表示為:
NH
4++H
2O

NH
3?H
2O+H
+NH
4++H
2O

NH
3?H
2O+H
+;在一定物質(zhì)的量濃度的硝酸銨溶液中滴加適量的NaOH溶液,使溶液的pH=7,則溶液中c(Na
+)+c(H
+)
<
<
c(NO
3-)+c(OH
-)(填寫“>”“=”或“<”)




 (2011?南平二模)火力發(fā)電廠釋放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等氣體會(huì)造成環(huán)境污染.對(duì)燃煤廢氣進(jìn)行脫硝、脫硫和脫碳等處理,可實(shí)現(xiàn)綠色環(huán)保、節(jié)能減排、廢物利用等目的.
(2011?南平二模)火力發(fā)電廠釋放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等氣體會(huì)造成環(huán)境污染.對(duì)燃煤廢氣進(jìn)行脫硝、脫硫和脫碳等處理,可實(shí)現(xiàn)綠色環(huán)保、節(jié)能減排、廢物利用等目的.
 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+