
黃鐵礦(主要成分為FeS2)是工業制取硫酸的重要原料,其燃燒產物為SO2和Fe2O3。
(1)已知1g FeS2完全燃燒放出7.1kJ熱量,則表示FeS2完全燃燒反應的熱化學方程式為:
______________________________________________________________。
(2)將0.050molSO2(g)和0.030molO2(g)放入容積為1L的密閉容器中,反應:2SO2(g)+O2(g)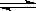 2SO3(g) 在一定條件下達到平衡,測得c(SO3)=0.040mol/L。則該條件下反應的平衡常數K的數值為___________,SO2的平衡轉化率為__________。
2SO3(g) 在一定條件下達到平衡,測得c(SO3)=0.040mol/L。則該條件下反應的平衡常數K的數值為___________,SO2的平衡轉化率為__________。
(3)當該反應處于平衡狀態時,欲使平衡向正反應方向移動且反應速率加快,下列措施可行的是 。(填字母)
| A.向平衡混合物中充入Ar | B.向平衡混合物中充入O2 |
| C.改變反應的催化劑 | D.降低反應的溫度 |
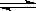 2SO3(g) △H<0 , SO2的轉化率在起始溫度T1=673K下隨反應時間(t)的變化如下圖,其他條件不變,僅改變起始溫度為T2=723K,請在圖中畫出溫度T2下SO2的轉化率隨反應時間變化的預期結果示意圖。
2SO3(g) △H<0 , SO2的轉化率在起始溫度T1=673K下隨反應時間(t)的變化如下圖,其他條件不變,僅改變起始溫度為T2=723K,請在圖中畫出溫度T2下SO2的轉化率隨反應時間變化的預期結果示意圖。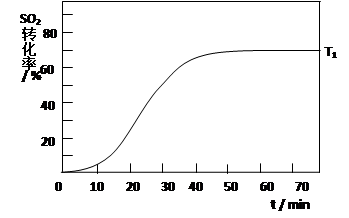
(1)4FeS2(s)+11O2(g) 2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol (2分)
2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol (2分)
(2)K=1.6×103(2分) 80% (2分) (3)B(1分,多選不得分) 
解析試題分析:(1)FeS2完全燃燒燃燒的化學方程式是4FeS2+11O2 2Fe2O3+8SO2,由于1g FeS2完全燃燒放出7.1kJ熱量,則4molFeS2完全燃燒放出的熱量是7.1kJ×120×4=3408kJ,所以該反應的熱化學方程式是4FeS2(s)+11O2(g)
2Fe2O3+8SO2,由于1g FeS2完全燃燒放出7.1kJ熱量,則4molFeS2完全燃燒放出的熱量是7.1kJ×120×4=3408kJ,所以該反應的熱化學方程式是4FeS2(s)+11O2(g) 2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol。
2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol。
(2) 2SO2(g)+O2(g)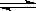 2SO3(g)
2SO3(g)
起始濃度(mol/L) 0.050 0.030 0
轉化濃度(mol/L) 0.040 0.020 0.040
平衡濃度(mol/L) 0.010 0.010 0.040
所以該溫度下平衡常數K=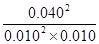 =1600
=1600
SO2的平衡轉化率=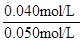 ×100%=80%
×100%=80%
(3)向平衡混合物中充入Ar,容器容積不變,濃度不變,反應速率和平衡狀態不變,A不正確;向平衡混合物中充入O2,增大反應物的濃度,反應速率增大,平衡向正反應方向移動,B正確;改變反應的催化劑平衡狀態不變,C不正確;降低反應的溫度,平衡向正反應方向移動,但反應速率降低,D不正確,答案選B。
(4)溫度高反應速率快,到達平衡的時間減少。由于正反應是放熱反應,所以溫度高不利于平衡向正反應方向進行,SO2的轉化率降低,因此正確的圖像是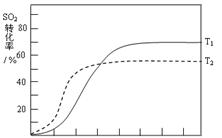 。
。
考點:考查熱化學方程式的書寫、平衡常數和轉化率的計算、外界條件對反應速率和平衡狀態的判斷以及可逆反應圖像的分析和判斷
點評:該題是高考中的常見考點和題型,屬于中等難度試題的考查,試題綜合性強,側重對學生能力的培養和解題方法的指導與訓練,旨在考查學生靈活運用基礎知識解決實際問題的能力,有利于培養學生的邏輯推理能力和發散思維能力,提升學生的學科素養。


科目:高中化學 來源: 題型:填空題
能源是現代社會發展的支柱之一。
(1)化學反應中的能量變化,通常主要表現為熱量的變化。
①下列反應中,屬于放熱反應的是___________(填序號)。
a. Ba(OH)2·8H2O與NH4Cl混合攪拌
b. 高溫煅燒石灰石
c. 鋁與鹽酸反應
②某同學進行如下圖所示實驗,測量稀鹽酸與燒堿溶液中和反應的能量變化。實驗表明:反應溫度升高,由此判斷該反應是_______(填“吸熱”或“放熱”)反應,其離子方程式是_______________。
(2)電能是現代社會應用最廣泛的能源之一。
下圖所示的原電池裝置中,其負極是_____________________,正極上能夠觀察到的現象是____________________________,正極的電極反應式是_________________________。
原電池工作一段時間后,若消耗鋅6.5g,則放出氣體__________g。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(I某氮肥廠氨氮廢水中的氮元素多以NH4+和NH3·H2O的形式存在。在微生物作用下,NH4+經過兩步反應被氧化成NO3-,兩步反應的能量變化示意圖如下: 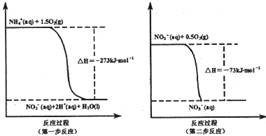
(1)1 mo1NH4+(aq)全部氧化成NO3-(aq)的熱化學方程式是 _ 。
(2)在一定條件下,向廢水中加入CH3OH,將HNO3還原成 N2,若該反應消耗32gCH3OH轉移6mol電子,則參加反應的還原劑和氧化劑的物質的量之比是_ 。
(B)超音速飛機在平流層飛行時,尾氣中的NO會破壞臭氧層。科學家正在研究利用催化技術
將尾氣中的NO和CO轉變成CO2和N2,化學方程式如下:2NO十2CO 2CO2+ N2 △H
2CO2+ N2 △H
某溫度下用氣體傳感器測得不同的時間的NO和CO濃度如下表: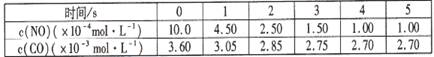
請回答下列問題(均不考慮溫度變化對催化劑催化效率的影響):
(1)在上述條件下反應能夠自發進行,則反應的△H 0(填寫“>”、“<”、“=”)
(2)在該溫度下,反應的平衡常數K= (只寫出計算結果);
(3)某同學設計了三組實驗,分別驗證溫度、催化劑比表面積對化學反應速率的影響規律,
部分實驗條件如下表:
該同學畫出了表中三個實驗條件下,混合氣體中NO濃度隨時間變化的趨勢曲線圖,請在圖上標明各條曲線的實驗編號; 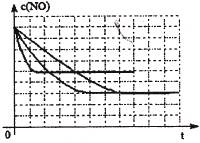
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業碳酸鈉(純度約為98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42—等雜質,提純工藝線路如圖所示:
Ⅰ.碳酸鈉的飽和溶液在不同溫度下析出的溶質如圖所示: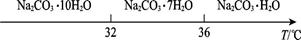
Ⅱ.有關物質的溶度積如下
| 物質 | CaCO3 | MgCO3 | Ca(0H)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
 Na2CO3(s)+10H2O(g)
Na2CO3(s)+10H2O(g) ="+532.36" kJ·mol-1
="+532.36" kJ·mol-1 Na2CO3·H2O(s)+9H2O(g)
Na2CO3·H2O(s)+9H2O(g)  ="+473.63" kJ·mol-1
="+473.63" kJ·mol-1查看答案和解析>>
科目:高中化學 來源: 題型:填空題
研究NO2.SO2.CO等大氣污染氣體的處理具有重要意義。
(1)NO2可用水吸收,也可用NH3處理,也可用CH4催化還原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用標準狀況下2.24L CH4還原NO2至N2整個過程中轉移的電子總數為______(阿伏加德羅常數的值用NA表示),放出的熱量為______kJ。
(2)已知:2SO2(g)+O2(g) 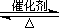 2SO3(g) ?H=-196.6 kJ·mol-1
2SO3(g) ?H=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ?H=-113.0 kJ·mol-1
2NO2(g) ?H=-113.0 kJ·mol-1
(ⅰ)則反應NO2(g)+SO2 (g) SO3(g)+NO(g)的?H= kJ·mol-1。
SO3(g)+NO(g)的?H= kJ·mol-1。
(ⅱ)一定條件下,將NO2與SO2以體積比1:2置于密閉容器中發生上述反應,下列能說明反應達到平衡狀態的是 。
A.每消耗1 mol SO3的同時生成1 mol NO2 B.體系壓強保持不變
C.混合氣體顏色保持不變 D. SO3和NO的體積比保持不變
(ⅲ)某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖(左)所示。
平衡狀態由A變到B時.平衡常數K(A)_______K(B)(填“>”.“<”或“=”)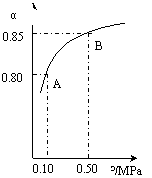
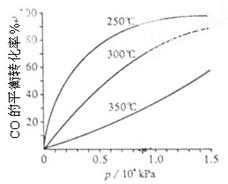
(3)CO可用于合成甲醇,反應方程式為CO(g)+2H2(g) CH3OH(g)。CO在不同溫度下的平衡轉化率與壓強的關系如上圖(右)所示。該反應?H 0(填“>”或“ <”)。
CH3OH(g)。CO在不同溫度下的平衡轉化率與壓強的關系如上圖(右)所示。該反應?H 0(填“>”或“ <”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氮是地球上含量豐富的原子元素,氮及其化合物在工農業生產、生活中有著重要作用。
(1)25℃時,0.1mol/LNH4NO3溶液中水的電離程度 (填“大于”、“等于”或“小于”) 0.1mol/L NaOH溶液中水的電離程度。
(2)若將0.1mol/L NaOH溶液和0.2mol/LNH4NO3溶液等體積混合,混合溶液中2c(NH4+)>c(NO3-),所得溶液中離子濃度由大到小的順序是 。
(3)發射火箭時肼(N2H4)為燃料,二氧化氮作氧化劑,兩者反應生成氮氣和氣態水。經測定16g氣體在上述反應中放出284kJ的熱量。則該反應的熱化學方程式是 。
(4)下圖是1mol NO2和1mol CO反應生成CO2和NO過程中能量變化示意圖。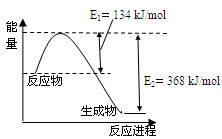
已知:N2(g)+O2(g)=2NO(g) △H=+180kJ/mol
2NO (g)+O2(g)=2NO2(g) △H=-112.3kJ/mol
則反應:2NO(g)+2CO(g) N2(g)+2CO2(g)的△H是 。
N2(g)+2CO2(g)的△H是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
⑴20世紀30年代,Eyring和Pzer在碰撞理論的基礎上提出化學反應的過渡態理論:化學反應并不是通過簡單的碰撞就能完成的,而是在反應物到生成物的過程中經過一個高能量的過渡態。如圖⑴所示是NO2和CO反應生成CO2和NO過程中的能量變化示意圖,說明這個反應是 (填“吸熱”或“放熱”)反應,NO2和CO的總能量 (填“>”、“<”或“=”)CO2和NO的總能量。

⑵某溫度時,在一個2 L的密閉容器中,X、Y、Z三種物質物質的量隨時間的變化曲線如圖⑵所示。根據圖中數據,試填寫下列空白:
①該反應在 min時達到平衡狀態(反應限度);
②該反應的化學方程式為: ;
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(16分)最近全國各地持續出現霧霾天氣,其首要污染物是可吸入顆粒物PM2.5和氮、硫的氧化物(PM2.5直徑接近2.5×10-6m,1納米=10-9m),主要來源為工業廢氣、機動車尾氣等。因此對PM2.5、SO2、NOx進行研究、處理意義重大。
(1) 下列關于PM2.5說法正確的是
a.PM2.5在空氣中形成了膠體;
b.PM2.5表面積大,能吸附大量有毒、有害物質;
c.少開私家車,盡量選擇公交、地鐵出行,某種程度可以減少PM2.5污染
(2) 取PM2.5樣本用蒸餾水處理制得試樣,若測得該試樣所含水溶性無機離子及其平均
濃度如下表
| 離子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 濃度/ mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
 2NO(g) △H=+180.5kJ·mol-1
2NO(g) △H=+180.5kJ·mol-1  2CO(g) △H ="-" 221.0 kJ·mol-1
2CO(g) △H ="-" 221.0 kJ·mol-1 CO2( g) △H ="-" 393.5 kJ·mol-1
CO2( g) △H ="-" 393.5 kJ·mol-1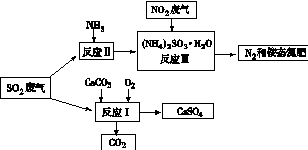
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
工業合成氨的反應為:N2(g)+3H2(g) 2NH3(g) △H <0
2NH3(g) △H <0
某實驗將3.0 mol N2(g)和4. 0 mol H2(g)充入容積為10L的密閉容器中,在溫度T1下反應。測得H2的物質的量隨反應時間的變化如下圖所示。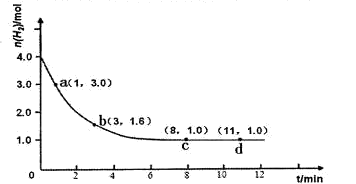
(1)反應開始3min內,H2的平均反應速率為 。
(2)計算該條件下合成氨反應的化學平衡常數(寫出計算過程,結果保留2位有效數字)。
(3)僅改變溫度為T2 ( T2小于TI)再進行實驗,請在答題卡框圖中畫出H2的物質的量隨反應時間變化的預期結果示意圖。
(4)在以煤為主要原料的合成氨工業中,原料氣氫氣常用下述方法獲得:
①C+H2O(g)  CO+H2;②CO+H2O(g)
CO+H2;②CO+H2O(g)  CO2+H2;
CO2+H2;
已知:CO(g)+1/2O2(g)=CO2(g) △H=—283.0kJ/mol
H2(g)+1/2O2(g)=H2O(g) △H=—241.8kJ/mol
寫出上述CO與H2O(g)反應的熱化學方程式: 。
(5)合成氨工業中,原料氣(N2、H2混有少量CO、NH3)在進入合成塔之前,用醋酸二氨合銅(I)溶液來吸收CO,其反應為:
CH3COO[Cu(NH3)2]+CO+NH3 CH3COO[Cu(NH3)3]?CO △H<0
CH3COO[Cu(NH3)3]?CO △H<0
寫出提高CO吸收率的其中一項措施: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com