
【題目】下列分散系中,分散質微粒直徑最小的是( )
A.氫氧化鐵膠體B.蛋白質溶液
C.石灰乳D.硝酸鉀溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】下列對化學反應熱現象的說法正確的是( )
A.放熱反應發生時不必加熱
B.化學反應的熱效應數值與參加反應的物質的多少無關
C.吸熱反應加熱后才能發生
D.化學反應一定有能量變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含1 mol HNO3的稀硝酸分別與不同質量的鐵粉反應,所得氧化產物與鐵粉物質的量的關系如圖所示(已知稀硝酸的還原產物只有NO),回答下列問題:
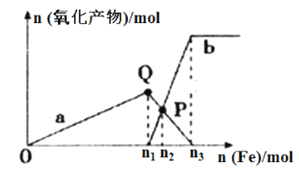
(1)曲線a表示_______________;曲線b表示_____________(填寫Fe2+或Fe3+)。
(2)P點時總反應的離子方程式可表示為_______________________。
(3)n3︰n2=________________(請寫出計算過程)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I現有①BaCl2、②金剛石、③KOH、④Na2SO4、⑤干冰、⑥碘片六種物質,按下列要求回答:
(1)熔化時不需要破壞化學鍵的是________(填寫物質的序號,下同),熔化時需要破壞共價鍵的是________。
(2)屬于離子化合物的是______________,只有離子鍵的物質是________。
(3)①的電子式是______________,⑤的電子式是_____________。
II下列粒子(分子或離子)均含有18個電子:
粒子 | A+ | B2- | C | D | E | F |
組成特點 | 單核離子 | 化合物,雙核分子 | 單質, 雙核分子 | 化合物,三核分子 | 化合物, 四核分子 | |
請回答下列問題:
(1)A的元素符號是____________,B2-的結構示意圖是________。
(2)C的結構式為__________,已知D的單質與水反應可生成氧氣及一種酸,寫出該反應的化學方程式:________________________________________
(3)E的電子式是____________________;F的水溶液常用于消毒劑,F的化學式是___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】草酸(H2C2O4)是一種二元弱酸。常溫下向H2C2O4溶液中滴加NaOH溶液,混合溶液里lgX[X表示![]() 或
或![]() ]隨pH的變化關系如圖所示。下列說法不正確的是
]隨pH的變化關系如圖所示。下列說法不正確的是

A. 直線I中X表示的是![]()
B. 直線I、Ⅱ的斜率均為1
C. c(HC2O4-)>c(C2O42-)>c(H2C2O4)對應1.22<pH<4.19
D. c(Na+)=c(HC2O4-)+2c(C2O42-)對應pH=7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究和深度開發CO、CO2的應用對構建生態文明社會具有重要的意義。回答下列問題:
I.CO可用于高爐煉鐵,已知
Fe3O4(s)+4CO(g)====3Fe(s)+4CO2(g) △H1 =a kJ/ mol
3Fe2O3(s)+CO(g)====2Fe3O4 (s)+CO2(g) △H2=bkJ/mol
則反應Fe2O3(s)+3CO(g)====2Fe(s)+3CO2(g)的△H3=_________kJ/mol(用含a、b的代數式表示)
Ⅱ.一定條件下,CO2和CO可以互相轉化。
(1)某溫度下,在容積為2L的密閉容器按甲、乙兩種方式投入反應物發生反應:CO2(g)+H2(g) ![]() CO(g)+H2O(g)。
CO(g)+H2O(g)。
甲容器15min后達到平衡,此時CO2的轉化率為75%。則0~15min內平均反應速率v(H2)= _________,此條件下該反應的平衡常數K=_________。
欲使平衡后乙與甲中相同組分氣體的體積分數相等,則ω、x、y、z需滿足的關系是_________,且_________ (用含y的等式表示)。
(2)研究表明,溫度、壓強對反應“C6H5CH2CH3(g)+CO2(g) ![]() C6H5CH=CH2(g)+CO(g)+H2O(g) △H”中乙苯的平衡轉化率影響如下圖所示:
C6H5CH=CH2(g)+CO(g)+H2O(g) △H”中乙苯的平衡轉化率影響如下圖所示:

則△H_________ 0(填“>”“<”或“=”),壓強p1、p 2、p3從大到小的順序是_________。
(3)CO可被NO2氧化:CO+NO2![]() CO2+NO。當溫度高于225℃時,反應速率v正=k正·c(CO)·c(NO2)、v逆=k逆·c(CO2)·c(NO),k正、k逆分別為正、逆反應速率常數。在上述溫度范圍內,k正、k逆與該反應的平衡常數K之間的關系為_________。
CO2+NO。當溫度高于225℃時,反應速率v正=k正·c(CO)·c(NO2)、v逆=k逆·c(CO2)·c(NO),k正、k逆分別為正、逆反應速率常數。在上述溫度范圍內,k正、k逆與該反應的平衡常數K之間的關系為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗:①![]()
![]() 溶液和
溶液和![]() 溶液各1mL混合得到紅色溶液a,均分溶液a置于b、c兩支試管中;
溶液各1mL混合得到紅色溶液a,均分溶液a置于b、c兩支試管中;
②向b中滴加3滴飽和![]() 溶液,溶液顏色加深;
溶液,溶液顏色加深;
③再向上述b溶液中滴加3滴![]() 溶液,溶液顏色變淺且出現渾濁;
溶液,溶液顏色變淺且出現渾濁;
④向c中逐漸滴加![]() 溶液
溶液![]() ,溶液顏色先變深后變淺。
,溶液顏色先變深后變淺。
下列分析不正確的是
A. 實驗②中增大![]() 濃度使平衡
濃度使平衡![]() 正向移動
正向移動
B. 實驗③中發生反應: ![]()
C. 實驗③和④中溶液顏色變淺的原因相同
D. 實驗②、③、④均可說明濃度改變對平衡移動的影響
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CH4、H2、C都是優質的能源物質,它們燃燒的熱化學方程式為:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
(1)在深海中存在一種甲烷細菌,它們依靠酶使甲烷與O2作用產生的能量存活,甲烷細菌使1mol甲烷生成CO2氣體與液態水,放出的能量________(填“>”“<”或“=”)890.3kJ。
(2)甲烷與CO2可用于合成水煤氣(主要成分是一氧化碳和氫氣):CH4+CO2=2CO+2H2,1gCH4完全反應可釋放15.46kJ的熱量,則:
①能表示該反應過程中能量變化的是________(填字母)。



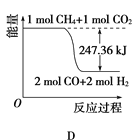
②若將物質的量均為1mol的CH4與CO2充入某恒容密閉容器中,體系放出的熱量隨著時間的變化如圖所示,則CH4的轉化率為________。
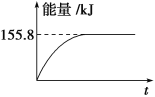
(3)C(s)與H2 (g)不反應,所以C(s)+2H2(g)=CH4(g)的反應熱無法直接測量,但通過上述反應可求出C(s)+2H2(g)=CH4(g)的反應熱ΔH=_____。
(4)目前對于上述三種物質的研究是燃料研究的重點,下列關于上述三種物質的研究方向中可行的是_______(填字母)。
A.尋找優質催化劑,使CO2與H2O反應生成CH4與O2,并放出熱量
B.尋找優質催化劑,在常溫常壓下使CO2分解生成碳與O2
C.尋找優質催化劑,利用太陽能使大氣中的CO2與海底開采的CH4合成水煤氣(CO、H2)
D.將固態碳合成為C60,以C60作為燃料
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com