
回答下列問題。
(1)常溫時,FeCl3溶液的pH 7(填“>”、“<”或“=”),實驗室配制FeCl3溶液時常將FeCl3固體先溶于較濃的鹽酸溶液中,然后再用蒸餾水稀釋到所需的濃度,原因是 ;將FeCl3溶液蒸干、灼燒,此過程中所涉及到的化學方程式是 。
(2)25℃時,向0.1 mol·L-1氨水中加入少量NH4Cl固體,當固體溶解后,測得溶液pH減小,主要原因是 。
(3)某溶液中只存在OH-、H+、Na+、CH3COO-四種離子。
①若溶液中只溶解了一種溶質,該溶質的名稱是 ,該溶液中四種離子的濃度由大到小的順序為 。
②若溶液中四種離子的大小順序為c(Na+)>c(OH-)>c(CH3COO-)>c(H+),則溶液中溶質的化學式為 。
③若溶液中c(Na+)=c(CH3COO-),則該溶液顯 (填“酸性”、“堿性”、“中性”),該溶液由體積相等的稀NaOH和CH3COOH溶液混合而成,則混合前c(NaOH) c(CH3COOH)(填“>”、“<”或“=”)。
(1)<,(1分) Fe3+發生水解,加入鹽酸后,抑制其水解。(2分)
FeCl3+3H2O Fe(OH)3+3HCl 或FeCl3+3H2O
Fe(OH)3+3HCl 或FeCl3+3H2O Fe(OH)3↓+3HCl ↑( 2分 )
Fe(OH)3↓+3HCl ↑( 2分 )
2Fe(OH)3 Fe2O3+3H2O (2分)
Fe2O3+3H2O (2分)
(2)氨水中存在電離平衡NH3·H2O NH4+ + OH-。NH4Cl溶于水,發生電離NH4Cl=NH4++Cl-,產生大量NH4+,使氨水的電離平衡向左移動,溶液中c(OH-)減小。(3分)
NH4+ + OH-。NH4Cl溶于水,發生電離NH4Cl=NH4++Cl-,產生大量NH4+,使氨水的電離平衡向左移動,溶液中c(OH-)減小。(3分)
(3)① 醋酸鈉 c(Na+)>c(CH3COO-)>c(OH-)>c(H+) (每空1分,共2)
②NaOH、CH3COONa (2分) ③中性,< (每空1分,共2分))
解析試題分析:(1)氯化鐵是強酸弱堿鹽,溶于水鐵離子水解溶液顯酸性,因此常溫時,FeCl3溶液的pH<7;氯化鐵是強酸弱堿鹽,溶于水鐵離子水解溶液顯酸性,加入鹽酸后,抑制鐵離子水解;水解是吸熱的,加熱促進水解。且生成的氯化氫極易揮發,因此最終得到氫氧化鐵固體,進一步灼燒得到氧化鐵,反應的反應式有FeCl3+3H2O Fe(OH)3+3HCl或FeCl3+3H2O
Fe(OH)3+3HCl或FeCl3+3H2O Fe(OH)3↓+3HCl↑、2Fe(OH)3
Fe(OH)3↓+3HCl↑、2Fe(OH)3 Fe2O3+3H2O。
Fe2O3+3H2O。
(2)氨水中存在一水合氨的電離平衡NH3·H2O NH4+ + OH-。NH4Cl溶于水,發生電離NH4Cl=NH4++Cl-,產生大量NH4+,增大溶液中c(NH4+)濃度,使一水合氨的電離平衡向左移動,因此溶液中c(OH-)減小。
NH4+ + OH-。NH4Cl溶于水,發生電離NH4Cl=NH4++Cl-,產生大量NH4+,增大溶液中c(NH4+)濃度,使一水合氨的電離平衡向左移動,因此溶液中c(OH-)減小。
(3)①只有醋酸鈉能同時電離出Na+、CH3COO-,而任何溶液中都存在水的電離平衡,所以若溶液中只溶解了一種溶質,該溶質的名稱是醋酸鈉。醋酸鈉溶于水電離出的CH3COO-水解溶液顯堿性,所以溶液中離子濃度大小關系是c(Na+)>c(CH3COO-)>c(OH-)>c(H+)。
②由于醋酸鈉的水解程度比較小,所以若溶液中四種離子的大小順序為c(Na+)>c(OH-)>c(CH3COO-)>c(H+),這說明溶液是由醋酸鈉和氫氧化鈉組成的混合液,則溶液中溶質的化學式NaOH、CH3COONa。
③根據電荷守恒可知c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以若溶液中c(Na+)=c(CH3COO-),則溶液中c(OH-)=(H+),所以該溶液顯中性。如果醋酸和氫氧化鈉恰好中和生成醋酸鈉,由于醋酸鈉水解溶液顯堿性。因此要使溶液顯中性,則醋酸一定是過量的。因此若該溶液由體積相等的稀NaOH和CH3COOH溶液混合而成,則混合前c(NaOH)< c(CH3COOH)。
考點:考查水解平衡的應用、外界條件對水解平衡的影響以及溶液中離子濃度大小比較


 第1卷單元月考期中期末系列答案
第1卷單元月考期中期末系列答案科目:高中化學 來源: 題型:填空題
科研、生產中常涉及鈉、硫及其化合物。
(1)實驗室可用無水乙醇處理少量殘留的金屬鈉,化學反應方程式為 。要清洗附著在試管壁上的硫,可用的試劑是 。
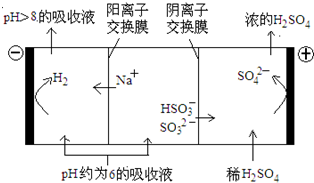
(2)如圖為鈉高能電池的結構示意圖,該電池的工作溫度為320 ℃左右,電池反應為2Na+xS=Na2Sx,正極的電極反應式為 。M(由Na2O和Al2O3制得)的兩個作用是 。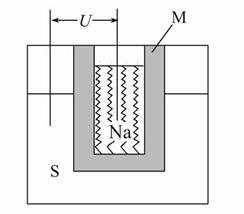
與鉛蓄電池相比,當消耗相同質量的負極活性物質時,鈉硫電池的理論放電量是鉛蓄電池的 __ 倍。
(3)Na2S溶液中離子濃度由大到小的順序為 ,向該溶液中加入少量固體CuSO4,溶液pH (填“增大”、“減小”或“不變”),Na2S溶液長期放置有硫析出,原因為 (用離子方程式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
Ⅰ.已知:H2A的A2-可表示S2-、S 、S
、S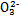 、Si
、Si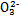 或C
或C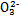 等離子。
等離子。
(1)常溫下,向20 mL 0.2 mol·L-1 H2A溶液中滴加0.2 mol·L-1 NaOH溶液。有關微粒物質的量變化如圖(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。請根據圖示填空: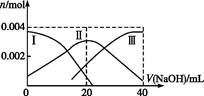
①當V(NaOH)="20" mL時,溶液中離子濃度大小關系: 。
②等體積等濃度的NaOH溶液與H2A溶液混合后,其溶液中水的電離程度比純水 (填“大”“小”或“相等”),欲使NaHA溶液呈中性,可以向其中加入 。
(2)若H2A為硫酸:t℃時,有pH=2的稀硫酸和pH=11的NaOH溶液等體積混合后溶液呈中性,則該溫度下水的離子積常數KW= 。
Ⅱ.已知:在25 ℃時 H2O H++OH- KW=10-14
H++OH- KW=10-14
CH3COOH H++CH3COO- Ka=1.8×10-5
H++CH3COO- Ka=1.8×10-5
(3)醋酸鈉水解的平衡常數Kh的表達式為 ,具體數值= ,當升高溫度時,Kh將 (填“增大”“減小”或“不變”)。
(4)0.5 mol·L-1醋酸鈉溶液pH為m,其水解的程度(已水解的醋酸鈉與原有醋酸鈉的比值)為a;1 mol·L-1醋酸鈉溶液pH為n,水解的程度為b,則m與n的關系為 ,a與b的關系為 。(填“大于”“小于”或“等于”)
Ⅲ.(5)25 ℃時,將a mol·L-1的氨水與b mol·L-1鹽酸等體積混合,反應后溶液恰好顯中性,則a b(填“大于”“小于”或“等于”)。用a、b表示NH3·H2O的電離平衡常數為 。
b(填“大于”“小于”或“等于”)。用a、b表示NH3·H2O的電離平衡常數為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某二元酸(化學式用H2A表示)在水溶液中的電離方程式是:
H2A=H++HA-,HA- H++A2-。
H++A2-。
試回答下列問題:
(1)Na2A溶液顯________(填“酸性”、“中性”或“堿性”),理由是_____________________(用離子方程式表示)。
(2)若0.1 mol·L-1 NaHA溶液的pH=2,則0.1 mol·L-1 H2A溶液中H+的物質的量濃度________0.11 mol·L-1。(填“>”、“=”或“<”)
(3)0.1 mol·L-1 NaHA溶液中各種離子濃度由大到小的順序是___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
最近霧霾天氣肆虐我國大部分地區。其中SO2是造成空氣的污染的主要原因,利用鈉堿循環法可除去SO2。
(1)鈉堿循環法中,吸收液為Na2SO3溶液,該反應的離子方程式是________。
(2)已知H2SO3的電離常數為K1=1.54×10-2,K2=1.024×10-7;H2CO3的電離常數為K1=4.30×10-7,K2=5.60×10-11,則下列微粒可以大量共存的是______(填序號)。
A.CO32- HSO3- B. HCO3- HSO3- C. SO32- HCO3- D. H2SO3 HCO3-
(3)吸收液吸收SO2的過程中,pH隨n(SO32-):n(HSO3-)變化關系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
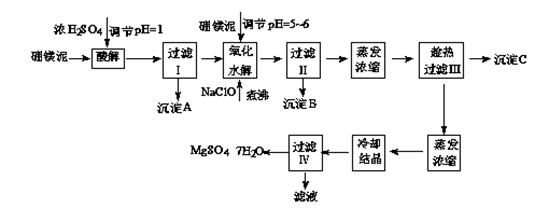
七水硫酸鎂(MgSO4·7H2O)在印染、造紙和醫藥等工業上都有廣泛的應用,利用化工廠生產硼砂的廢渣-硼鎂泥可制取七水硫酸鎂。硼鎂泥的主要成分是MgCO3,還含有其他雜質(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分陽離子以氫氧化物形式完全沉淀時溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
| 溫度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
25℃時,電離平衡常數:
| 化學式 | CH3COOH | H2CO3 | HClO | H2C4H4O6(酒石酸) | H2SO3 |
| 電離平衡常數 | 2.0×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 | K1=9.1×10-4 K2=4.3×10-5 | K1=1.3×10-2 K2=6.3×10-8 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
一種含鋁、鋰、鈷的新型電子材料,生產中產生的廢料數量可觀,廢料中的鋁以金屬鋁箔的形式存在;鈷以Co2O3·CoO的形式存在,吸附在鋁箔的單面或雙面;鋰混雜于其中。
從廢料中回收氧化鈷(CoO)的工藝流程如下: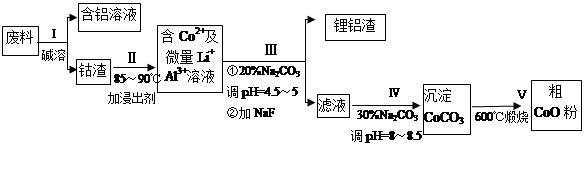
(1)過程I中采用NaOH溶液溶出廢料中的Al,反應的離子方程式為 。
(2)過程Ⅲ得到鋰鋁渣的主要成分是LiF和Al(OH)3,碳酸鈉溶液在產生Al(OH)3時起重要作用,請寫出該反應的離子方程式________ ____________。
(3)碳酸鈉溶液在過程III和IV中所起作用有所不同,請寫出在過程IV中起的作用是 。
(4)在Na2CO3溶液中存在多種粒子,下列各粒子濃度關系正確的是___ ___(填序號)。
| A.c(Na+) = 2c(CO32-) |
| B.c(Na+) > c(HCO3-) > c(CO32-) |
| C.c(OH-) > c(HCO3-) > c(H+) |
| D.c(OH-) - c(H+) = c(HCO3-) + 2c(H2CO3) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
以食鹽為原料進行生產并綜合利用的某些過程如下圖所示: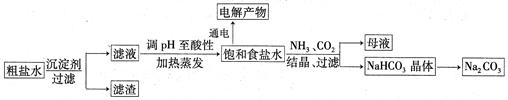
(1)為除去粗鹽中的Ca2+、Mg2+和SO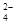 ,得到純凈的NaCl晶體,需加入以下試劑:
,得到純凈的NaCl晶體,需加入以下試劑:
| A.過量的NaOH溶液; | B.過量的Na2CO3溶液; | C.適量的鹽酸; | D.過量的BaCl2溶液。 |
 (OH-)的比值是_________。
(OH-)的比值是_________。查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com