
【題目】燃煤和汽車尾氣是造成空氣污染產生霧霾的原因之一。消除汽車尾氣是減少城市空氣污染的熱點研究課題。
(1)已知:①N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
②CO(g)+1/2 O2(g)=CO2 (g) △H=-283kJ·mol-1
則汽車尾氣中NO和CO在催化轉化器中相互反應成無污染的氣體的熱化學方程式是__________。
(2)在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線,如圖所示。

已知當固體催化劑的質量一定時,增大其表面積可提高化學反應速率。若催化劑的表面積S1>S2,在圖中畫出c(CO2)在T2、S2條件下達到平衡過程的變化曲線_____________。
(3)在一定溫度下,將2.0mol NO、2.4mol氣體CO 通入到固定容積為2L的容器中,反應過程中部分物質的濃度變化如右圖所示:
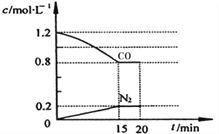
①有害氣體NO的轉化率為________, 0~15min NO的平均速率v(NO)=______mol/(L·min)。(保留兩位有效數字)
②20min時,若改變反應條件,導致CO濃度減小,則改變的條件可能是________(選填序號)。
a.縮小容器體積b.增加CO的量 c.降低溫度 d.擴大容器體積
③若保持反應體系的溫度不變,20min時再向容器中充入NO、N2各0.4mol,化學平衡將___________移動(選填“向左”、“向右”或“不”),移動后在達到平衡時的平衡常數的值是____________(保留兩位有效數字)。
【答案】 2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5kJmol-1 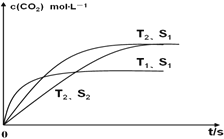 40% 0.027mol/(Lmin) cd 向左 0.14
40% 0.027mol/(Lmin) cd 向左 0.14
【解析】試題分析:(1)根據蓋斯定律計算汽車尾氣中NO和CO在催化轉化器中相互反應生成無污染氣體的焓變;(2)催化劑能加快化學反應速率,不能使平衡發生移動,平衡時CO2的濃度與T2、S2相同;(3)①根據轉化率=![]() 計算;根據
計算;根據![]() 計算速率;②根據平衡移動原理分析CO濃度減小的原因;③利用“三段式”計算平衡常數,計算再向容器中充入NO、N2各0.4mol時的Q值,根據Q、K的關系判斷平衡移動方向;溫度相同,平衡常數不變;
計算速率;②根據平衡移動原理分析CO濃度減小的原因;③利用“三段式”計算平衡常數,計算再向容器中充入NO、N2各0.4mol時的Q值,根據Q、K的關系判斷平衡移動方向;溫度相同,平衡常數不變;
解析:(1)①N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
②CO(g)+1/2 O2(g)=CO2 (g) △H=-283kJ·mol-1
根據蓋斯定律,②×2-①得2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5kJmol-1;(2)催化劑能加快化學反應速率,不能使平衡發生移動,平衡時CO2的濃度與T2、S2相同,所以若催化劑的表面積S1>S2, c(CO2)在T2、S2條件下達到平衡過程的變化曲線是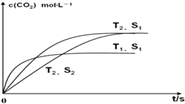 ;
;
(3)根據圖像
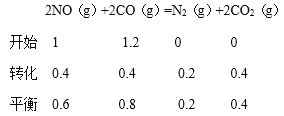
①轉化率=![]() =
=![]() ;
; ![]() =
=![]() 0.027mol/(Lmin);②a.縮小容器體積,CO濃度增大,故a錯誤;b.增加CO的量,CO的濃度一定增大,故b錯誤; c.降低溫度,平衡正向移動,CO濃度減小,故c正確; d.擴大容器體積,CO濃度一定減小,故d正確,選cd;③根據“三段式”,平衡常數
0.027mol/(Lmin);②a.縮小容器體積,CO濃度增大,故a錯誤;b.增加CO的量,CO的濃度一定增大,故b錯誤; c.降低溫度,平衡正向移動,CO濃度減小,故c正確; d.擴大容器體積,CO濃度一定減小,故d正確,選cd;③根據“三段式”,平衡常數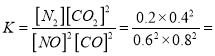 0.14 ,再向容器中充入NO、N2各0.4mol時的Q=
0.14 ,再向容器中充入NO、N2各0.4mol時的Q=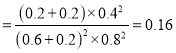 , Q>K,平衡向左移動;溫度相同,平衡常數不變,移動后在達到平衡時的平衡常數的值是0.14;
, Q>K,平衡向左移動;溫度相同,平衡常數不變,移動后在達到平衡時的平衡常數的值是0.14;


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】室溫下如圖,關閉活塞,在左右兩室(體積相同)各充入一定量H2和Cl2,且恰好使兩容器內氣體密度相同,打開活塞,點燃使H2與Cl2充分反應生成氯化氫氣體:H2+Cl2=2HCl,恢復到原溫度后,下列判斷正確的是

A. 開始時左右兩室分子數相同
B. 最終容器內無H2存在
C. 反應前后H2室壓強相同
D. 最終容器內密度與原來相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】蛋白質是生命的物質基礎。某學習小組通過實驗探究一種蛋白質的元素組成。
I.確定該蛋白質中的某些組成元素
(1)為確定該蛋白質中含氮元素,將樣品中有機氮轉化成銨鹽,能證明銨鹽存在的實驗方法是_________________。
(2)為確定該蛋白質中含碳、氫、硫三種元素,采用如下圖裝置進行研究,通入氧氣使樣品在裝置A中充分燃燒,并使其產物依次緩緩通過其余裝置。

①裝置B中的試劑是_________。
②裝置D的作用是____________________。
③當裝置B、C、E、F依次出現下列現象:________________,品紅褪色,______________,出現白色渾濁;可證明燃燒產物中含有H2O、SO2、CO2。
結論:該蛋白質中含碳、氫、硫、氮等元素。
II.為測定該蛋白質中硫元素的質量分數,小組取蛋白質樣品充分燃燒,先用足量碘水吸收二氧化硫,再取吸收液,以淀粉為指示劑,用硫代硫酸鈉溶液滴定過量的碘。已知:2S2032-+I2=S4062-+2I-
(3)寫出二氧化硫與碘水反應的化學方程式:___________________________。
(4)滴定終點的現象為:______________________。
(5)取蛋白質樣品mg進行測定,采用C1mol/L的碘水V1mL進行吸收,滴定過量的碘時消耗C2mol/L硫代硫酸鈉溶液V2mL。該蛋白質中的硫元素的質量分數為______________。
(6)若燃燒時過量氧氣進入吸收液中,可能會導致該蛋白質中的硫元素的質量分數測定值___(填“偏大”或“偏小”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)100°C時,KW=1.0×10﹣12,在該溫度下,測得0.1mol/LNa2A溶液pH=6.
①H2A在水溶液中的電離方程式為_____;
②體積相等pH=1的鹽酸與H2A溶液分別與足量的Zn反應,與鹽酸相比,H2A溶液產生的H2____(填“多”、“少”或“一樣多”).
(2)將0.4 mol/L HB溶液與0.2 mol/L NaOH溶液等體積混合(忽略混合后溶液體積的變化),測得混合溶液中c(Na+)>c(B-)。
①混合溶液中c(B﹣)_____c(HB)(填“>”、“<” 或“=”);
②混合溶液中c(HB)+ c(B-)_____0.2mol/L(填“>”、“<”或“=”).
(3)已知在常溫下常見弱酸的電離平衡常數Ka如表所示:
溶質 | CH3COOH | H2CO3 | HClO | HCN |
電離平衡常數Ka | 1.75×10-5 | Ka1=4.4×10-7 Ka2=4.7×10-11 | 3.2×10-8 | 6.2×10-10 |
①少量二氧化碳通入NaClO溶液中的離子方程式_____;
②濃度均為0.01mol/L的下列4種物質的溶液分別加水稀釋100倍,pH變化最小的是_____(填編號);
a.CH3COOH b.HCN c.HClO d.H2CO3
③常溫下濃度相同的醋酸和醋酸鈉混合液pH=6,則c( CH3COO-)﹣c( CH3COOH)=___mol/L(用數值列出計算式即可).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求完成下列各小題
(1)寫出NaHSO4在水溶液中的電離方程式______________________________________。
(2)氯化鋁的水溶液常溫時呈_____(填“酸”、“中”、“堿”)性,把氯化鋁溶液蒸干,灼燒,最后得到的固體產物是__________。
(3)實驗室配制FeSO4溶液,溶解時先要加入少量的稀硫酸,其原因是___________________(用離子方程式和適當文字說明);配制完畢后要加入少量鐵屑,其目的是____________________________。
(4)t℃時,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12,則:
①該溫度下水的離子積常數Kw=________________;
②在該溫度下,將100mL 0.1 mol·L-1的稀H2SO4與100mL 0.4 mol·L-1的NaOH溶液混合后,溶液的pH= _____________。
【答案】 NaHSO4=Na++H++SO42- 酸 Al2O3 Fe2++2H2OFe(OH)2+2H+ 抑制Fe2+水解 防止Fe2+氧化 1.0×10-12 11
【解析】(1). NaHSO4是強酸的酸式鹽,在水溶液中完全電離,電離方程式為:NaHSO4=Na++H++SO42-,故答案為:NaHSO4=Na++H++SO42-;
(2).AlCl3是強酸弱堿鹽,水解使溶液呈酸性;Al3++3H2O![]() Al(OH)3+3H+,加熱蒸干氯化鋁溶液,促進鋁離子的水解,使平衡正向移動,因HCl易揮發,則蒸干后得到Al(OH)3固體,灼燒時Al(OH)3發生分解:2Al(OH)3
Al(OH)3+3H+,加熱蒸干氯化鋁溶液,促進鋁離子的水解,使平衡正向移動,因HCl易揮發,則蒸干后得到Al(OH)3固體,灼燒時Al(OH)3發生分解:2Al(OH)3 ![]() Al2O3+3H2O,所以灼燒后得到氧化鋁固體,故答案為:酸;Al2O3;
Al2O3+3H2O,所以灼燒后得到氧化鋁固體,故答案為:酸;Al2O3;
(3).實驗室配制FeSO4溶液,因亞鐵離子發生水解:Fe2++2H2O![]() Fe(OH)2+2H+,則溶解時先加入少量的稀硫酸,增大氫離子濃度,抑制Fe2+水解;因Fe2+容易被空氣中的氧氣氧化為Fe3+,配制完畢后加入少量鐵屑,可以發生:Fe+2Fe3+=3Fe2+,從而達到防止Fe2+被氧化的作用,故答案為:Fe2++2H2O
Fe(OH)2+2H+,則溶解時先加入少量的稀硫酸,增大氫離子濃度,抑制Fe2+水解;因Fe2+容易被空氣中的氧氣氧化為Fe3+,配制完畢后加入少量鐵屑,可以發生:Fe+2Fe3+=3Fe2+,從而達到防止Fe2+被氧化的作用,故答案為:Fe2++2H2O![]() Fe(OH)2+2H+,抑制Fe2+水解;防止Fe2+氧化;
Fe(OH)2+2H+,抑制Fe2+水解;防止Fe2+氧化;
(4).① . t℃時,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,則Kw= c(H+)×c(OH-)= 10-a mol·L-1×10-b mol·L-1=1.0×10-(a+b),已知a+b=12,則Kw=1.0×10-12,故答案為:1.0×10-12;
②在該溫度下,100mL 0.1 mol·L-1的稀H2SO4溶液中n(H+)=0.1L×0.1 mol·L-1×2=0.02mol,100mL 0.4 mol·L-1的NaOH溶液中n(OH-)=0.1L×0.4 mol·L-1=0.04mol,兩溶液混合后氫氧根離子過量,所得溶液中c(OH-)=![]() = 0.1mol/L,則c(H+)=
= 0.1mol/L,則c(H+)=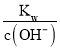 =10-11mol/L,則pH= -lgc(H+)=11,故答案為:11。
=10-11mol/L,則pH= -lgc(H+)=11,故答案為:11。
【題型】綜合題
【結束】
24
【題目】已知25 ℃時,部分弱電解質的電離平衡常數數據如下表:
弱酸化學式 | CH3COOH | HCN | H2CO3 |
電離平衡常數 | 1.7×10-5 | 6.2×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
(1)用離子方程式表示Na2CO3溶液呈堿性的原因:____________________。
(2)等物質的量濃度的A.CH3COONa B.NaCN C.Na2CO3 D.NaHCO3溶液的pH由大到小的順序為____________________________________(填字母)。
(3)已知在25℃時, 將HCN溶液與NaOH溶液等體積等濃度混合后,此溶液中離子濃度由大到小的順序是____________________________________。
(4)常溫下,0.1mol·L-1的CH3COOH溶液加水稀釋,下列表達式的數據變大的是______。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
(5)體積均為10 mL ,pH均為2的醋酸溶液與鹽酸分別與足量Zn反應,反應剛開始時產生H2的速率:v(HCl)______v(CH3COOH)(填“=”、“>”或“<”下同),反應完全后,所得氫氣的質量:m(H2)鹽酸_______m(H2)醋酸。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銀鋅蓄電池應用廣泛,放電時總反應為Zn+Ag2O2+H2O==Zn(OH)2+Ag2O,某小組以銀鋅蓄電池為電源,用惰性電極電解飽和Na2SO4溶液制備H2SO4和NaOH,設計如圖所示裝置。連通電路后,下列說法正確是

A. 電池的a極反應式為Ag2O2+H2O+2e-=Ag2O+2OH-
B. 氣體Y為H2
C. pq膜適宜選擇陽離子交換膜
D. 電池中消耗65gZn,理論上生成1mol氣體X
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】納米級Cu2O由于具有優良的催化性能而受到關注,下表為制取Cu2O的三種方法:
納米級Cu2O由于具有優良的催化性能而受到關注,下表為制取Cu2O的三種方法:
方法a | 用炭粉在高溫條件下還原CuO |
方法b | 電解法,反應為2Cu + H2O |
方法c | 用肼(N2H4)還原新制Cu(OH)2 |
(1)已知:2Cu(s)+![]() O2(g)=Cu2O(s)△H =-169kJ·mol-1
O2(g)=Cu2O(s)△H =-169kJ·mol-1
C(s)+![]() O2(g)=CO(g)△H =-110.5kJ·mol-1
O2(g)=CO(g)△H =-110.5kJ·mol-1
Cu(s)+![]() O2(g)=CuO(s)△H =-157kJ·mol-1
O2(g)=CuO(s)△H =-157kJ·mol-1
則方法a發生反應的熱化學方程式是_____________________________________。
(2)方法b采用離子交換膜控制電解液中OH-的濃度而制備納米Cu2O,裝置如圖所示,該離子交換膜為______離子交換膜(填“陰”或“陽”),該電池的陽極反應式為______________________________________。

(3)方法c為加熱條件下用液態肼(N2H4)還原新制Cu(OH)2來制備納米級Cu2O,同時放出N2,該制法的化學方程式為________________________________________。
(4)在容積為1L的恒容密閉容器中,用以上方法制得的三種納米級Cu2O分別進行催化分解水的實驗:2H2O(g) ![]() 2H2(g)+O2(g),ΔH>0。水蒸氣的濃度c隨時間t的變化如下表所示。
2H2(g)+O2(g),ΔH>0。水蒸氣的濃度c隨時間t的變化如下表所示。

①對比實驗的溫度:T2_________T1(填“>”、“<”或“=”)
②催化劑催化效率:實驗①________實驗②(填“>”或“<”)
③在實驗③達到平衡狀態后,向該容器中通入水蒸氣與氫氣各0.1mol,則反應再次達到平衡時,容器中氧氣的濃度為 ____________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com