
【題目】NaClO溶液是一種紡織工業(yè)用漂白劑,可用一定比例NaOH、Na2CO3的混合溶液和Cl2反應(yīng)制備。
(1)NaHCO3的存在能增強(qiáng)NaClO溶液的穩(wěn)定性。Cl2與混合溶液中Na2CO3反應(yīng)制備NaClO,同時(shí)生成NaHCO3,其化學(xué)方程式為___。
(2)NaClO溶液中若含有NaClO3會(huì)影響產(chǎn)品的品質(zhì)。測定堿性NaClO樣品中NaClO3物質(zhì)的量濃度的方法如下:取20.00mLNaClO溶液試樣,加入過量H2O2,充分反應(yīng)后,加熱煮沸,冷卻至室溫,加入硫酸酸化,再加入0.1000mol·L-1FeSO4標(biāo)準(zhǔn)溶液30.00mL,充分反應(yīng)后,用0.01000mol·L-1酸性K2Cr2O7溶液滴定過量的FeSO4溶液至終點(diǎn)(Cr2O72-被還原為Cr3+),消耗該溶液25.00mL。
已知:ClO3-在堿性條件下性質(zhì)穩(wěn)定,在酸性條件下表現(xiàn)出強(qiáng)氧化性;ClO3-+Fe2++H+—Cl-+Fe3++H2O(未配平)。
①加入過量H2O2的目的是__。
②實(shí)驗(yàn)中若缺少加熱煮沸步驟,所測NaClO3物質(zhì)的量濃度會(huì)有較大誤差,原因可能是___(答出一個(gè)即可)。
③計(jì)算樣品中NaClO3物質(zhì)的量濃度___(寫出計(jì)算過程)。
【答案】2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3 將NaClO完全還原 NaClO3在酸性條件下被過量的H2O2還原或部分硫酸亞鐵被過量H2O2氧化 1.250×10-2mol·L-1
【解析】
(1)根據(jù)題意,反應(yīng)物為Na2CO3、Cl2、H2O,其中Cl2、H2O反應(yīng)產(chǎn)生HCl和HClO,都可以與Na2CO3反應(yīng),故產(chǎn)物有NaClO、NaHCO3、NaCl。方程式為:2Na2CO3+Cl2+H2O= NaClO+NaCl+2NaHCO3;
(2)①由于NaClO也有強(qiáng)氧化性,會(huì)影響NaClO3的測定,所以開始時(shí)加H2O2是為了將NaClO完全還原,避免跟后面加入的還原劑Fe2+反應(yīng),影響實(shí)驗(yàn)結(jié)果;
②加熱煮沸主要目的是讓H2O2分解。若H2O2有剩余,則可能跟酸性條件下NaClO3的反應(yīng),或者跟Fe2+反應(yīng),使結(jié)果出現(xiàn)誤差;
③根據(jù)題意,Fe2+既與K2Cr2O7反應(yīng),又與NaClO3反應(yīng)。Fe2+的物質(zhì)的量為0.1mol/L×0.03L=0.003mol, K2Cr2O7的物質(zhì)的量為:0.01mol/L×0.025L =0.00025mol。由電子轉(zhuǎn)移守恒可得![]() ,則與Cr2O72-反應(yīng)的Fe2+的物質(zhì)的量為0.00025mol×6=0.0015mol,那么與ClO3-反應(yīng)的Fe2+的物質(zhì)的量為0.003mol-0.0015mol=0.0015mol,根據(jù)電子轉(zhuǎn)移守恒可得
,則與Cr2O72-反應(yīng)的Fe2+的物質(zhì)的量為0.00025mol×6=0.0015mol,那么與ClO3-反應(yīng)的Fe2+的物質(zhì)的量為0.003mol-0.0015mol=0.0015mol,根據(jù)電子轉(zhuǎn)移守恒可得![]() ,則ClO3-的物質(zhì)的量為0.0015mol÷6=0.00025mol,所以NaClO3物質(zhì)的量濃度c=
,則ClO3-的物質(zhì)的量為0.0015mol÷6=0.00025mol,所以NaClO3物質(zhì)的量濃度c=![]() 。
。


 科學(xué)實(shí)驗(yàn)活動(dòng)冊系列答案
科學(xué)實(shí)驗(yàn)活動(dòng)冊系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:
【題目】制取乙烯時(shí),常因溫度過高而發(fā)生副反應(yīng),部分乙醇跟濃H2SO4 反應(yīng)生成SO2,CO2,水蒸氣和炭黑。
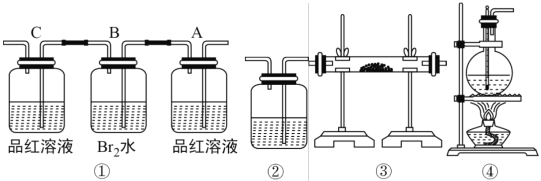
(1)用編號(hào)為①→④的實(shí)驗(yàn)裝置設(shè)計(jì)一個(gè)實(shí)驗(yàn),以驗(yàn)證上述反應(yīng)混合氣體中含CO2,SO2和水蒸氣。寫出裝置的連接順序(按產(chǎn)物氣流從左到右的流向填寫編號(hào)):______。
(2)實(shí)驗(yàn)的裝置①中 A 瓶的現(xiàn)象是______;結(jié)論為__________。 B 瓶中的現(xiàn)象是__________; B 瓶溶液作用為__________。若 C 瓶中品紅溶液不褪色,可得到結(jié)論為__________。
(3)裝置③中加的固體藥品是______以驗(yàn)證混合氣體中有______。裝置②中盛的溶液是_____以驗(yàn)證混合氣體中有______。
(4)簡述裝置①在整套裝置中位置的理由__________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】一種制氫技術(shù)原理如圖所示。容器Ⅰ中發(fā)生的某反應(yīng)a為C(s)+2H2O(g)![]() CO2(g)+2H2(g);ΔH。下列有關(guān)說法正確的是( )
CO2(g)+2H2(g);ΔH。下列有關(guān)說法正確的是( )
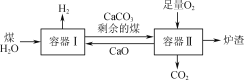
A.已知反應(yīng)a在一定條件下能夠自發(fā)進(jìn)行,則該反應(yīng)的ΔH<0
B.向容器Ⅰ中加入CaO能有效實(shí)現(xiàn)H2與CO2的分離
C.剩余的煤進(jìn)入容器Ⅱ是為了充分利用其與O2反應(yīng)放出的熱量
D.煤中含有的S在容器Ⅱ中最終轉(zhuǎn)化為CaSO3進(jìn)入爐渣
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】隨著原子序數(shù)的遞增,八種短周期元素(用字母x、y、z……表示)的原子半徑相對(duì)大小、最高正價(jià)或最低負(fù)價(jià)的變化如下圖所示。

請回答下列問題:
(1)f在周期表中的位置為______________;x形成的陰離子的結(jié)構(gòu)示意圖為_____________________。
(2)比較d、e常見離子的半徑大小:__________________(填化學(xué)式,下同);比較g、h的最高價(jià)氧化物對(duì)應(yīng)水化物的酸性強(qiáng)弱:_______________________。
(3)x、y、z、d四種元素能形成多種化合物。
①能形成離子化合物,其中一種x、y、z、d四種原子的個(gè)數(shù)比為5∶2∶1 ∶4,其化學(xué)式為__________________________。
②能形成共價(jià)化合物,寫出其中一種的結(jié)構(gòu)簡式____________________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】化合物F是從我國特產(chǎn)植物中提取的一種生物堿,其人工合成路線如圖:
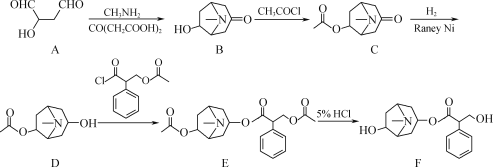
(1)A中含氧官能團(tuán)的名稱為___和___。
(2)C→D的反應(yīng)類型為___。
(3)E→F的過程中,會(huì)有副產(chǎn)物X(分子式為C8H15NO2)生成,寫出X的結(jié)構(gòu)簡式:___。
(4)C的一種同分異構(gòu)體同時(shí)滿足下列條件,寫出該同分異構(gòu)體的結(jié)構(gòu)簡式:__。
①分子中有醚鍵;
②能與FeCl3溶液發(fā)生顯色反應(yīng),能與鹽酸反應(yīng);
③有4種不同化學(xué)環(huán)境的氫且數(shù)目比為9∶2∶2∶2。
(5)已知:R—O—R′+2HBr![]() R—Br+R′—Br十H2O(R、R′表示烴基)。
R—Br+R′—Br十H2O(R、R′表示烴基)。
寫出以![]() 、CH3NH2和CO(CH2COOH)2為原料制備
、CH3NH2和CO(CH2COOH)2為原料制備![]() 的合成路線流程圖___(無機(jī)試劑任用,合成路線流程圖示例見本題題干)。
的合成路線流程圖___(無機(jī)試劑任用,合成路線流程圖示例見本題題干)。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】磷精礦濕法制備磷酸的一種工藝流程如下:

已知:磷精礦主要成分:Ca5(PO4)3(OH),還含有Ca5(PO4)3F和有機(jī)碳等。
(1)上述流程中所采取的實(shí)驗(yàn)措施能加快反應(yīng)速率有_____________。
(2)酸浸時(shí),磷精礦中Ca5(PO4)3(OH)與H2SO4反應(yīng)的化學(xué)方程式為_____________。
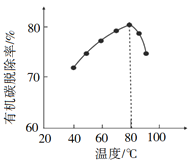
(3)H2O2將粗磷酸中的有機(jī)碳氧化為CO2脫除,同時(shí)自身也會(huì)發(fā)生分解。相同投料比、相同反應(yīng)時(shí)間,不同溫度下的有機(jī)碳脫除率如圖所示。80℃后脫除率變化的原因______。
(4)脫硫時(shí),CaCO3稍過量,充分反應(yīng)后仍有SO42-殘留,加入BaCO3代替CaCO3可進(jìn)一步提高硫的脫除率,原因是_____。向粗磷酸中加入BaCO3脫硫,發(fā)生反應(yīng)的離子方程式是_____。
(5)取ag所得精制磷酸,加適量水稀釋,以百里香酚酞作指示劑,用b mol·L-1 NaOH 溶液滴定至終點(diǎn)時(shí)生成Na2HPO4,消耗NaOH溶液c L,精制磷酸中H3PO4的質(zhì)量分?jǐn)?shù)是_____。(已知摩爾質(zhì)量為98g·mol-1)
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】(Ⅰ)、如圖為一“鐵鏈”圖案,小明在圖案上分別寫了H2、CO2、Na2O、NaCl、FeCl3五種物質(zhì),圖中相連的兩種物質(zhì)均可歸屬為一類,相交部分A、B、C、D為其相應(yīng)的分類依據(jù)代號(hào)。請回答下列問題:
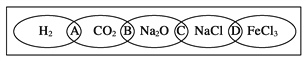
(1)請將分類依據(jù)代號(hào)填入相應(yīng)的括號(hào)內(nèi):
(______)兩種物質(zhì)都不是電解質(zhì)
(______)兩種物質(zhì)都是鹽
(2)用潔凈的燒杯取少量蒸餾水,用酒精燈加熱至沸騰,向燒杯中逐滴加入飽和的圖中某種物質(zhì)M的溶液加熱至呈紅褐色。
①物質(zhì)M的化學(xué)式為________________。
②證明有紅褐色膠體生成的實(shí)驗(yàn)操作是________________________________________。
(Ⅱ)反應(yīng):A.2F2+2H2O=4HF+O2↑; B.2Na+2H2O=2NaOH+H2↑;
C.CaO+H2O=Ca(OH)2; D.2H2O=2H2↑+O2↑。
其中水是氧化劑的是______,水是還原劑的是________。(填序號(hào))
(Ⅲ)反應(yīng):3Cu + 8HNO3 = 3Cu(NO3)2+2NO↑+4H2O,還原劑與氧化劑的物質(zhì)的量之比:_______,當(dāng)有0.6mol電子轉(zhuǎn)移時(shí)。生成的NO在標(biāo)準(zhǔn)狀況的體積為________L。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】太陽能的開發(fā)利用在新能源研究中占據(jù)重要地位,單晶硅太陽能電池片在加工時(shí),一般摻雜微量的銅、鈷、硼、鎵、硒等。回答下列問題:
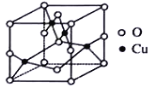
(1)基態(tài)二價(jià)銅離子的電子排布式為______,已知高溫下Cu2O比CuO更穩(wěn)定,試從核外電子排布角度解釋______。
(2)銅的某種氧化物晶胞如圖,該晶胞中陰離子的個(gè)數(shù)為_________。
(3)銅與(SCN)2反應(yīng)生成Cu(SCN)2,中心體為___________,HSCN結(jié)構(gòu)有兩種,硫氰酸(H-S-C≡N)的沸點(diǎn)低于異硫氰酸(H-N=C=S)的原因是_________。
(4)BF3能與NH3反應(yīng)生成BF3·NH3。B與N之間形成配位鍵,氮原子提供_____,第二周期元素中,電離能介于B和N之間的元素有_______個(gè)。
(5)如圖EMIM+離子中,碳原子的雜化方式是___________。分子中的大π鍵可用符號(hào)πnm表示,其中n代表參與形成大π鍵的原子數(shù),m代表參與形成大π鍵的電子數(shù)(如苯分子中的大π鍵可表示為π66),則EMM+離子中的大π鍵應(yīng)表示為___________。
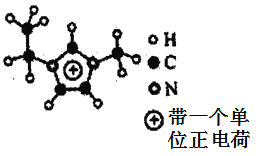
(6)如圖六方氮化硼晶體結(jié)構(gòu)與石墨晶體相似,則六方氮化硼晶體中層間的相互作用為___________。六方氮化硼在高溫高壓下,可以轉(zhuǎn)化為立方氮化硼,其結(jié)構(gòu)、硬度與金剛石相似,其晶胞如圖,晶胞邊長為361.5pm,立方氮化硼的密度是___________g·cm-3(只列算式,![]() 為阿伏加德羅常數(shù)的值)。
為阿伏加德羅常數(shù)的值)。

查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】在一絕熱(不與外界發(fā)生熱交換)的恒容容器中,發(fā)生反應(yīng):2A(g)+B(s) ![]() C(g)+D(g),下列描述中不能表明反應(yīng)已達(dá)到平衡狀態(tài)的是( )
C(g)+D(g),下列描述中不能表明反應(yīng)已達(dá)到平衡狀態(tài)的是( )
A. 混合氣體的密度不變 B. 單位時(shí)間內(nèi)生成n molD,同時(shí)生成n molC
C. 混合氣體的平均相對(duì)分子質(zhì)量不變 D. C(g)的物質(zhì)的量濃度不變
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com