
下表是元素周期表的一部分,X、Y、Z、W均為短周期元素,下列說法不正確的是( )
| | X | | Y |
| Z | | W | |
C
解析試題分析:A、根據元素周期律中原子半徑的比較,電子層數越多半徑越大,核電荷數越多,半徑越小,所以原子半徑:Z>W>X,正確;B、由4種元素在周期表中的位置判斷,非金屬性最強的W也只能是S元素,而硫化氫不穩定,越向左移,W的非金屬性越弱,其氣態氫化物越不穩定,正確;C、設Y的原子序數是x,則W的原子序數是x+7,則x+x+7=23,解得x=8,Z是Al元素,不能形成堿性氧化物而能形成兩性氧化物,錯誤;D、X能形成兩種常見的液態化合物,則X是O元素,形成的水與過氧化氫都是液態化合物,W是Cl元素,其單質溶于水生成的次氯酸具有漂白性,正確,答案選C。
考點:考查元素周期表及元素周期律的應用,物質的判斷


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:單選題
有X、Y、Z、W、M五種短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+與M2-具有相同的電子層結構;離子半徑:Z2->W-;Y的單質晶體熔點高、硬度大,是一種重要的半導體材料。下列說法中,正確的是( )
| A.X、M兩種元素只能形成X2M型化合物 |
| B.由于W、Z、M元素的氫氣化物相對分子質量依次減小,所以其沸點依次降低 |
| C.元素Y、Z、W的單質晶體屬于同種類型的晶體 |
| D.元素W和M的某些單質可作為水處理中的消毒劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知W、X、Y、Z為短周期元素,它們的原子半徑依次增大,W與Z、X和Y分別同主族,Y、Z同周期。X和Y能形成兩種常見共價化合物,Z能與X形成兩種常見的離子化合物,陰、陽離子個數比均為1:2。下列說法錯誤的是
| A.Y、Z、X、W的原子序數依次減小 |
| B.X的簡單氫化物的沸點低于Y的簡單氫化物的沸點 |
| C.由W、X、Y、Z四種元素組成的化合物可能顯強酸性 |
| D.W和X形成的化合物,與W和Y形成的化合物中各元素質量比可能相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
硒被譽為“生命的奇效元素”,富硒食品倍受追捧,重慶多地打造富硒農產品基地。已知硒元素與氧元素同族,與鈣元素同周期,下列關于硒的描述錯誤的是( )
| A.原子序數是24 |
| B.元素周期表中硒位于第四周期第VIA族 |
| C.最高價氧化物是SeO3,是酸性氧化物 |
| D.氣態氫化物化學式是H2Se,穩定性比HCl差 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
美國科學家將兩種元素鉛和氪的原子核對撞,獲得了一種質子數118,中子數為175的超重
元素,該元素原子核內中子數與核外電子數之差是( )
| A.57 | B.47 | C.61 | D.293 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
X、Y、Z、W四種短周期元素的最外層電子數之和為24,它們在元素周期表中的位置如下圖所示,下列說法一定正確的是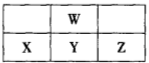
| A.X、Y、Z的含氧酸的酸性依次增強 |
| B.W元素形成的單核陰離子還原性強于X |
| C.W、X、Y的原子半徑依次增大 |
| D.W與氫元素形成的化合物中可能含有非極性鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
X、Y、Z、Q、M為常見的短周期元素,其原子序數依次增大。有關信息如下表:
| X | 動植物生長不可缺少的元素,是蛋白質的重要成分 |
| Y | 最外層電子數是次外層的3倍 |
| Z | 短周期中,其原子半徑最大 |
| Q | 生活中大量使用其合金制品,工業上可用電解其氧化物的方法制備 |
| M | 海水中大量富集的元素之一,其最高正化合價與負價的代數和為6 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知短周期元素的離子aW3+、bX+、cY2-、dZ-具有相同的電子層結構,下列關系正確的是( )。
| A.質子數c>b |
| B.原子半徑X<W |
| C.氫化物的穩定性H2Y>HZ |
| D.離子的還原性Y2->Z- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com