
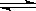 2CO(g)+2H2(g) △H= kJ·mol-1
2CO(g)+2H2(g) △H= kJ·mol-1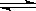 2CO(g)+2H2(g),測得CH4的平衡轉化率與溫度、壓強的關系如下圖所示。
2CO(g)+2H2(g),測得CH4的平衡轉化率與溫度、壓強的關系如下圖所示。
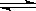 CO(g)+H2 (g)來制取。
CO(g)+H2 (g)來制取。| A.體系壓強不再變化 | B.H2與CO的物質的量之比為1 :1 |
| C.混合氣體的密度保持不變 | D.氣體平均相對分子質量為15,且保持不變 |

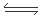 2CO(g)+2H2(g) △H=+248KJ/mol。(2)①據圖可知,甲烷在P1、P2、 P3、P4的轉化率的關系是P1 > P2> P3> P4。由于反應CH4(g)+CO2(g)
2CO(g)+2H2(g) △H=+248KJ/mol。(2)①據圖可知,甲烷在P1、P2、 P3、P4的轉化率的關系是P1 > P2> P3> P4。由于反應CH4(g)+CO2(g)  2CO(g)+2H2(g)的正反應是氣體體積增大的反應,根據平衡移動原理,減小壓強,平衡向氣體體積增大的反應方向即向正反應方向移動。所以這幾種條件下的壓強由大到小的順序P4> P3> P2> P1。②在壓強為P4、1100℃的條件下,該反應5min時達到平衡點X,此時甲烷的轉化率為80%,所以c(CO)=2×0.08=0.16mol/L則v(CO)=" 0.016mol/L÷5min=0.032mol/(L·min)." 該溫度下,反應的平衡常數為
2CO(g)+2H2(g)的正反應是氣體體積增大的反應,根據平衡移動原理,減小壓強,平衡向氣體體積增大的反應方向即向正反應方向移動。所以這幾種條件下的壓強由大到小的順序P4> P3> P2> P1。②在壓強為P4、1100℃的條件下,該反應5min時達到平衡點X,此時甲烷的轉化率為80%,所以c(CO)=2×0.08=0.16mol/L則v(CO)=" 0.016mol/L÷5min=0.032mol/(L·min)." 該溫度下,反應的平衡常數為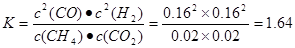 .(3)① A.由于該反應是反應前后氣體體積不等的反應,若反應未達到平衡,則容器的壓強就要發生變化,所以體系壓強不再變化,能證明反應達到平衡。正確。B.在任何時刻都存在關系:H2與CO的物質的量之比為1 :1,因此不能作為判斷平衡的標志。錯誤。C.由于反應物有固體參加,若反應未達到平衡,則氣體的密度就要增大或減小,若達到平衡,氣體的密度就不會發生變化。因此混合氣體的密度保持不變可以證明反應達到平衡的標志。正確。D. 若氣體完全是CO與氫氣,由于生成的二者的物質的量的比為1:1,氣體平均相對分子質量為15,若氣體完全是水蒸氣,則氣體的相對分子質量為18,由于可逆反應達到平衡狀態時是三者的共同體,所以氣體的平均相對分子質量應該在15~18,且保持不變。錯誤。②對于C(s)+H2O(g)
.(3)① A.由于該反應是反應前后氣體體積不等的反應,若反應未達到平衡,則容器的壓強就要發生變化,所以體系壓強不再變化,能證明反應達到平衡。正確。B.在任何時刻都存在關系:H2與CO的物質的量之比為1 :1,因此不能作為判斷平衡的標志。錯誤。C.由于反應物有固體參加,若反應未達到平衡,則氣體的密度就要增大或減小,若達到平衡,氣體的密度就不會發生變化。因此混合氣體的密度保持不變可以證明反應達到平衡的標志。正確。D. 若氣體完全是CO與氫氣,由于生成的二者的物質的量的比為1:1,氣體平均相對分子質量為15,若氣體完全是水蒸氣,則氣體的相對分子質量為18,由于可逆反應達到平衡狀態時是三者的共同體,所以氣體的平均相對分子質量應該在15~18,且保持不變。錯誤。②對于C(s)+H2O(g)  CO(g)+H2 (g),若增大壓強,根據平衡移動原理,應該向氣體體積減小的方向就是向逆反應方向移動。在第2分鐘時混合氣體的平均相對分子質量為:
CO(g)+H2 (g),若增大壓強,根據平衡移動原理,應該向氣體體積減小的方向就是向逆反應方向移動。在第2分鐘時混合氣體的平均相對分子質量為: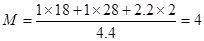 。第5min時達到新的平衡,假如生成物完全轉化為反應物,則混合氣體的物質的量減小1mol,質量減輕12g,所以混合氣體的相對分子質量不變,的平均相對分子質量仍然是12。2~5min內容器中氣體平均相對分子質量的變化曲線如圖:
。第5min時達到新的平衡,假如生成物完全轉化為反應物,則混合氣體的物質的量減小1mol,質量減輕12g,所以混合氣體的相對分子質量不變,的平均相對分子質量仍然是12。2~5min內容器中氣體平均相對分子質量的變化曲線如圖: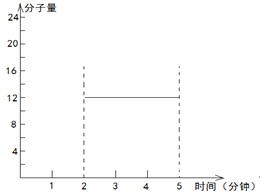 。
。

科目:高中化學 來源:不詳 題型:單選題
 C(s)+4D(g) ΔH<0,下圖中a、b表示一定條件下,D的體積分數隨時間t的變化情況。若要使曲線b變為曲線a,可采取的措施是( )
C(s)+4D(g) ΔH<0,下圖中a、b表示一定條件下,D的體積分數隨時間t的變化情況。若要使曲線b變為曲線a,可采取的措施是( )
| A.①② | B.①③ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| | 鉀 | 鈉 | Na2CO3 | 金剛石 | 石墨 |
| 熔點(℃) | 63.65 | 97.8 | 851 | 3550 | 3850 |
| 沸點(℃) | 774 | 882.9 | 1850(分解產生CO2) | --- | 4250 |
 2Na2CO3(1)+C(s,金剛石);△H=-1080.9kJ/mol
2Na2CO3(1)+C(s,金剛石);△H=-1080.9kJ/mol
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題

 、
、查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 CO2(g)+H2(g)反應的平衡常數和溫度的關系如下:
CO2(g)+H2(g)反應的平衡常數和溫度的關系如下:| |溫度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常數 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
 ΔH=+8.0kJ·mol-1
ΔH=+8.0kJ·mol-1 ΔH=+90.4kJ·mol-1
ΔH=+90.4kJ·mol-1 ΔH=-556.0kJ·mol-1
ΔH=-556.0kJ·mol-1 ΔH=-483.6kJ·mol-1
ΔH=-483.6kJ·mol-1 與
與 反應生成
反應生成 熱化學方程式 。
熱化學方程式 。查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題

 向_________極移動。
向_________極移動。 。一定溫度下,向2 L容積不變的密閉容器中充入4 mol
。一定溫度下,向2 L容積不變的密閉容器中充入4 mol  和6 mo1 H2O(g)發生反應,10 min時,反應達到平衡狀態,測得CH4(g)和H2(g)的物質的量隨時間變化的曲線如圖所示。
和6 mo1 H2O(g)發生反應,10 min時,反應達到平衡狀態,測得CH4(g)和H2(g)的物質的量隨時間變化的曲線如圖所示。
 (CO)表示的化學反應速率為_________。
(CO)表示的化學反應速率為_________。
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 xC(g)+2D(g)。若經5min后反應達到平衡狀態,容器內的壓強變小,并知D的平均反應速率為0.2mol/(L?min),請填寫下列空白:
xC(g)+2D(g)。若經5min后反應達到平衡狀態,容器內的壓強變小,并知D的平均反應速率為0.2mol/(L?min),請填寫下列空白:查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題


 。
。查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
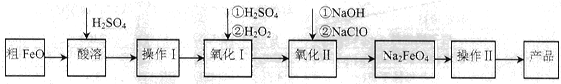
| 溫度/℃ | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| NaClO濃度/mol·L-1 | 4.6 | 5.2 | 5.4 | 5.5 | 4.5 | 3.5 | 2 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com