
自然界中的物質多數是以混合物的形式存在,下面是混合物的分離和提純,請填空:
(1)除去NaCl固體中混有的少量CaCO3,所進行的實驗操作為: 、 、蒸發、結晶。
(2)除去NaCl中的Na2SO4,依次加入的溶液為(填溶質化學式): 、 、 。
科目:高中化學 來源: 題型:填空題
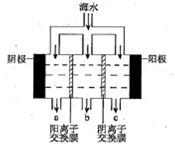
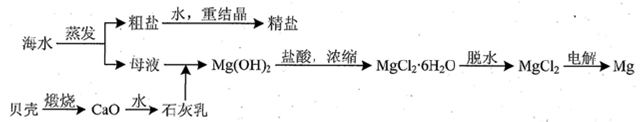
海水中主要離子的含量如下:
| 成分 | 含量/(mg/L) | 成分 | 含量/(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Mg2+ | 1272 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
以黃鐵礦為原料制硫酸產生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。實驗室模擬工業以硫酸渣制備鐵紅(Fe2O3),過程如下:
(1)硫酸渣的成分中屬于兩性氧化物的是 , 寫出酸溶過程Fe2O3與稀硫酸反應的離子反應方程式: ;
(2)生產過程中,為了確保鐵紅的純度,氧化過程需要調節溶液的pH的范圍是_________;(部分陽離子以氫氧化物形式沉淀時溶液的pH見下表)
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 開始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
銀銅合金廣泛應用于航空工業。從切割廢料中回收銀并制備銅的化工產品CuAlO2的工藝如下:(注:Al(OH)3和Cu(OH)2開始分解的溫度分別為450℃和80℃)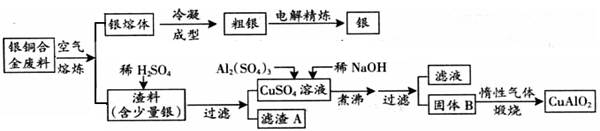
(1)銅的核外電子排布式為 .
(2)電解精煉銀時,陰極反應式為 濾渣A與稀HNO3反應,產生的氣體在空氣中迅速變為紅棕色,該氣體變色的化學方程式為 .
(3)固體混合物B的組成為 ;在生成固體B的過程中,需控制NaOH的加入量,若NaOH過量,最后將得不到CuAlO2 ,寫出因NaOH過量引起的反應的離子方程式 .
(4)若將上述流程圖中加入的稀NaOH溶液改為加入過量的氨水(其它均不變),則濾液中的陽離子有 .
(5)完成上述煅燒過程中一個反應的化學方程式:
CuO + Al2O3 Cu AlO2 + (系數1也要寫).
Cu AlO2 + (系數1也要寫).
(6)若銀銅合金中銅的質量分數為64%,理論上5.0kg廢料中的銅可完全轉化為CuAlO2,至少需要1.0mol·L-1的Al2(SO4)3溶液 L .
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(Ⅰ)二氧化鈰(CeO2)是一種重要的稀土氧化物。平板電視顯示屏生產過程中產生大量的廢玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物質)。某課題組以此粉末為原料回收鈰,設計實驗流程如下: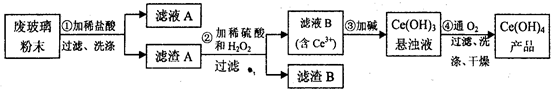
(1)洗滌的目的主要是為了除去Cl-和___________(填離子符號),檢驗該濾渣A洗凈的方法是_____________________。
(2)第②步反應的離子方程式是____________________________。
(3)取上述流程中得到的Ce(OH)4產品0.536 g,加硫酸溶解后,用0.1000mol· L-1FeSO4標準溶液滴定終點時(鈰被還原為Ce3+),消耗25.00mL標準溶液,該產品中Ce(OH)4的質量分數為_____________。
(Ⅱ)氧化鎂在醫藥、建筑等行業應用廣泛.硫酸鎂還原熱解制備高純氧化鎂是一種新的探索.以菱鎂礦(主要成分為MgCO3,含少量FeCO3)為原料制備高純氧化鎂的實驗流程如下: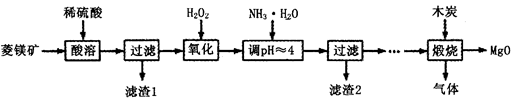
(1)加入H2O2氧化時,發生反應的化學方程式為________________。
(2)濾渣2的成分是______________(填化學式)。
(3)煅燒過程存在以下反應:2MgSO4+C=2MgO+2SO2↑+CO2↑
MgSO4+C=MgO+SO2↑+CO↑ MgSO4+3C=MgO+S↑+3CO↑
利用如圖裝置對煅燒產生的氣體進行分步吸收或收集。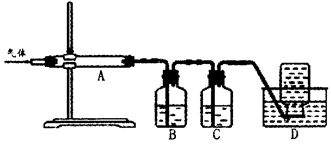
①D中收集的氣體可以是______________(填化學式)。
②B中盛放的溶液可以是______________(填字母)。
| A.NaOH溶液 | B.Ca(OH)2溶液 | C.稀硝酸 | D.KMnO4溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某白色粉末由碳酸鈉、硝酸鎂、硫酸銅、氯化鉀、氯化銨中的一種或幾種組成。為了檢驗它們所含的物質,做了以下實驗。①取部分粉末,加水溶解,得無色溶液。將所得溶液分成兩份,分別進行實驗;②在第一份溶液中滴加足量稀鹽酸,有氣泡產生,繼續往反應后的溶液中滴加AgNO3溶液有白色沉淀生成;③在第二份溶液中滴加氫氧化鈉溶液并加熱,將濕潤的紅色石蕊試紙放在試管口,試紙變藍。由此可判斷固體混合物中肯定含 (寫化學式,下同),肯定沒有 ,可能含有 。對可能有的物質,可采用 來檢驗,如果含有該物質,其現象是 。步驟③中有關的化學方程式為: 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鑒別下列各組物質,按要求回答問題。
(1)稀硫酸、稀鹽酸
①可選作鑒別的試劑有(填編號,可多選)_________。
A.BaCl2溶液 B.Mg(NO3)2溶液 C.Na2CO3溶液
②鑒別反應的離子方程式:_________________________。
(2)飽和碳酸鈉溶液、澄清石灰水
①可選用鑒別的試劑有(填編號,可多選)____。
a.鹽酸 b.NaCI c.硝酸 d.BaCl2溶液
②依次寫出鑒別中有明顯現象的反應的離子方程式:________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
為了達到下列表格中的實驗要求,請從供選擇的化學試劑及實驗方法中選出合適的,將其標號填入對應的空格中。
| 實驗要求 | 試劑及方法 |
| 證明明礬水溶液呈酸性 | |
| 鑒別甲烷與乙烯 | |
| 除去MgO中含有的Al2O3 | |
| 鑒別乙醇和乙醛 | |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(18分)NO很容易與許多分子迅速發生反應,科學家發現在生物體中不斷地產生NO,用于細胞間傳遞信息;NO還參與心血管系統、免疫系統以及中樞和外圍神經系統的調控。
Ⅰ.(1)實驗室用金屬銅和稀硝酸制取NO的離子方程式為
_____________________________________________________。
(2)NO是有毒氣體,某學生為防止污染,用分液漏斗和燒杯裝配了一套簡易的、能隨開隨用、隨關隨停的NO氣體發生裝置,如圖甲所示。
①實驗室若沒有銅絲,而只有小銅粒,在使用上述裝置進行實驗時,可用絲狀材料包裹銅粒以代替銅絲進行實驗,這種絲狀材料的成分可以是________(填選項編號)。
| A.鐵 | B.鋁 | C.鉑 | D.玻璃 |



查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com