
某課外活動小組設計了如圖所示的裝置,調節滑動變阻器控制電流強度適中的情況下用其進行緩慢電解NaCl溶液及相關實驗(此時,打開止水夾a,關閉止水夾b)。由于粗心,實驗并未達到預期目的,但也看到了很令人高興的現象。(陽離子交換膜只允許陽離子和水通過)
請幫助他們分析并回答下列問題:
(1)寫出B裝置中的電極反應:
陰極:________;陽極:________。
(2)觀察到A裝置中的現象是:①________;②________;③________。
(3)當觀察到A裝置中的現象后,他們關閉止水夾a,打開止水夾b。再觀察C裝置,若無現象,請說明理由;若有現象,請寫出有關反應的化學方程式(是離子反應的寫離子方程式):____________________________________。
(4)若想達到電解NaCl溶液的目的,應如何改進裝置,請提出你的意見:
__________________________________________________________________。
科目:高中化學 來源: 題型:填空題
(12分)(1)右圖為陽離子交換膜法電解飽和食鹽水(滴有酚酞)原理示意圖,E口產生H2,電解食鹽水的離子方程式為: ,溶液變紅色的是: 區(填A或B)。
(2)電化腐蝕是鋼鐵發生腐蝕的主要原因,又可分為吸氧腐蝕和析氫腐蝕,發生吸氧腐蝕的電極反應式:負極 正極
(3)下圖是一套電化學實驗裝置,圖中C、D均為鉑電極,U為鹽橋,G是靈敏電流計

此裝置中進行的反應是可逆反應,其反應方程式式為:AsO43-+2I-+H+ AsO33-+I2+H2O,向B杯中加入適量較濃的硫酸,發現G的指針向右偏移。此時A杯中的主要實驗現象是 D電極上的電極反應式為
AsO33-+I2+H2O,向B杯中加入適量較濃的硫酸,發現G的指針向右偏移。此時A杯中的主要實驗現象是 D電極上的電極反應式為
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某興趣小組利用如圖所示裝置進行實驗。
(1)斷開K2、閉合K1,U形管內除電極上有氣泡外,還可觀察到的現象是 ;陽極電極反應式為 。當電路中轉移0.001mol電子時,右側注射器最多可以收集到氣體 mL(折算為標準狀況)。
(2)斷開K2、閉合K1一段時間,待注射器中充有一定量的氣體后,斷開K1、閉合K2,此時裝置內化學能轉化為電能。實現能量轉化的化學方程式為 ;
(3)假設實驗裝置不漏氣,當(2)中注射器內氣體全部參加反應后,U形管內的溶液理論上 (填“能”或“不能”)恢復原樣。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某同學在做原電池原理的實驗時,有如下實驗步驟:
①用導線將靈敏電流計的兩端分別與純凈的鋅片和銅片相連接(如圖1);
②把一塊純凈的鋅片插入盛有稀硫酸的燒杯中;
③把一塊純凈的銅片插入盛有稀硫酸的燒杯中;
④用導線把鋅片和銅片連接起來后,再平行地插入盛有稀硫酸的燒杯中(如圖2)。
回答下列問題:
(1)實驗步驟①中應觀察到的現象是 。
(2)實驗步驟②中應觀察到的現象是 。
(3)實驗步驟③中應觀察到的現象是 。
(4)實驗步驟④中應觀察到的現象是 。
(5)通過實驗步驟④該同學頭腦中有了一個猜想(或假設),該猜想是 。
(6)為了證實該猜想,該同學又設計了第⑤步實驗,請簡要畫出第⑤步實驗的裝置示意圖。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業上電解飽和食鹽水能制取多種化工原料,其中部分原料可用于制備多晶硅。
(1)上圖是離子交換膜法電解飽和食鹽水示意圖,電解槽陽極產生的氣體是________;NaOH溶液的出口為________(填字母);精制飽和食鹽水的進口為________(填字母);干燥塔中應使用的液體是________。
(2)多晶硅主要采用SiHCl3還原工藝生產,其副產物SiCl4的綜合利用受到廣泛關注。
①SiCl4可制氣相白炭黑(與光導纖維主要原料相同),方法為高溫下SiCl4與H2和O2反應,產物有兩種,化學方程式為___________________________________。
②SiCl4可轉化為SiHCl3而循環使用,一定條件下,在20 L恒容密閉容器中的反應:
3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)
4SiHCl3(g)
達平衡后,H2和SiHCl3物質的量濃度分別為0.140 mol/L和0.020 mol/L,若H2全部來源于離子交換膜法的電解產物,理論上需消耗純NaCl的質量為________kg。
(3)采用無膜電解槽電解飽和食鹽水,可制取氯酸鈉,同時生成氫氣,現制得氯酸鈉213.0 kg,則生成氫氣________m3(標準狀況)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
新型鋰離子電池材料Li2MSiO4(M為Fe,Co,Mn,Cu等)是一種發展潛力很大的電池電極材料。工業制備Li2MSiO4有兩種方法。
方法一:固相法,2Li2SiO3+FeSO4 Li2FeSiO4+Li2SO4+SiO2。
Li2FeSiO4+Li2SO4+SiO2。
方法二:溶膠-凝膠法,CH3COOLi、Fe(NO3)3、Si(OC2H5)4等試劑 膠體
膠體 干凝膠
干凝膠 Li2FeSiO4。
Li2FeSiO4。
(1)固相法中制備Li2FeSiO4過程采用惰性氣體氣氛,其原因是
______________________________________________________________________。
(2)溶膠凝膠法中,檢查溶液中有膠體生成的方法是________;生產中,生成1 mol Li2FeSiO4整個過程轉移電子的物質的量為________mol。
(3)以Li2FeSiO4和嵌有Li的石墨為電極材料,含鋰的導電固體作電解質,構成電池的總反應式為Li+LiFeSiO4 Li2FeSiO4,則該電池的負極是________;充電時,陽極反應的電極反應式為________。
Li2FeSiO4,則該電池的負極是________;充電時,陽極反應的電極反應式為________。
(4)使用(3)組裝的電池必須先________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
有A、B兩位學生均想利用原電池反應驗證金屬的活動性順序,并探究產物的有關性質,分別設計了如圖所示的原電池,請完成下列問題:
(1)①負極材料:
A池________,B池________。
②電極反應式:
A池:正極:________,負極:________
B池:正極:________,負極:________
(2)B池總反應的離子方程式為_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)普通鋅錳干電池的結構如圖所示。回答下列問題。
①電池中電解質溶液為________。
②正極反應式為________。
③放電時,NH4+向________(填“正極”或“負極”)移動。
(2)廢電池中的鋅皮常用于實驗室制氫氣,廢鋅皮和純鋅粒分別與同濃度的稀硫酸反應,產生氫氣速率較大的是________,原因是________________________。
若用過量的純鋅粒與一定量的稀硫酸反應,為了加快反應速率又不影響產生氫氣的量,下列措施可行的是________(填序號)。
| A.微熱 |
| B.加入適量氧化銅 |
| C.加入少量硫酸銅溶液 |
| D.加水 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
電化學原理在工業生產中有著重要的作用,請利用所學知識回答有關問題。
(1)用電解的方法將硫化鈉溶液氧化為多硫化物的研究具有重要的實際意義,將硫化物轉變為多硫化物是電解法處理硫化氫廢氣的一個重要內容。如圖,是電解產生多硫化物的實驗裝置:
①已知陽極的反應為(x+1)S2-=Sx+S2-+2xe-,則陰極的電極反應式是________________________________________________________________________。
當反應轉移x mol電子時,產生的氣體體積為____________(標準狀況下)。
②將Na2S·9H2O溶于水中配制硫化物溶液時,通常是在氮氣氣氛下溶解。其原因是(用離子反應方程式表示):___________________________________________________。
(2)MnO2是一種重要的無機功能材料,制備MnO2的方法之一是以石墨為電極,電解酸化的MnSO4溶液,陽極的電極反應式為______________________。現以鉛蓄電池為電源電解酸化的MnSO4溶液,如圖所示,鉛蓄電池的總反應方程式為_______________________________________________,當蓄電池中有4 mol H+被消耗時,則電路中通過的電子的物質的量為________,MnO2的理論產量為________g。
(3)用圖電解裝置可制得具有凈水作用的FeO42-。實驗過程中,兩極均有氣體產生,Y極區溶液逐漸生成FeO42-。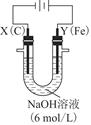
①電解過程中,X極區溶液的pH________(填“增大”“減小”或“不變”)。
②電解過程中,Y極發生的電極反應為Fe-6e-+8OH-=FeO42-+4H2O和________________________________________________________________________,
若在X極收集到672 mL氣體,在Y極收集到168 mL氣體(均已折算為標準狀況時氣體體積),則Y電極(鐵電極)質量減少________g。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com