
隨著大氣污染的日趨嚴重,“節能減排”,減少全球溫室氣體排放,研究NOx、SO2、CO等大氣污染氣體的處理具體有重要意義。
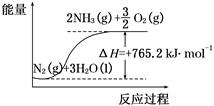
(1)如圖是在101 kPa,298K條件下1mol NO2和1mol CO反應生成1mol CO2和1mol NO過程中的能量變化示意圖。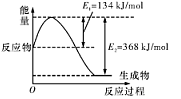
已知: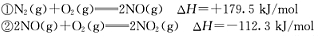
請寫出NO與CO反應生成無污染氣體的熱化學方
程式: 。
(2)將0.20 mol N02和0.10 mol CO充入一個容積恒定為1L的密閉容器中發生反應,在不同條件下,反應過程中部分物質的濃度變化狀況如圖所示。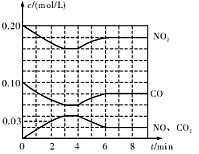
①下列說法正確的是 (填序號)。
a.容器內的壓強不發生變化說明該反應達到乎衡
b.當向容器中再充人0. 20 mol NO時,平衡向正反應方向移動,K增大
c.升高溫度后,K減小,N02的轉化率減小
d.向該容器內充人He氣,反應物的體積減小,濃度增大,所以反應速率增大
②計算產物NO在0~2 min內平均反應速率v(NO)= mol·L-1·min-1
③第4 min時改變的反應條件為 (填“升溫’’、“降溫’’)。
④計算反應在第6 min時的平衡常數K= 。若保持溫度不變,此時再向容器中充人CO、NO各0.060 mol,平衡將 移動(填“正向”、“逆向”或“不”)。
(3)有學者想以如圖所示裝置用原電池原理將SO2轉化為重要的化工原料。其負極反應式為 ,當有0.25 mol SO2被吸收,則通過質子(H+)交換膜的H+的物質的量為 mol。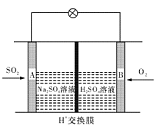
(1)2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-759.8kJ/mol;(2分)
(2)①c (2分) ②0.015 (2分)③升溫 (2分)④1/36 (2分) 逆向(2分)
(3)SO2+ 2H2O-2e-=SO42-+4H+ (2分) 0.5 (2分)
解析試題分析:(1)由圖知298K條件下1mol NO2和1mol CO反應生成1mol CO2和1mol NO 的熱化學方程式為NO2(g)+CO(g)=NO(g) +CO2(g)△H=-234kJ/mol ③;NO與CO反應生成無污染氣體是氮氣和二氧化碳氣體,根據蓋斯定律得②-①+2×③即為所求,所以答案是2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-759.8kJ/mol;
(2)①NO2(g)+CO(g)=NO(g) +CO2(g),該反應為反應前后氣體物質的量不變的可逆反應,壓強始終不變,a錯誤;b、體積不變,NO的物質的量增加,濃度增大,平衡逆向移動,K不變,錯誤;c、升高溫度后,平衡逆向移動,K減小,N02的轉化率減小,正確;d、充入氦氣,容器體積不變,所以反應物的濃度不變,平衡不移動,錯誤答選c;
②在0~2 min內NO的濃度增加0.03mol/L,所以v(NO)="0.03mol/L/2min=0.015" mol·L-1·min-1
③第4 min時反應物濃度增大,生成物濃度減小,說明平衡逆向移動,所以是升溫;
④6min時各物質的平衡濃度分別為c(NO2)="0.18" mol·L-1,c(CO)="0.08" mol·L-1,c(NO)=c(CO2)="0.02" mol·L-1,所以K= c(NO)·c(CO2)/c(NO2)·c(CO)=1/36;此時再向容器中充人CO、NO各0.060 mol,則c(NO)·c(CO2)/c(NO2)·c(CO)>1/36,所以平衡逆向移動;
(3)二氧化硫在負極通入,發生氧化反應,電極反應式為SO2+ 2H2O-2e-=SO42-+4H+,當有0.25molSO2被吸收時,轉移電子的物質的量是0.5mol,根據得失電子守恒,正極發生O2+4e-+4H+=2H2O,則通過質子(H+)交換膜的H+的物質的量為0.5mol。
考點:考查熱化學方程式和蓋斯定律的計算應用,化學平衡的移動,化學平衡常數的計算,電化學原理理解分析


科目:高中化學 來源: 題型:填空題
.(17分)減少污染、保護環境是全世界最熱門的課題。
(1)為了減少空氣中SO2的排放,常采取的措施有:
①將煤轉化為清潔氣體燃料。
已知:H2(g)+1/2O2(g)==H2O(g) ΔH1=-241.8 kJ·mol-1
C(s)+1/2O2(g)===CO(g) ΔH2=-110.5 kJ·mol-1
則焦炭與水蒸氣反應生成CO的熱化學方程式為 。
②洗滌含SO2的煙氣。以下物質可作洗滌劑的是 (填序號):
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(2)CO在催化劑作用下可以與H2反應生成甲醇:CO(g)+2H2(g)  CH3OH(g)。在密閉容器中充有10 mol CO與20 mol H2,CO的平衡轉化率與溫度、壓強的關系如右圖所示。
CH3OH(g)。在密閉容器中充有10 mol CO與20 mol H2,CO的平衡轉化率與溫度、壓強的關系如右圖所示。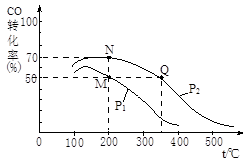
①M、N兩點平衡狀態下,容器中總物質的物質的量之比為:n(M)總:n(N)總= 。
②若M、N、Q三點的平衡常數KM、KN、KQ的大小關系為 。
(3)催化硝化法和電化學降解法可用于治理水中硝酸鹽的污染。
①催化硝化法中,用H2將NO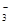 還原為N2,一段時間后,溶液的堿性
還原為N2,一段時間后,溶液的堿性
明顯增強。則該反應離子方程式為 。
②電化學降解NO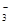 的原理如圖所示,電源正極為 (填“a”或“b”);
的原理如圖所示,電源正極為 (填“a”或“b”);
若總反應為4NO3-+4H+通電5O2↑+2N2↑+2H2O,則陰極反應式為 。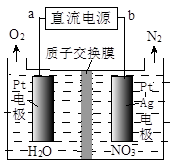
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
研究人員通過對北京地區PM2.5的化學組成研究發現,汽車尾氣和燃煤污染分別 占4%、l8%
I.(1)用于凈化汽車尾氣的反應為:2NO(g)+2CO(g) 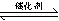 2CO2(g)+N2(g),已知該反應在570K時的平衡常數為1×1059,但反應速率極慢。下列說法正確的是:
2CO2(g)+N2(g),已知該反應在570K時的平衡常數為1×1059,但反應速率極慢。下列說法正確的是:
| A.裝有尾氣凈化裝置的汽車排出的氣體中不再含有NO或CO |
| B.提高尾氣凈化效率的最佳途徑是使用高效催化劑 |
| C.增大壓強,上述平衡右移,故實際操作中可通過增壓的方式提高其凈化效率 |
| D.提高尾氣凈化效率的常用方法是升高溫度 |
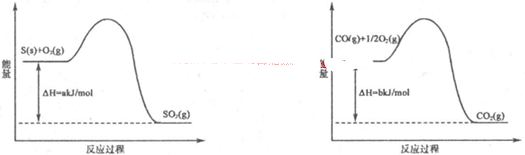
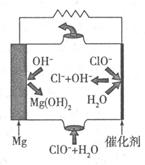
 N2(g)+CO2(g)
N2(g)+CO2(g)  H=akJ·mol-1,向某密閉容器加入一定量的活性炭和NO,恒溫(T1℃)條件下反應,反應進行到不同時間測得各物質的濃度如下:
H=akJ·mol-1,向某密閉容器加入一定量的活性炭和NO,恒溫(T1℃)條件下反應,反應進行到不同時間測得各物質的濃度如下:| 濃度/mol·L-1 時間/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.050 | 0.025 | 0.025 |
| 30 | 0.050 | 0.025 | 0.025 |
| 40 | 0.036 | 0.032 | 0.010 |
| 50 | 0.036 | 0.032 | 0.010 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知某反應A(g)+B(g)??C(g)+D(g)過程中的能量變化如圖所示,回答問題。
該反應是 (填“吸熱”或“放熱”)反應,該反應的ΔH= kJ/mol(用含E1、E2的代數式表示),1 mol氣體A和1 mol氣體B具有的總能量比1 mol氣體C和1 mol氣體D具有的總能量 (填“一定高”“一定低”或“高低不一定”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
一種“人工固氮”的新方法是在常溫、常壓、光照條件下,N2在催化劑表面與水發生反應生成NH3:N2+3H2O 2NH3+O2
2NH3+O2
進一步研究NH3生成量與溫度的關系,部分實驗數據見下表(反應時間3 h):
| T/℃ | 30 | 40 | 50 |
| 生成NH3量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
 2NH3(g) ΔH=-92.4 kJ·mol-1。在某壓強恒定的密閉容器中加入2 mol N2和4 mol H2,達到平衡時,N2的轉化率為50%,體積變為10 L。求:
2NH3(g) ΔH=-92.4 kJ·mol-1。在某壓強恒定的密閉容器中加入2 mol N2和4 mol H2,達到平衡時,N2的轉化率為50%,體積變為10 L。求:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氨是重要的化工產品和化工原料。
(1)氨的電子式是 。
(2)已知: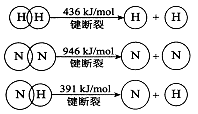
①合成氨的熱化學方程式是 。
②降低溫度,該反應的化學平衡常數K .(填“增大”、“減小’’或“不變”)。
(3)有人設想以N2和H2為反應物,以溶有A的稀鹽酸為電解質溶液,可制造出既能提供電能,又能固氮的新型燃料電池,裝置如圖l所示。
電池正極的電極反應式是 ,A是 。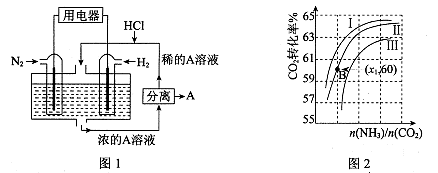
(4)用氨合成尿素的反應為2NH3(g)+CO2(g) CO(NH2)2(l)+ H2O(g)。工業生產時,原料氣帶有水蒸氣。圖2表示CO2的轉化率與氨碳比
CO(NH2)2(l)+ H2O(g)。工業生產時,原料氣帶有水蒸氣。圖2表示CO2的轉化率與氨碳比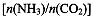 、水碳比
、水碳比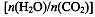 的變化關系。
的變化關系。
①曲線I、II、III對應的水碳比最大的是 。
②測得B點氨的轉化率為40%,則x1 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
天然氣、重油、煤都可以與水反應制得氫氣。下表是某合成氨廠采用不同原料時的相對投資費用和能量消耗的數據。
| 原料 | 天然氣 | 重油 | 煤 |
| 相對投資費用 | 1.0 | 1.5 | 2.0 |
| 能量消耗/J·t-1 | 28×109 | 38×109 | 48×109 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
火箭推進器中盛有強還原劑液態肼(N2H4)和強氧化劑液態雙氧水。當它們混合反應時,即產生大量氮氣和水蒸氣,并放出大量熱。已知0.4 mol液態肼與足量液態雙氧水反應,生成水蒸氣和氮氣,放出256.652 kJ的熱量。
(1)反應的熱化學方程式為 _________________________。
(2)已知H2O(l) H2O(g) ΔH="+44" kJ·mol-1則16 g液態肼與液態雙氧水反應生成液態水時放出的熱量是 kJ。
H2O(g) ΔH="+44" kJ·mol-1則16 g液態肼與液態雙氧水反應生成液態水時放出的熱量是 kJ。
(3)此反應用于火箭推進,除釋放大量熱和快速產生大量氣體外,還有一個很大的優點是
___________________________________。
(4)發射衛星可用肼為燃料,二氧化氮作氧化劑,兩者反應生成氮氣和水蒸氣。已知:
N2(g)+2O2(g) 2NO2(g) ΔH="+67.7" kJ·mol-1
2NO2(g) ΔH="+67.7" kJ·mol-1
N2H4(g)+O2(g) N2(g)+2H2O(g) ΔH="-534" kJ·mol-1
N2(g)+2H2O(g) ΔH="-534" kJ·mol-1
肼和二氧化氮反應的熱化學方程式為 __________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫的化合物在生產和科研中發揮著重要作用。
(1)SO2Cl2常用于制造醫藥品、染料、表面活性劑等。已知:SO2Cl2(g) SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某溫度時向體積為1 L的恒容密閉容器中充入0. 20mol SO2Cl2,達到平衡時,容器中含0.18mol SO2,則此過程反應吸收的熱量為_____kJ,該溫度時反應的平衡常數為_____。將上述所得混合氣體溶于足量BaCl2溶液中,最終生成沉淀的質量為_______。
SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某溫度時向體積為1 L的恒容密閉容器中充入0. 20mol SO2Cl2,達到平衡時,容器中含0.18mol SO2,則此過程反應吸收的熱量為_____kJ,該溫度時反應的平衡常數為_____。將上述所得混合氣體溶于足量BaCl2溶液中,最終生成沉淀的質量為_______。
(2)工業上制備硫酸的過程中存在反應:2SO2(g)+O2(g) 2SO3(g) △H=-198kJ·mol-1400℃,1.01×105Pa,向容積為2L的恒容密閉容器中充入一定量 SO2和O2,n(SO3)和n(O2)隨時間的變化曲線如圖所示。
2SO3(g) △H=-198kJ·mol-1400℃,1.01×105Pa,向容積為2L的恒容密閉容器中充入一定量 SO2和O2,n(SO3)和n(O2)隨時間的變化曲線如圖所示。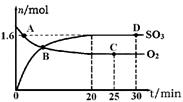
①0~20min反應的平均速率υ(O2)=___________。
②下列敘述正確的是 。
a.A點υ正(SO2)>υ逆(SO2)
b.B點處于平衡狀態
c.C點和D點n(SO2)相同
d.其它條件不變,500℃時反應達平衡,n(SO3)比圖中D點的值大
(3)工業上用Na2SO3溶液吸收煙氣中的SO2。將煙氣通入1.0 mol·L-1的Na2SO3溶液,當溶液pH約為6時,Na2SO3溶液吸收SO2的能力顯著下降,應更換吸收劑。此時溶液中c (SO32-)的濃度是0.2 mol·L-1,則溶液中c(HSO3-)是_________mol·L-1。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com