
制取尿素[CO(NH2)2]的反應:2NH3(g)+CO2(g) 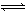 CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
某溫度下體積為10L的密閉容器中,測得各物質的物質的量數據如下:
| 物質的量mol | 0min | 2 min | 3 min | 4 min |
| NH3 | 2.0 | 1.4 | n1 | n1 |
| CO2 | 1.0 | 0.7 | n2 | n2 |
| H2O | 0 | 0.3 | n3[ | n3 |
(1)0.03mol/(L·min)(2分);1.2(2分)(2)K=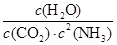 (2分)(3)CD(2分)
(2分)(3)CD(2分)
解析試題分析:(1)根據表中數據可知,0~2min內NH3的物質的量減少了2.0mol-1.4mol=0.6mol,其濃度變化量=0.6mol÷10L=0.06mol/L,所以氨氣的平均反應速率=0.06mol/L÷2min=0.03mol/(L·min)。
2NH3(g)+CO2(g) 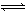 CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
起始量(mol) 2.0 1.0 0
變化量(mol) (2.0-n1) (1.0-0.5n1) (1.0-0.5n1)
平衡量(mol) n1 0.5 n1 (1.0-0.5n1)
則根據壓強之比是相應氣體的物質的量之比可知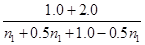 =
=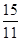
解得n1=1.2
(2)化學平衡常數是在一定條件下,當可逆反應達到平衡狀態時,生成物濃度的冪之積和反應物濃度的冪之積的比值,所以根據反應的方程式可知,該反應的平衡常數表達式K=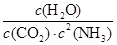 。
。
(3)在一定條件下,當可逆反應的正反應速率和逆反應速率相等時(但不為0),反應體系中各種物質的濃度或含量不再發生變化的狀態,稱為化學平衡狀態。A、反應速率之比等于相應的化學計量數之比,因此根據方程式可知,消耗NH3的物質的量與生成H2O的物質的量之比始終為2∶1,A不能說明反應達到平衡狀態;B、平衡時濃度不再發生變化,但物質的濃度之間不一定相等或滿足某種關系,因此c(NH3):c(CO2):c(H2O)=2∶1∶1不能說明反應達到平衡狀態;C、密度是混合氣的質量和容器容積的比值,在反應過程中容積始終是不變的,但質量是減少的,因此當氣體密度不再變化時可以說明反應達到平衡狀態;D、該反應是氣體體積減小的可逆反應,所以壓強也是減小的,因此容器壓強不再變化可以說明反應達到平衡狀態,答案選CD。
考點:考查反應速率的有關計算、平衡常數表達式、平衡狀態的判斷


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:填空題
汽車尾氣中含有CO、NO2等有毒氣體,對汽車加裝尾氣凈化裝置,可使有毒氣體相互反應轉化為無毒氣體。汽車尾氣中CO、NO2氣體在一定條件下可以發生反應:4CO(g)+2NO2(g) 4CO2(g)+N2(g) ΔH="-1" 200 kJ·mol-1
4CO2(g)+N2(g) ΔH="-1" 200 kJ·mol-1
(1)恒溫恒容條件下,不能說明該反應已達到平衡狀態的是 (填字母,下同)。
A.容器內混合氣體顏色不再變化
B.容器內的壓強保持不變
C.2v(NO2)逆=v(N2)正
D.容器內混合氣體密度保持不變
(2)能使該反應的反應速率增大,且平衡向逆反應方向移動的是 。
A.及時分離出CO2
B.適當升高溫度
C.減小容器體積使體系壓強增大
D.選擇高效催化劑
(3)對于該反應,溫度不同(T2>T1)、其他條件相同時,下列圖像正確的是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
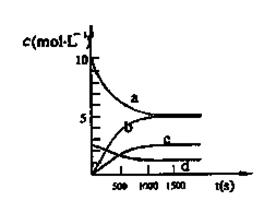
25 ℃時,在體積為2 L的密閉容器中,氣態A、B、C的物質的量n隨時間t的變化如圖1所示,已知達到平衡后,降低溫度,A的轉化率將增大。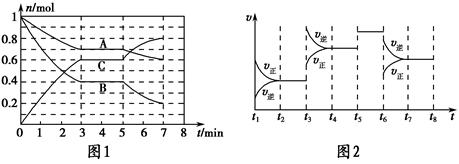
| t2~t3 | t4~t5 | t5~t6 | t7~t8 |
| K1 | K2 | K3 | K4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某溫度時,在一個容積為2 L的密閉容器中,X、Y、Z,三種物質的物質的量隨時間的變化曲線如圖所示。根據圖中數據,試填寫下列空白:
(1)該反應的化學方程式為______________;
(2)反應開始至2 min,用氣體Z表示的反應速率為_____;
(3)若X、Y、Z均為氣體,反應達到平衡時:
①壓強是開始時的________倍;
②若此時將容器的體積縮小為原來的 0.5倍,達到平衡時,容器內溫度將降低(容器不與外界進行熱交換),則該反應的正反應為________反應(填“放熱”或“吸熱”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
一定溫度下,在2L密閉容器中NO2和O2可發生下列反應: 4NO2(g)+O2(g)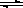 2N2O5(g)+5286 kJ已知體系中n(NO2)隨時間變化如下表:
2N2O5(g)+5286 kJ已知體系中n(NO2)隨時間變化如下表:
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一定體積的密閉容器中,進行化學反應CO2 (g)+H2 (g) CO (g)+H2O (g),其化學平衡常數K和溫度t的關系如下表:
CO (g)+H2O (g),其化學平衡常數K和溫度t的關系如下表:
| t / ℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
化學反應原理在科研和生產中有廣泛應用。
Ⅰ、如圖裝置所示,A、B中的電極為多孔的惰性電極;C、D為夾在浸有Na2SO4溶液的濾紙條上的鉑夾;電源有a、b兩極。若A、B中充滿KOH溶液后倒立于KOH溶液的水槽中。切斷K1,閉合K2、K3通直流電。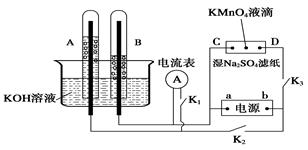
回答下列問題:
(1) a是電源的 極,寫出A中的電極反應式為_____。
(2)濕的Na2SO4濾紙條上能觀察到的現象有____________。
(3)電解一段時間后,A、B中均有氣體包圍電極,若此時切斷K2、K3,閉合K1,發現電流表的指針移動,寫出此時B中的電極反應式為 。
Ⅱ、甲醇是一種可再生能源,具有廣泛的開發和應用前景。工業上一般采用下列反應合成甲醇:CO(g)+2H2(g)  CH3OH(g) ΔH,下表所列數據是該反應在不同溫度下的化學平衡常數(K)。請回答下列問題:
CH3OH(g) ΔH,下表所列數據是該反應在不同溫度下的化學平衡常數(K)。請回答下列問題:
| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
Ⅰ.課本中通過向草酸(H2C2O4)溶液中滴加用硫酸酸化高錳酸鉀中研究濃度對化學反應速率的影響,請你寫出該反應的化學方程式 ,該反應不需使用指示劑的原因是 ;
Ⅱ.某同學根據課本外界條件對化學反應速率的影響原理,設計了硫代硫酸鈉與硫酸反應有關實驗,實驗過程的數據記錄如下(見表格),請結合表中信息,回答有關問題:
| 實驗 序號 | 反應溫度 (℃) | 參加反應的物質 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/mol?L-1 | V/mL | c/mol?L-1 | V/mL | ||
| A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| B | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
| C | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
| D | 40 | 5 | 0.1 | 10 | 0.1 | 5 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在體積為10L的容器中,通人一定量的CO和H2O,在850℃時發生如下反應:
CO(g)十H2O(g)  CO2(g)十H2 (g) △H<0 , CO和H2O濃度變化如下圖,
CO2(g)十H2 (g) △H<0 , CO和H2O濃度變化如下圖,
(1) 3min—4min之間反應處于____狀態(填平衡、不平衡);
(2)要使反應在8min后,平衡向逆方向移動,可采取的措施是__ ___,要使反應在8min后,反應速率降低,平衡向正方向移動,可采取的措施是________。(填a,b,c,d)
a.增加水蒸氣 b.降低溫度 c.使用催化劑 d.增加氫氣濃度
(3)求出850℃ 時,該反應的平衡常數和CO的平衡轉化率(寫出詳細計算過程)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com