
閃鋅礦(主要成份為ZnS)是含鋅主要礦物之一,空氣中高溫加熱閃鋅礦生成ZnO和SO2。ZnO用于冶煉金屬鋅,SO2可制亞硫酸鹽或硫酸。回答下列問題(以下計算保留2位小數)
(1)取1.56 g閃鋅礦樣品,在空氣中高溫加熱(雜質不反應),充分反應后,冷卻,得到殘留
固體的質量為1.32 g,樣品中含硫化鋅的質量分數是_________。
(2)取1.95 g鋅加入到12.00 mL 18.4 mol/L的濃硫酸中(反應中只生成一種還原產物),充分反應后,小心地將溶液稀釋到1000 mL,取出15.00 mL,以酚酞為指示劑,用0.25 mol/L的NaOH溶液中和余酸,耗用NaOH溶液的體積為21.70 mL。
①反應后溶液中多余的硫酸是____________ mol。
②通過計算確定濃硫酸被還原的產物是________________________。
(3)將標況下4.48 L SO2氣體慢慢通入200 mL一定濃度NaOH溶液中,SO2氣體全部被吸收,將反應后的溶液在空氣中小心蒸干(不考慮酸式鹽的分解),得到不超過兩種物質的無水晶體26.8g。通過計算確定所得晶體的成分與物質的量。
(1)0.93
(2)0.18mol (2分)還原產物是S。(2分) (3)
(3)



解析試題分析:(1)設閃鋅礦中ZnS的質量為x,雜質為y
2ZnS+3O2="2" ZnO+2SO2
x/97 x/97
有
解得x=1.455g,y=0.105g,所以樣品中w(ZnS)=1.455g÷1.56g×100%=93%
(2)設濃硫酸被還原的產物中S的化合價為x。56、根據題意過量的硫酸用堿滴定,則過量的硫酸n(H2SO4)= n(NaOH)×1000/15="0.25" mol/L×0.02170 L×1000/15=0.1808mol,所以反應的硫酸n(H2SO4)="18.4" mol/L×0.012L-0.1808mol=0.04mol,又反應后溶液為硫酸鋅,所以n(ZnSO4)= n(Zn)="1.95" g÷65g/mol=0.03mol,所以作酸的硫酸n(H2SO4)= n(ZnSO4)=0.03mol,做氧化劑硫酸n(H2SO4)=0.04mol-0.03mol=0.01mol,因為Zn反應0.03mol失去0.06mol電子,所以根據得失電子守恒,(+6-x) ×0.01mol=0.06mol,解得x=0,所以還原產物中S的化合價為0價,還原產物為S單質。
(3)n(SO2)=0.2mol,通入未知濃度的NaOH溶液,若NaOH溶液過量則所得溶液為Na2SO3 、NaOH;若恰好完全反應則所的溶液為Na2SO3 溶液;若SO2稍過量則所得溶液為Na2SO3 、NaHSO3 ;若SO2過量恰好完全被吸收則生成NaHSO3 溶液;(1)若所得溶液為Na2SO3 、NaOH:則有n(Na2SO3)= n(SO2)=0.2mol,則m(Na2SO3)=25.2g<26.8g,蒸干后若得到的是Na2SO3 、NaOH時,滿足條件,此時m(NaOH)= 26.8g-25.2g=1.6g,即n(NaOH)=0.04mol.(2)若恰好完全反應所得溶液為Na2SO3 :因n(Na2SO3)= n(SO2)=0.2mol,則m(Na2SO3)=25.2g<26.8g,蒸干后必有部分Na2SO3 被氧化為Na2SO4 ;設n(Na2SO3)=x,n(Na2SO4)=y,則有:
解得x=0.1mol,y=0.1mol即n(Na2SO3)=0.1mol,n(Na2SO4)= 0.1mol.(3)若SO2稍過量所得溶液為Na2SO3 、NaHSO3 :當蒸干后固體全為Na2SO3時,m(Na2SO3)=25.2g<26.8g,所以蒸干溶液后所得晶體不可能是Na2SO3 、NaHSO3 組合;當蒸干后固體全為Na2SO4 時,m(Na2SO4)="0.2mol×142g/mol=28.4g" >26.8g,所以蒸干后不可能全是Na2SO4,可以是Na2SO4 和NaHSO3或者是Na2SO4 和NaHSO4 ,因此有
設n(NaHSO3)=x,n(Na2SO4)=y
解得x=0.042mol,y=0.158mol即n(NaHSO3)= 0.042mol,n(Na2SO4)= 0.158mol
設n(NaHSO4)=x,n(Na2SO4)=y
解得x=0.073mol,y=0.127mol即n(NaHSO3)= 0.073mol,n(Na2SO4)= 0.127mol。(4)若SO2過量恰好被吸收所得溶液為NaHSO3 :則蒸干后所得固體無論是NaHSO3 還是NaHSO4 或者二者混合,都不可能。
考點:本題考查的是氧化還原計算、金屬與酸反應計算、多元酸的酸性氧化物與堿反應的計算。


科目:高中化學 來源: 題型:填空題
實驗室配制480 mL 0.600 mol·L-1的NaCl溶液,有如下操作步驟:
①把稱量好的NaCl晶體放入小燒杯中,加適量蒸餾水溶解
②把①所得溶液小心轉入容量瓶中
③繼續向容量瓶中加蒸餾水至液面距刻度線1 cm~2 cm處,改用膠頭滴管小心滴加蒸餾水至溶液凹液面與刻度線相切
④用少量蒸餾水洗滌燒杯和玻璃棒2~3次,每次洗滌的液體都小心轉入容量瓶,并輕輕搖勻
⑤將容量瓶瓶塞塞緊,充分搖勻
請填寫下列空白:
(1)操作步驟的正確順序為(填序號) 。
(2)實驗室有如下規格的容量瓶:①100 mL,②250 mL,③500 mL,④1000 mL,本實驗選用(填序號) 。
(3)本實驗用到的基本實驗儀器除容量瓶、玻璃棒外,還有 。
(4)需要使用玻璃棒的操作有 (填步驟序號),其作用為 。
(5)誤差分析:(填“偏高”“偏低”或“無影響”)
①稱量NaCl時,物碼倒置(1 g以下用游碼) 。
②某同學觀察液面的情況如右圖所示,對所配溶液濃度將有何影響 。
③沒有進行操作步驟④ 。
④加蒸餾水時不慎超過了刻度線,立即用膠頭滴管將多余的水吸出 。
⑤容量瓶中原來有少量水 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下圖是200 mg MnC2O4·2H2O晶體放在坩堝里加熱分解時,所得固體產物的質量(m)隨溫度(T)變化的曲線(已知草酸錳不穩定,但其中錳元素的化合價在300 ℃以下不變)。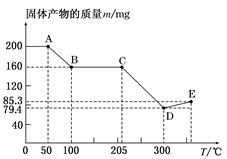
試回答下列問題:
(1)寫出B點固體產物的化學式:_________________________________________。
(2)從B點到C點過程中固體物質質量不變的原因是_____________________________________________________。
(3)通過計算確定D點產物的相對分子質量,并推斷其合理的化學式:____________
(4)從D點到E點過程中固體物質質量增加的原因是___________________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
把2.0mol/LCuSO4溶液和1.0mol/LH2SO4溶液等體積混合(假設混合后溶液的體積等于兩溶液的體積之和)。
(1)溶液中H+的物質的量濃度為 ,SO42-的物質的量濃度為 。
(2)向混合溶液中加入足量的鐵粉,經足夠長的時間后,鐵粉有剩余。此時,溶液中的Fe2+物質的量濃度為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
向200 mL 某物質的量濃度的NaOH溶液中緩慢通入一定量的CO2,充分反應后,得到Na2CO3和NaHCO3的混合溶液。向上述所得溶液中,逐滴滴加2 mol·L-1的鹽酸,所得氣體的體積與所加鹽酸的體積關系如圖所示: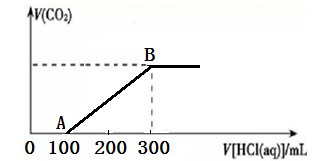
(1)OA段、AB段發生反應的離子方程式__________________、__________________。
(2)B點時,反應所得溶液中溶質的物質的量濃度是______________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
取20 mL NaOH溶液平均分成兩份,分別放入A、B兩支試管中。向A、B中通入不等量的CO2,再繼續向兩溶液中逐滴加入0.1mol/L的鹽酸,標準狀況下產生的CO2氣體體積與所加的鹽酸溶液體積之間的關系如下表所示:
| 鹽酸體積(單位:mL) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| A產生CO2的體積 | 0 | 0 | 0 | 0 | 0 | 22.4 | 44.8 | 44.8 | 44.8 |
| B產生CO2的體積 | 0 | 0 | 22.4 | 44.8 | 67.2 | 89.6 | x | x | x |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
天然堿的組成可以用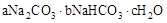 (a、b、c為整數)表示。現有A、B兩種不同的天然堿樣品,分別進行如下實驗以確定其化學式。
(a、b、c為整數)表示。現有A、B兩種不同的天然堿樣品,分別進行如下實驗以確定其化學式。
將質量為31.0 g的天然堿A于300℃加熱分解至完全(300℃時Na2CO3不分解),產生CO2 2.24 L(標準狀況)和水5.4 g。
(1)天然堿A的化學式中: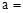
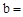

已知:Na2CO3與稀鹽酸的反應分下列兩步進行:
Na2CO3+HCl NaCl+NaHCO3 NaHCO3+HCl
NaCl+NaHCO3 NaHCO3+HCl NaCl+CO2↑+H2O
NaCl+CO2↑+H2O
將質量為12.45 g的天然堿B溶于水,逐滴滴加某濃度的稀鹽酸,產生氣體的體積與加入鹽
酸的體積(標準狀況)的關系如下表所示:
| 鹽酸體積(mL) | 20 | 40 | 60 | 80 |
| 產生氣體體積(mL) | 0 | 560 | 1680 | 2520 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)①現有11g由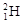 和
和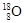 組成的水分子的物質的量 mol,其中含中子數為 mol,電子數為 個。
組成的水分子的物質的量 mol,其中含中子數為 mol,電子數為 個。
②請畫出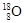 2-微粒的結構示意圖: 。
2-微粒的結構示意圖: 。
(2)質量相等的兩種物質SO2和SO3,兩種物質中硫元素質量之比為 ,分子物質的量之比為 ,所含氧原子個數之比為 。
(3)0.2L 0.5mol/L Al2(SO4)3溶液和0.5L 0.5mol/L Al2(SO4)3溶液所含SO42—離子濃度之比為____________,SO42—離子數目之比為____________。
(4)20.6g NaR 含有Na+0.2mol,則NaR的摩爾質量為 ,則含R 8.0g 的NaR的物質的量為 mol 。
(5)實驗室用二氧化錳與濃鹽酸反應制取氯氣,反應方程式如下:
MnO2+4HCl(濃) MnCl2+2H2O+Cl2↑。若0.1 molMnO4與足量的濃鹽酸充分反應,則有 mol HCl被氧化,轉移電子的物質的量為 mol,產生的Cl 2在標準狀況下的體積為 L。
MnCl2+2H2O+Cl2↑。若0.1 molMnO4與足量的濃鹽酸充分反應,則有 mol HCl被氧化,轉移電子的物質的量為 mol,產生的Cl 2在標準狀況下的體積為 L。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氨和聯氨(N2H4)是氮的兩種常見化合物,在科學技術和生產中有重要的應用。根據題意完成下列計算:
(1)聯氨用亞硝酸氧化生成氮的另一種氫化物,該氫化物的相對分子質量為43.0,其中氮原子的質量分數為0.977,計算確定該氫化物的分子式為________。該氫化物受撞擊則完全分解為氮氣和氫氣。4.30 g該氫化物受撞擊后產生的氣體在標準狀況下的體積為________L。
(2)聯氨和四氧化二氮可用作火箭推進劑,聯氨是燃料,四氧化二氮做氧化劑,反應產物是氮氣和水。由聯氨和四氧化二氮組成的火箭推進劑完全反應生成72.0 kg水,則推進劑中聯氨的質量________。
(3)氨的水溶液可用于吸收NO與NO2混合氣體,反應方程式為6NO+ 4NH3=5N2+6H2O 6NO2+ 8NH3=7N2+12H2O。NO與NO2混合氣體180 mol被8.90×103g氨水(質量分數0.300)完全吸收,產生156 mol氮氣。吸收后氨水密度為0.980 g/cm3。則①該混合氣體中NO與NO2的體積比為________,②吸收后氨水的物質的量濃度________(答案保留1位小數)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com