
甲醇是一種可再生能源,具有廣泛的開發(fā)和應(yīng)用前景.
(1)工業(yè)上一般采用下列兩種反應(yīng)合成甲醇: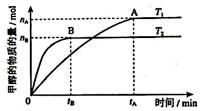
反應(yīng)I: CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反應(yīng)II: CO2(g)+3H2(g) CH3OH(g)+ H2O(g) ΔH2
CH3OH(g)+ H2O(g) ΔH2
①上述反應(yīng)符合“原子經(jīng)濟(jì)”原則的是 (填“I”或“Ⅱ”).
②在其他條件不變得情況下,考察溫度對(duì)反應(yīng)II的影響,實(shí)驗(yàn)結(jié)果如圖所示
由圖中數(shù)據(jù)判斷 ΔH2 0 (填“>”,“=”或“<”).
③某溫度下,將2 mol CO2和6 mol H2充入2L的密閉容器中,發(fā)生反應(yīng)II,達(dá)到平衡后,測(cè)得c(CO2)= 0.2 mol/L, 則此時(shí)容器中的壓強(qiáng)為原來的 倍
(2)已知在常溫常壓下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH =-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH =-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH =-44.0 kJ/mol
請(qǐng)計(jì)算1 mol甲醇不完全燃燒生成1 mol一氧化碳和液態(tài)水放出的熱量為 。
(3)某實(shí)驗(yàn)小組依據(jù)甲醇燃燒的反應(yīng)原理,設(shè)計(jì)如圖所示的電池裝置.
①該電池負(fù)極的電極反應(yīng)為
②此電池消耗甲醇1.6克時(shí),反應(yīng)中電子轉(zhuǎn)移數(shù)目為
③若以此燃料電池為鉛蓄電池充電,則應(yīng)將圖中右側(cè)電極連接蓄電池的 (填正極或負(fù)極)
(1) ① I ② < ③ 0.6 (2)442.8 KJ (3)CH3OH+8OH- -6e- = CO32- +6H2O0.3NA 負(fù)極
解析試題分析:(1)原子經(jīng)濟(jì)就是反應(yīng)物的原子全部轉(zhuǎn)化為生成物。選擇反應(yīng)I的化合反應(yīng)。由圖可知:T2>T1。升高溫度甲醇的物質(zhì)的量減少,說明升高溫度化學(xué)平衡向逆反應(yīng)方向移動(dòng)。根據(jù)平衡移動(dòng)原理:升高溫度化學(xué)平衡向吸熱反應(yīng)方向移動(dòng)。即逆反應(yīng)方向是吸熱反應(yīng),所以正反應(yīng)是放熱反應(yīng)。故△H2<0.③反應(yīng)開始時(shí)C(CO2)="1mol/L," C(H2)=3mol/L由于達(dá)到平衡后,測(cè)得c(CO2)= 0.2 mol/L,CO2改變濃度是0.8mol/L,所以H2改變濃度為2.4mol/L. H2平衡濃度為0.6mol/L.產(chǎn)生的甲醇、水蒸汽的濃度都是0.8mol/L.平衡時(shí)總濃度是2.4mol/L,而開始時(shí)總濃度是4mol/L。所以這時(shí)的壓強(qiáng)是開始的2.4mol/L÷4mol/L=0.6倍。(2)①-②+③×4得:2CH3OH(l) + 2O2(g) =" 2CO" (g) + 4H2O(l) ΔH =-1275.6 kJ/molΔH =-885.6 kJ/mol。所以產(chǎn)生1mol一氧化碳和液態(tài)水放出的熱量為442.8 KJ.(3)甲醇燃料電池的負(fù)極是通入甲醇的電極,電極反應(yīng)為CH3OH+8OH- -6e- = CO32- +6H2O。每摩爾的甲醇反應(yīng)轉(zhuǎn)移電子9摩爾。消耗甲醇1.6克時(shí),n(CH3OH)=1.6g÷32g/mol=0.05mol,所以轉(zhuǎn)移電子0.3 NA。③若以此燃料電池為鉛蓄電池充電,則應(yīng)將圖中右側(cè)電極連接蓄電池的負(fù)極。
考點(diǎn):考查燃料電池、電解池的由于及電極反應(yīng)、電子轉(zhuǎn)移等知識(shí)。


 名校課堂系列答案
名校課堂系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:填空題
I.已知:反應(yīng)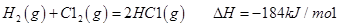
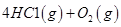
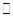
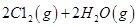

請(qǐng)回答: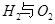 反應(yīng)生成氣態(tài)水的熱化學(xué)方程式__________________________
反應(yīng)生成氣態(tài)水的熱化學(xué)方程式__________________________
II.實(shí)施以減少能源浪費(fèi)和降低廢氣排放為基本內(nèi)容的節(jié)能減排政策,是應(yīng)對(duì)全球氣候問題、建設(shè)資源節(jié)約型、環(huán)境友好型社會(huì)的必然選擇。化工業(yè)的發(fā)展必須符合國(guó)家節(jié)能減排的總體要求。試運(yùn)用所學(xué)知識(shí),解決下列問題:
(1)已知某反應(yīng)的平衡表達(dá)式為: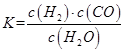
它所對(duì)應(yīng)的化學(xué)方程式為:_________________________________________________
(2)已知在400℃時(shí),反應(yīng)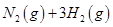
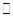
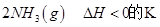 =0.5,則400℃時(shí),在0.5L的反應(yīng)容器中進(jìn)行合成氨反應(yīng),一段時(shí)間后,測(cè)得N2、H2、NH3的物質(zhì)的量分別為2mol、1mol、2mol,則此時(shí)反應(yīng)
=0.5,則400℃時(shí),在0.5L的反應(yīng)容器中進(jìn)行合成氨反應(yīng),一段時(shí)間后,測(cè)得N2、H2、NH3的物質(zhì)的量分別為2mol、1mol、2mol,則此時(shí)反應(yīng)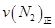 ____________
____________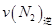 (填:>、<、=、不能確定);
(填:>、<、=、不能確定);
欲使得該反應(yīng)的化學(xué)反應(yīng)速率加快,同時(shí)使平衡時(shí)NH3的體積分?jǐn)?shù)增加,
可采取的正確措施是____________(填序號(hào))
A.加催化劑 B.升高溫度 C.縮小體積增大壓強(qiáng) D.使氨氣液化移走
(3)在一定體積的密閉容器中,進(jìn)行如下化學(xué)反應(yīng):
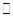
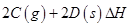 ,其化學(xué)平衡常數(shù)K與溫度T的關(guān)系如下表:
,其化學(xué)平衡常數(shù)K與溫度T的關(guān)系如下表:
請(qǐng)完成下列問題:
①判斷該反應(yīng)的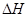 ___________0(填“>”或“<”)
___________0(填“>”或“<”)
②在一定條件下,能判斷該反應(yīng)一定達(dá)化學(xué)平衡狀態(tài)的是___________(填序號(hào))。
A. B.容器內(nèi)壓強(qiáng)保持不變
B.容器內(nèi)壓強(qiáng)保持不變
C.A和B的轉(zhuǎn)化率相等 D.混合氣體的密度保持不變
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
工業(yè)制硫酸時(shí),利用催化氧化反應(yīng)將SO2轉(zhuǎn)化為SO3是一個(gè)關(guān)鍵步驟。
(1)某溫度下,2SO2(g)+O2(g) 2SO3(g) △H="-197" kj/mol。開始時(shí)在10 L的密閉容器中加入4.0 mol SO2(g)和10.0 mol O2(g),當(dāng)反應(yīng)達(dá)到平衡時(shí)共放出197kJ的熱量,該溫度下的平衡常數(shù)K= ,升高溫度K將 (填“增大、減小或不變”)。
2SO3(g) △H="-197" kj/mol。開始時(shí)在10 L的密閉容器中加入4.0 mol SO2(g)和10.0 mol O2(g),當(dāng)反應(yīng)達(dá)到平衡時(shí)共放出197kJ的熱量,該溫度下的平衡常數(shù)K= ,升高溫度K將 (填“增大、減小或不變”)。
(2)一定條件下,向一帶活塞的密閉容器中充入2mol SO2和1mol O2,發(fā)生下列反應(yīng): 2SO2(g)+O2(g) 2SO3(g),達(dá)到平衡后,改變下述條件,SO2、O2、SO3的平衡濃度都比原來增大的是 (填字母)。
2SO2(g)+O2(g) 2SO3(g),達(dá)到平衡后,改變下述條件,SO2、O2、SO3的平衡濃度都比原來增大的是 (填字母)。
A.恒溫恒容,充入2mol SO3 B.恒溫恒容,充入2mol N2
C.恒溫恒壓,充入1 mol SO3 D.升高溫度
(3)在一密閉容器中進(jìn)行下列反應(yīng):2SO2(g)+O2(g)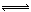 2SO3(g),化學(xué)興趣小組的同學(xué)探究了其他條件不變時(shí),改變某一條件時(shí)對(duì)上述反應(yīng)的影響,并根據(jù)實(shí)驗(yàn)數(shù)據(jù)作出了下列關(guān)系圖。下列判斷中正確的是 (填字母)。
2SO3(g),化學(xué)興趣小組的同學(xué)探究了其他條件不變時(shí),改變某一條件時(shí)對(duì)上述反應(yīng)的影響,并根據(jù)實(shí)驗(yàn)數(shù)據(jù)作出了下列關(guān)系圖。下列判斷中正確的是 (填字母)。
A.圖Ⅰ研究的是不同催化劑對(duì)反應(yīng)的影響,且乙使用的催化劑效率較高
B.圖Ⅱ研究的是壓強(qiáng)對(duì)反應(yīng)的影響,且甲的壓強(qiáng)較高
C.圖Ⅱ研究的是溫度對(duì)反應(yīng)的影響,且乙的溫度較低
D.圖Ⅲ研究的是不同催化劑對(duì)反應(yīng)的影響,且甲使用的催化劑效率較高
(4)某實(shí)驗(yàn)小組設(shè)想如下圖所示裝置用電化學(xué)原理生產(chǎn)硫酸,寫出通入SO2的電極的電極反應(yīng)式: 。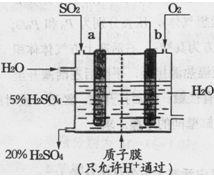
(5)焙燒產(chǎn)生的SO2可用于制硫酸。已知25℃、101 kPa時(shí):
SO2(g)+O2(g) 2SO3(g) △H1="-197" kJ/mol;
2SO3(g) △H1="-197" kJ/mol;
H2O(g)=H2O(1) △H2="-44" kJ/mol:
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(1) H3="-545" kJ/mol。
寫出SO3(g)與H2O(1)反應(yīng)的熱化學(xué)方程式是 。
(6)由硫酸可制得硫酸鹽.在一定溫度下,向K2SO4溶液中滴加Na2CO3溶液和BaCl2溶液,當(dāng)兩種沉淀共存時(shí),SO42-和CO32-的濃度之比 。[已知該溫度時(shí),Ksp(BaSO4)=1.3x10-10,KsP(BaCO3)=5.2x10-9]。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
2SO2(g)+ O2(g) 2SO3(g) △H =" a" kJ·mol-1,反應(yīng)過程的能量變化如圖所示。已知1mol SO2(g)完全轉(zhuǎn)化為1mol SO3(g)放熱99 kJ。請(qǐng)回答:
2SO3(g) △H =" a" kJ·mol-1,反應(yīng)過程的能量變化如圖所示。已知1mol SO2(g)完全轉(zhuǎn)化為1mol SO3(g)放熱99 kJ。請(qǐng)回答:
(1)圖中A點(diǎn)表示_______________________,a="__________" 。
(2) Ea的大小對(duì)該反應(yīng)的△H _______(填“有” 或“無”)影響。該反應(yīng)常用V2O5作催化劑,加入V2O5會(huì)使圖中B點(diǎn)_________(填“升高”、“降低”或“不變”)。
(3)已知單質(zhì)硫的標(biāo)準(zhǔn)燃燒熱為296kJ·mol-1,寫出反應(yīng)的熱化學(xué)方程式:________________________ ____,常溫常壓下,由單質(zhì)硫和氧氣經(jīng)兩步反應(yīng),若生成1mol SO3(g),放出的總熱量為___ ___ 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
已知H2(g)和CO(g)的燃燒熱△H分別為-285.8kJ·mol-1、-283.0kJ·mol。
則一氧化碳與液態(tài)水反應(yīng),生成二氧化碳和氫氣的熱化學(xué)方程式為
________________________________________________________;
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
由于催化劑可以為化學(xué)工業(yè)生產(chǎn)帶來巨大的經(jīng)濟(jì)效益,催化劑研究和尋找一直是受到重視的高科技領(lǐng)域。
(1)V2O5是接觸法制硫酸的催化劑。下圖為硫酸生產(chǎn)過程中2SO2 (g) + O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1反應(yīng)過程的能量變化示意圖。
2SO3(g) ΔH=-196.6 kJ·mol-1反應(yīng)過程的能量變化示意圖。
①V2O5的使用會(huì)使圖中B點(diǎn) (填“升高”、“降低”)。
②一定條件下,SO2與空氣反應(yīng)tmin后,SO2和SO3物質(zhì)的量濃度分別為a mol/L和b mol/L,則SO2起始物質(zhì)的量濃度為 mol/L;生成SO3的化學(xué)反應(yīng)速率為 mol/(L·min)。
(2)下圖是一種以銅、稀硫酸為原料生產(chǎn)藍(lán)礬的生產(chǎn)流程示意圖。
①生成CuSO4的總反應(yīng)為2Cu+O2+2H2SO4=2 CuSO4+2H2O,少量 起催化作用,使反應(yīng)按以下兩步完成:
起催化作用,使反應(yīng)按以下兩步完成:
第一步:Cu+2Fe3+=2Fe2++Cu2+
第二步: 。(用離子方程式表示)
②調(diào)節(jié)溶液pH為3~4的目的是 ,調(diào)節(jié)時(shí)加入的試劑可以為 。(選填序號(hào))
a.NaOH溶液 b.CuO粉末 c.Cu2(OH)2CO3 d.氨水
(3)納米TiO2是優(yōu)良的光敏催化劑。工業(yè)上用鈦鐵礦制得粗TiO2;再轉(zhuǎn)化為TiCl4(l);由TiCl4(l)制取納米TiO2的方法之一是將TiCl4氣體導(dǎo)入氫氧火焰中(700~1000℃)進(jìn)行水解。
已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
①寫出TiO2和焦炭、氯氣反應(yīng)生成TiCl4和CO的熱化學(xué)方程式: 。
②寫出上述TiCl4(l)制取納米TiO2的化學(xué)方程式: 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(1)某化學(xué)興趣小組要完成反應(yīng)熱的測(cè)定。實(shí)驗(yàn)桌上備有燒杯(大、小兩個(gè)燒杯)、泡沫塑料、泡沫塑料板、膠頭滴管、環(huán)形玻璃攪拌器、0.50mol· L-1鹽酸、0.50mol· L-1NaOH溶液,實(shí)驗(yàn)尚缺少的玻璃用品是_____________、_______________。
(2)已知2molCO氣體完全燃燒生成CO2 氣體放出566 kJ熱量;1 mol氫氣完全燃燒生成液態(tài)水放出286 kJ熱量;1 molCH4氣體完全燃燒生成CO2氣體和液態(tài)水放出890 kJ熱量。寫出用標(biāo)準(zhǔn)燃燒熱作為反應(yīng)熱的CO燃燒的熱化學(xué)方程式__________________。
若1 molCH4氣體完全燃燒生成CO2固體和液態(tài)水,放出熱量_____890 kJ( 填“>”、 “<”、“=”)。若將a molCH4、CO和H2的混合氣體完全燃燒,生成 CO2氣體和液態(tài)水,且CO2和水的物質(zhì)的量相等時(shí),則放出熱量(Q)的的取值范圍是________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
在化學(xué)反應(yīng)中,只有極少數(shù)能量比平均能量高得多的反應(yīng)物分子發(fā)生碰撞時(shí)才可能發(fā)生化學(xué)反應(yīng),這些分子稱為活化分子,使普通分子變成活化分子所需提供的最低限度的能量叫活化能,其單位通常用kJ/mol表示。請(qǐng)認(rèn)真觀察右圖,然后回答問題。
(l)圖中所示反應(yīng)是______(填“吸熱”或“放熱”)反應(yīng),該反應(yīng)_______(填“需要”或“不需要”)加熱,該反應(yīng)的△H=_______(用含 、
、 的代數(shù)式表示)。
的代數(shù)式表示)。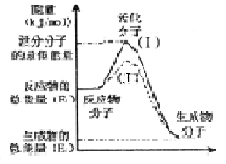
(2)已知熱化學(xué)方程式:H2(g) +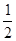 O2(g)═H2O(g);△H=-241.5kJ/mol,該反應(yīng)的活化能為167. 4kJ/mol,則其逆反應(yīng)的活化能為________________。
O2(g)═H2O(g);△H=-241.5kJ/mol,該反應(yīng)的活化能為167. 4kJ/mol,則其逆反應(yīng)的活化能為________________。
(3)對(duì)于同一反應(yīng),圖中虛線(Ⅱ)與實(shí)線(I)相比,活化能大大降低,活化分子的百分?jǐn)?shù)增多,反應(yīng)速率加快,你認(rèn)為最可能的原因是_____________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
紅磷P(s)和Cl2發(fā)生反應(yīng)生成PCl3和PCl5,反應(yīng)過程和能量關(guān)系如圖所示(圖中的△H表示生成1mol產(chǎn)物的數(shù)據(jù))
據(jù)圖回答下列問題
(1)P和Cl2反應(yīng)生成PCl3的熱化學(xué)方程式 ;
(2)PCl5分解生成PCl3和Cl2的熱化學(xué)方程式 ;
上述分解反是一個(gè)可逆反應(yīng),溫度T1時(shí),在密閉容器中加入0.8mol PCl5,反應(yīng)達(dá)到平衡時(shí)還剩余0.6mol PCl5,其分解率α1等于 ;若反應(yīng)溫度由T1升高到T2,平衡時(shí)PCl5分解率α2,α2 α1(填“大于”,“小于”或“等于”);
(3)工業(yè)上制備PCl5通常分兩步進(jìn)行,先將P和Cl2反應(yīng)生成中間產(chǎn)物PCl3,然后降溫,再和Cl2反應(yīng)生成PCl5。原因是 ;
(4)P和Cl2分兩步反應(yīng)生成1mol PCl5的△H3= ;P和Cl2一步反應(yīng)生成1mol PCl5的△H4 △H3 (填“大于”、“小于”或“等于”),原因是 。
查看答案和解析>>
國(guó)際學(xué)校優(yōu)選 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com