
工業上用某礦渣(主要成分為Cu2O,還含有Al2O3、Fe2O3、SiO2)提取銅的操作流程如下:
(固體混合物B經處理后可回收銅)
已知:Cu2O+2H+=Cu+Cu2++H2O。
(1)實驗操作Ⅰ的名稱為_________;在空氣中灼燒固體混合物D時,用到多種硅酸鹽材質的儀器,除玻璃棒、酒精燈、泥三角外,還有_________(填儀器名稱)。
(2)濾液A中鐵元素的存在形式為_______(填離子符號),生成該離子的離子方程式為_____________________。
檢驗濾液A中存在該離子的試劑為 (填試劑名稱)。
(3)常溫下,等pH的NaAlO2和NaOH兩份溶液中,由水電離出的c(OH-)前者為后者的108倍,則兩種溶液的pH=_______。
(4) ①利用電解法進行粗銅精煉時,下列敘述正確的是________(填代號)。
a.電能全部轉化為化學能 b.粗銅接電源正極,發生氧化反應
c.精銅作陰極,電解后電解液中Cu2+濃度減小
d.粗銅精煉時通過的電量與陰極析出銅的量無確定關系
②從濃硫酸、濃硝酸、蒸餾水中選用合適的試劑,測定粗銅樣品中金屬銅的質量分數,涉及的主要步驟:稱取一定質量的樣品→_____________________ _______→過濾、洗滌、干燥→稱量剩余固體銅的質量。(填缺少的操作步驟,不必描述操作過程的細節)
(1)過濾 坩堝
(2)Fe2+ 2Fe3+ + Cu = 2Fe2+ + Cu2+ 硫氰化鉀溶液和新制氯水(寫化學式不給分)
(3)11 (4)①bc ②將濃硫酸用蒸餾水稀釋,將樣品與足量稀硫酸充分反應
解析試題分析:礦渣中的Al2O3、Fe2O3均與鹽酸反應,分別生成AlCl3、FeCl3,Cu2O與鹽酸反應生成Cu和Cu2+,溶液中的Fe3+與Cu反應:2Fe3+ + Cu = 2Fe2+ + Cu2+,SiO2不與鹽酸反應,通過過濾把Cu、SiO2與溶液分離,所以固體混合物B經處理后可回收銅,濾液A中含有Cu2+、Fe2+、Al3+,加入足量的NaOH溶液,濾液C中含有AlO2–,金屬E為Al,固體D為Cu(OH)2和Fe(OH)3的混合物,在空氣中灼燒,F為CuO和Fe2O3的混合物,粗銅為Cu、Al和Fe的混合物,經過電解精煉可得純銅。
(1)分離固體與液體的混合物采用過濾的方法,灼燒固體應放在坩堝中。
(2)由以上分析知,濾液A中鐵元素的存在形式為Fe2+,生成該離子的離子方程式為2Fe3+ + Cu = 2Fe2+ + Cu2+,檢驗Fe2+的試劑為硫氰化鉀溶液和新制氯水。
(3)設pH=a,NaAlO2溶液顯堿性是由AlO2–水解所致,所以水電離出的氫氧根離子濃度為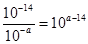 ,NaOH抑制水的電離,水電離出的OH–濃度為10–amol·L–1,
,NaOH抑制水的電離,水電離出的OH–濃度為10–amol·L–1, ,則2a–14 =8,a=11。
,則2a–14 =8,a=11。
(4)①電解過程中,電能除轉化為化學能外,還有部分轉化為熱能,a項錯誤;電解精煉時粗銅應為陽極,與電源的正極相連,發生氧化反應,b項正確;電解時,粗銅中的鐵、鋁也放電,而陰極只有Cu2+得電子,所以溶液中的Cu2+濃度略有降低,c正確;根據電極反應Cu2+ + 2e– = Cu可知,陰極析出銅的物質的量是轉移電子物質的量的二分之一,錯誤。②粗銅為Cu、Al和Fe的混合物,濃硫酸稀釋后,稀硫酸可與混合物中的Al和Fe反應,而銅不反應,通過反應前后固體的質量差可測定銅的質量分數。
考點:考查實驗設計、實驗原理分析、離子檢驗、離子方程式的書寫、pH計算等內容,考查信息處理能力 和綜合分析能力。


 智慧小復習系列答案
智慧小復習系列答案科目:高中化學 來源: 題型:填空題
鈷酸鋰(LiCoO2)鋰離子電池是一種應用廣泛的新型電源,實驗室嘗試利用廢舊鈷酸鋰鋰離子電池回收鋁、鐵、銅、鈷、鋰元素,實驗過程如下:
(1)堿浸泡過程中,鋁被溶解的離子方程式為__________________________
(2)濾液A中加入草酸銨溶液,使Co元素以CoC2O4·2H2O沉淀形式析出。草酸鈷是制備氧化鈷及鈷粉的重要原料。在空氣中CoC2O4·2H2O的熱分解失重數據見下表,請補充完整表中的熱分解方程式。
| 序號 | 溫度范圍/℃ | 熱分解方程式 | 固體失重率 |
| ① | 120~220 | | 19.67% |
| ② | 280~310 | | 56.10% |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
碳酸鋰廣泛應用于陶瓷和醫藥等領域,以β—鋰輝石(主要成分為Li2O·Al2O3·4SiO2)為原料制備Li2CO3的工藝流程如下:
已知:Fe3+、Al3+、Fe2+和Mg2+以氫氧化物形式完全沉淀時,溶液的pH分別為3.2、5.2、9.7和12.4;Li2SO4、LiOH和Li2CO3在303 K下的溶解度分別為34.2 g、12.7 g和1.3 g。
(1)步驟Ⅰ前,β—鋰輝石要粉碎成細顆粒的目的是 。
(2)步驟Ⅰ中,酸浸后得到的酸性溶液中含有Li+、SO42-;另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等雜質,需在攪拌下加入 (填“石灰石”、“氯化鈣”或“稀硫酸”)以調節溶液的pH到6.0~6.5,沉淀部分雜質離子,然后分離得到浸出液。
(3)步驟Ⅱ中,將適量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的雜質金屬離子有 。
(4)步驟Ⅲ中,生成沉淀的離子方程式為 。
(5)從母液中可回收的主要物質是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
多晶硅(硅單質的一種)被稱為“微電子大廈的基石”,制備中副產物以SiCl4為主,它環境污染很大,能遇水強烈水解,放出大量的熱。研究人員利用SiCl4水解生成的鹽酸和鋇礦粉(主要成分為BaCO3,且含有鐵、鎂等離子),制備BaCl2 ? 2H2O,工藝流程如下:
已知: ① 常溫下Fe3+、Mg2+ 完全沉淀的pH分別是3.4、12.4;
② BaCO3的相對分子質量是197; BaCl2 ? 2H2O的相對分子質量是244;
(1)SiCl4發生水解反應的化學方程式__________________________________
(2)高溫下,SiCl4 (g) 用H2還原可制取純度很高的硅,當反應中有1mol電子轉移時吸收
59 kJ熱量,則該反應的熱化學方程式為__________________________________
(3)加鋇礦粉調節pH=7的作用是:
①使BaCO3轉化為BaCl2 ②_______________________________
(4)生成濾渣A的離子方程式________________________________________
(5)BaCl2濾液經__________、_________、過濾、洗滌,再經真空干燥后得到BaCl2 ? 2H2O
(6)10噸含78.8% BaCO3的鋇礦粉理論上最多能生成BaCl2 ? 2H2O___________噸。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鋇鹽行業生產中排出大量的鋇泥[主要含有 、
、 、
、 、
、 等]。某主要生產
等]。某主要生產 、
、 、
、 的化工廠利用鋇泥制取
的化工廠利用鋇泥制取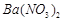 ,其部分工藝流程如下:
,其部分工藝流程如下:
(1)酸溶后溶液中 ,
, 與
與 的反應化學方程式為 。
的反應化學方程式為 。
(2)酸溶時通常控制反應溫度不超過70℃,且不使用濃硝酸,
原因是 、 。
(3)該廠結合本廠實際,選用的X為 (填化學式);中和Ⅰ使溶液中 (填離子符號)的濃度減少(中和Ⅰ引起的溶液體積變化可忽略)。
(4)上述流程中洗滌的目的是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
重鉻酸鉀(K2Cr2O7)為用途極廣的鉻化合物。鉻鐵礦的主要成分可表示為FeO?Cr2O3,還含有SiO2、Al2O3等雜質,以鉻鐵礦為原料制備K2Cr2O7晶體的過程
如下圖所示:
已知:①K2Cr2O7有強氧化性
②NaFeO2遇水強烈水解
③Cr2O72-+ H2O  2CrO42- + 2H+
2CrO42- + 2H+
請回答:
(1)煅燒鉻鐵礦生成Na2CrO4和NaFeO2反應的化學方程式是 。
(2)濾液1的成分除NaOH、Na2CrO4外,還含有(填化學式) ;
生成濾渣1中紅褐色物質的反應離子方程式是 。
(3)由濾液2轉化為Na2Cr2O7溶液應加入的試劑是 。
(4)向Na2Cr2O7溶液中加入K2SO4固體,發生復分解反應而制得K2Cr2O7。生成K2Cr2O7晶體的過程是:加熱濃縮、降溫結晶、過濾、洗滌、干燥。試簡述此法能夠制得K2Cr2O7晶體的原因是: ;
洗滌時應選用 (選填字母)。
| A.蒸餾水 | B.酒精 | C.稀硫酸 | D.飽和K2SO4溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某混合金屬粉末,除Mg外還含有Al、Zn中的一種或兩種,含量都在10%以上。某研究小組設計實驗探究該混合金屬粉末中鋁、鋅元素的存在。
所用試劑:樣品、pH試紙、稀H2SO4、NaOH溶液、稀NH3·H2O。
該小組探究過程如下:
●查閱資料:
| ①鎂、鋁、鋅都是銀白色的金屬 ②鋅(Zn)可以與NaOH溶液反應生成H2 ③Zn(OH)2為白色固體,難溶于水,可溶于強堿及NH3·H2O ④Zn2+易形成絡合物如[Zn(NH3)4]2+,該絡合物遇強酸分解生成Zn2+、NH4+ |

查看答案和解析>>
科目:高中化學 來源: 題型:計算題
某工廠廢液中含有苯酚、乙酸苯酚酌,實驗小組對該廢液進行探究,設計如下方案:
己知熔點:乙酸16.6℃、苯酚43℃。沸點:乙酸118℃、苯酚182℃。
(1)寫出②的反應化學方程式 。
(2)②中分離B的操作名稱是 。
(3)現對物質C的性質進行實驗探究,請你幫助實驗小組按要求完成實驗過程記錄,在答題卡上填寫出實驗操作、預期現象和現象解釋。
限選試劑:蒸餾水、稀HNO3、2moL·L-1 NaOH、0.1 mol?L-1 KSCN、酸性KMnO4溶液、FeCl3溶液、飽和浪水、紫色石蕊試液。
| 實驗操作 | 預期現象 | 現象解釋 |
| 步驟1:取少量C放入a試管,加入少量蒸餾水,振蕩。 | | |
| 步驟:取少量C的稀溶液分裝b、c兩支試管,往b試管 | 產生白色沉淀 | |
| 步驟3:往c試管 | | C與加入的試劑發生顯色反應。 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com