
【題目】在25℃時,將兩個鉑電極插入一定量飽和Na2SO4溶液中進行電解,通電一段時間后,在陽極上放出a mol氣體,同時有w g Na2SO410H2O晶體析出.若溫度不變,此時剩余溶液中溶質的質量分數為( )
A.![]() ×100%
×100%
B.![]() ×100%
×100%
C.![]() ×100%
×100%
D.![]() ×100%
×100%
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】鎳鎘(Ni-Cd)可充電電池在現代生活中有廣泛應用。電解質溶液為KOH溶液,電池反應為:Cd +2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2,下列有關鎳鎘電池的說法正確的是:( )
Cd(OH)2+2Ni(OH)2,下列有關鎳鎘電池的說法正確的是:( )
A. 放電時電池內部OH-向正極移動
B. 放電時正極附近溶液的pH減小
C. 充電時陽極反應為Cd(OH)2+2e -= Cd + 2OH-
D. 充電時與直流電源正極相連的電極上發生Ni(OH)2轉化為NiO(OH)的反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨基甲酸銨(NH2COONH4)是重要的氨化劑,在潮濕的空氣中能轉化為碳酸銨,受熱易分解、易被氧化。實驗小組對氨基甲酸銨的性質進行了如下探究。請回答下列問題:
(1)氨基甲酸銨在潮濕的空氣中轉化為碳酸銨的化學方程式為____________________________。
(2)用下圖裝置探究氨基甲酸銨的分解產物(夾持裝置略去,下同)。

①點燃A處的酒精燈之前,需先打開k,向裝置中通入一段時間的N2,目的為_________________。
②儀器B的名稱為_________________。
③裝置D的作用為________________________________________________________。
④能證明分解產物中有NH3的現象為_________________________________________。
⑤試劑A用于檢驗分解產物中的CO2,該試劑的名稱為_______________________。
(3)已知:CuO高溫能分解為Cu2O和O2。若用上述裝置和下列部分裝置進一步檢驗分解產物中是否有CO,裝置E后應依次連接_________________(按從左到右的連接順序填選項字母)。
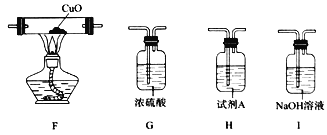
(4)通過實驗得出結論:氨基甲酸銨受熱分解為NH3和CO2。該反應的化學方程式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】足量銅與一定量濃硝酸反應,得到硝酸銅溶液和NO2、NO的混合氣體,這些氣體與1.68 L O2(標準狀況)混合后通入水中,所有氣體完全被水吸收生成硝酸。若向所得硝酸銅溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,則消耗NaOH溶液的體積是( )
A. 60 mL B. 45 mL C. 30 mL D. 15 mL
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知Ka1(H2CO3)>Ka(HClO)>Ka2(H2CO3).現將0.1molL﹣1次氯酸溶液與0.1molL﹣1碳酸鈉溶液等體積混合,在所得混合溶液中各種粒子濃度關系正確的是( )
A.c(Na+)>c(ClO﹣)>c(HCO ![]() )>c(H+)
)>c(H+)
B.c(Na+)>c(HCO ![]() )>c(C1O﹣)>c(OH﹣)
)>c(C1O﹣)>c(OH﹣)
C.c(HClO)+c(C1O﹣)=c(HCO ![]() )+c(H2CO3)
)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO ![]() )+c(ClO﹣)+c(OH﹣)+c(CO
)+c(ClO﹣)+c(OH﹣)+c(CO ![]() )
)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學學習小組設計了如下從海帶灼燒后的海帶灰中提取碘單質的流程:

(1)溶解海帶灰時要加熱煮沸2~3min的目的是_________________,操作a的名稱為 ____________。
(2)向酸化的溶液I中加入H2O2的目的為__________________________________。
(3)已知I2與40%的NaOH溶液反應生成的氧化產物和還原產物的物質的量之比為1:5,寫出對應的化學方程式:________________________________。
(4)最后過濾得到的I2需要進行洗滌和干燥,下列洗滌劑中最應該選用的是_________(填選項字母)。 A.熱水 B.乙醇 C.冷水 D.二硫化碳
(5)用Na2S2O3的標準溶液測定產品的純度,發生反應:I2+2Na2S2O3=Na2S4O6+2NaI。取5.0g產品,配制成100ml溶液。取10.00ml溶液,以淀粉溶液為指示劑,用濃度為0.050mol·L-1Na2S2O3的標準溶液進行滴定,相關數據記錄如下表所示。
編號 | 1 | 2 | 3 |
溶液的體積/mL | 10.00 | 10.00 | 10.00 |
消耗Na2S2O3,標準溶液的體積/mL | 19.95 | 17.10 | 20.05 |
滴定時,達到滴定終點的現象是________________,碘單質在產品中的質量分數是________________(用百分數表示,且保留1位小數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,2L物質的量濃度為0.5molL﹣1KOH溶液含有( )
A.0.5mol的K+
B.0.5mol的H+
C.1.0mol的H+
D.1.0mol的OH﹣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下用惰性電極電解200mLNaCl、CuSO4的混合溶液,所得氣體的體積隨時間變化如下圖所示,根據圖中信息回答下列問題:( 注:氣體體積已換算成標準狀況下的體積,且忽略氣體在水中的溶解和溶液體積的變化.)
(1)曲線(選填“Ⅰ”或“Ⅱ”) 表示陽極產生氣體的變化情況.
(2)NaCl的物質的量濃度為;CuSO4 的物質的量濃度 .
(3)t2時所得溶液的pH為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物A、B均為合成某種抗支氣管哮喘藥物的中間體,A在一定條件下可轉化為B(如下圖所示),下列說法正確的是

A.分子A中所有碳原子均位于同一平面
B.用FeCl3溶液可檢驗物質B中是否混有A
C.物質B既能發生銀鏡反應,又能發生水解反應
D.1mol B最多可與5mol H2發生加成反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com