
已知甲和乙在溶液中的轉(zhuǎn)化關(guān)系如圖所示: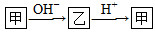 。請(qǐng)回答下列問(wèn)題:
。請(qǐng)回答下列問(wèn)題:
(1)若甲是10電子的陽(yáng)離子,乙是堿性氣體。1 mol乙通入足量強(qiáng)酸溶液中與H+反應(yīng),反應(yīng)過(guò)程中的能量變化如圖。寫(xiě)出乙的一種用途________________。該反應(yīng)的熱化學(xué)方程式為_(kāi)__________________________。
(2)若甲是CO2,用CO2和NH3反應(yīng)可以合成尿素,合成尿素的反應(yīng)分為如下兩步。
第一步:2NH3(l)+CO2(g) H2NCOONH4(l)(氨基甲酸銨) ΔH1
H2NCOONH4(l)(氨基甲酸銨) ΔH1
第二步:H2NCOONH4(l) H2O(l)+H2NCONH2(l)(尿素) ΔH2
H2O(l)+H2NCONH2(l)(尿素) ΔH2
在一體積為0.5 L的密閉容器中投入4 mol氨和1 mol二氧化碳,實(shí)驗(yàn)測(cè)得反應(yīng)中各組分的物質(zhì)的量隨時(shí)間的變化如圖Ⅰ所示。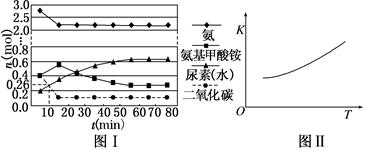
①已知總反應(yīng)的快慢由慢的一步?jīng)Q定,則合成尿素總反應(yīng)的快慢由第________步反應(yīng)決定。
②反應(yīng)進(jìn)行到10 min時(shí)測(cè)得CO2的物質(zhì)的量如圖Ⅰ所示,則前10 min用CO2表示的第一步反應(yīng)的速率為_(kāi)_______。
③第二步反應(yīng)的平衡常數(shù)K隨溫度的變化如圖Ⅱ所示,則ΔH2________0(填“>”、“<”或“=”)。
(1)制氮肥 NH3(g)+H+(aq)===NH4+(aq) ΔH=-(b-c) kJ·mol-1
(2)①二 ②0.148 mol·L-1·min-1 ③>
解析



| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來(lái)源: 題型:填空題
對(duì)含氮物質(zhì)的研究和利用有著極為重要的意義。
(1)N2、O2和H2相互之間可以發(fā)生化合反應(yīng),已知反應(yīng)的熱化學(xué)方程式如下:
N2(g)+O2(g)=2NO(g) 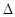 H=+180.5kJ·mol-1;
H=+180.5kJ·mol-1;
2H2(g)+O2(g)=2H2O(g) 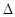 H =-483.6 kJ·mol-1;
H =-483.6 kJ·mol-1;
N2(g)+3H2(g)=2NH3(g) 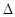 H =-92.4 kJ·mol-1。
H =-92.4 kJ·mol-1。
則氨的催化氧化反應(yīng)的熱化學(xué)方程式為 。
(2)汽車(chē)尾氣凈化的一個(gè)反應(yīng)原理為:2NO(g)+2CO(g) N2(g)+2CO2(g)
N2(g)+2CO2(g) 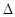 H<0。
H<0。
一定溫度下,將2.8mol NO、2.4mol CO通入固定容積為2L的密閉容器中,反應(yīng)過(guò)程中部分物質(zhì)的物質(zhì)的量變化如圖所示。
①NO的平衡轉(zhuǎn)化率為 ,0~20min平均反應(yīng)速率v(NO)為 。25min時(shí),若保持反應(yīng)溫度不變,再向容器中充入CO、N2各0.8 mol,則化學(xué)平衡將 移動(dòng)(填“向左”、“向右”或“不”)。
②若只改變某一反應(yīng)條件X,反應(yīng)由原平衡I達(dá)到新平衡II,變量Y的變化趨勢(shì)如下圖所示。下列說(shuō)法正確的是 (填字母代號(hào))。
|
 (3)某化學(xué)小組擬設(shè)計(jì)以N2和H2為電極反應(yīng)物,以HCl—NH4Cl為電解質(zhì)溶液制成燃料電池,則該電池的正極反應(yīng)式為 。假設(shè)電解質(zhì)溶液的體積不變,下列說(shuō)法正確的是 (填字母代號(hào))。
(3)某化學(xué)小組擬設(shè)計(jì)以N2和H2為電極反應(yīng)物,以HCl—NH4Cl為電解質(zhì)溶液制成燃料電池,則該電池的正極反應(yīng)式為 。假設(shè)電解質(zhì)溶液的體積不變,下列說(shuō)法正確的是 (填字母代號(hào))。 1023個(gè)電子,則有標(biāo)準(zhǔn)狀況下11.2L電極反應(yīng)物被氧化
1023個(gè)電子,則有標(biāo)準(zhǔn)狀況下11.2L電極反應(yīng)物被氧化查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:填空題
制備鋅印刷電路板是用稀硝酸腐蝕鋅板,產(chǎn)生的廢液稱(chēng)“爛板液”。“爛板液”中含硝酸鋅外,還含有自來(lái)水帶入的Cl—和Fe3+。在實(shí)驗(yàn)室里,用“爛板液”制取ZnSO4·7H2O的過(guò)程如下: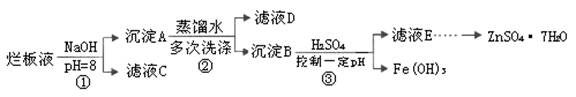
(1)若稀硝酸腐蝕鋅板時(shí)還原產(chǎn)物為N2O,氧化劑與還原劑的物質(zhì)的量之比是 。
(2)若步驟①的pH>12,則Zn(OH)2溶解生成四羥基合鋅酸鈉。寫(xiě)出Zn(OH)2被溶解的離子方程式 。
(3)濾液D中除了含有OH—離子外,還含有的陰離子有 (填離子符號(hào))。
(4)若濾液E的pH=4,c(Zn2+)=2mol·L-1,c(Fe3+)=2.6×l0-9mol·L-1,能求得的溶度積是 (填選項(xiàng))。
A.Ksp[Zn(OH)2] B.Ksp[Zn(OH)2]和Ksp[Fe(OH)3] C.Ksp[Fe(OH)3]
(5)步驟③要控制pH在一定范圍。實(shí)驗(yàn)室用pH試紙測(cè)定溶液pH的方法是: 。
(6)已知:①Fe(OH)3(s) Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1
Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1
②H2O(l)  H+(aq)+OH-(aq) ;ΔH=" b" kJ?mol-1
H+(aq)+OH-(aq) ;ΔH=" b" kJ?mol-1
請(qǐng)寫(xiě)出Fe3+發(fā)生水解反應(yīng)的熱化學(xué)方程式: 。
若①的溶度積常數(shù)為KSP,②的離子積常數(shù)為KW,F(xiàn)e3+發(fā)生水解反應(yīng)的平衡常數(shù):
K= 。(用含KSP、KW的代數(shù)式表示)
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:填空題
2013年初,霧霾天氣多次肆虐我國(guó)中東部地區(qū)。其中,汽車(chē)尾氣和燃煤尾氣是造成空氣污染的原因之一。
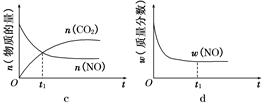
(1)汽車(chē)尾氣凈化的主要原理為:2NO(g)+2CO(g)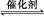 2CO2(g)+N2(g)。在密閉容器中發(fā)生該反應(yīng)時(shí),c(CO2)隨溫度(T)、催化劑的表面積(S)和時(shí)間(t)的變化曲線(xiàn),如圖所示。
2CO2(g)+N2(g)。在密閉容器中發(fā)生該反應(yīng)時(shí),c(CO2)隨溫度(T)、催化劑的表面積(S)和時(shí)間(t)的變化曲線(xiàn),如圖所示。
據(jù)此判斷:
①該反應(yīng)的ΔH 0(填“>”或“<”)。
②在T2溫度下,0~2 s內(nèi)的平均反應(yīng)速率v(N2)= 。
③當(dāng)固體催化劑的質(zhì)量一定時(shí),增大其表面積可提高化學(xué)反應(yīng)速率。若催化劑的表面積S1>S2,在上圖中畫(huà)出c(CO2)在T1、S2條件下達(dá)到平衡過(guò)程中的變化曲線(xiàn)。
④若該反應(yīng)在絕熱、恒容的密閉體系中進(jìn)行,下列示意圖正確且能說(shuō)明反應(yīng)在進(jìn)行到t1時(shí)刻達(dá)到平衡狀態(tài)的是 (填代號(hào))。 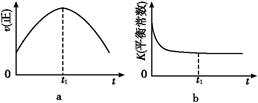
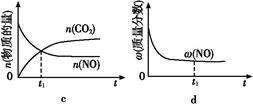
(2)直接排放煤燃燒產(chǎn)生的煙氣會(huì)引起嚴(yán)重的環(huán)境問(wèn)題。
①煤燃燒產(chǎn)生的煙氣含氮的氧化物,用CH4催化還原NOx可以消除氮氧化物的污染。
例如:
CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH1="-867" kJ/mol
N2(g)+CO2(g)+2H2O(g) ΔH1="-867" kJ/mol
2NO2(g) N2O4(g) ΔH2="-56.9" kJ/mol
N2O4(g) ΔH2="-56.9" kJ/mol
寫(xiě)出CH4(g)催化還原N2O4(g)生成N2(g)和H2O(g)的熱化學(xué)方程式: 。
②將燃煤產(chǎn)生的二氧化碳回收利用,可達(dá)到低碳排放的目的。如圖是通過(guò)人工光合作用,以CO2和H2O為原料制備HCOOH和O2的原理示意圖。催化劑b表面發(fā)生的電極反應(yīng)式為 。 
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:填空題
根據(jù)下列條件計(jì)算有關(guān)反應(yīng)的焓變:
(1)已知:Ti(s)+2Cl2(g)=TiCl4(l)ΔH=-804.2 kJ·mol-1
2Na(s)+Cl2(g)=2NaCl(s) ΔH=-882.0 kJ·mol-1
Na(s)=Na(l) ΔH=+2.6 kJ·mol-1
則反應(yīng)TiCl4(l)+4Na(l)=Ti(s)+4NaCl(s)的ΔH=________ kJ·mol-1。
(2)已知下列反應(yīng)數(shù)值:
| 反應(yīng)序號(hào) | 化學(xué)反應(yīng) | 反應(yīng)熱 |
| ① | Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) | ΔH1=-26.7 kJ·mol-1 |
| ② | 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) | ΔH2=-50.8 kJ·mol- |
| ③ | Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) | ΔH3=-36.5 kJ·mol-1 |
| ④ | FeO(s)+CO(g)=Fe(s)+CO2(g) | ΔH4 |
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:填空題
2013年初,霧霾天氣多次肆虐我國(guó)中東部地區(qū)。其中,汽車(chē)尾氣和燃煤尾氣是造成空氣污染的原因之一。
(1)汽車(chē)尾氣凈化的主要原理為2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密閉容器中發(fā)生該反應(yīng)時(shí),c(CO2)隨溫度(T)、催化劑的表面積(S)和時(shí)間(t)的變化曲線(xiàn)如圖所示。
2CO2(g)+N2(g)。在密閉容器中發(fā)生該反應(yīng)時(shí),c(CO2)隨溫度(T)、催化劑的表面積(S)和時(shí)間(t)的變化曲線(xiàn)如圖所示。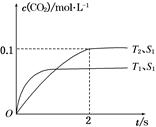
據(jù)此判斷:
①該反應(yīng)的ΔH________0(填“>”或“<”)
②在T2溫度下,0~2 s內(nèi)的平均反應(yīng)速率v(N2)=______________________。
③當(dāng)固體催化劑的質(zhì)量一定時(shí),增大其表面積可提高化學(xué)反應(yīng)速率。若催化劑的表面積S1>S2,在上圖中畫(huà)出c(CO2)在T1、S2條件下達(dá)到平衡過(guò)程中的變化曲線(xiàn)。
④若該反應(yīng)在絕熱、恒容的密閉體系中進(jìn)行,下列示意圖正確且能說(shuō)明反應(yīng)在進(jìn)行到t1時(shí)刻達(dá)到平衡狀態(tài)的是________(填代號(hào))。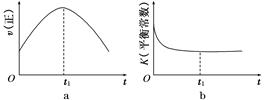
(2)直接排放煤燃燒產(chǎn)生的煙氣會(huì)引起嚴(yán)重的環(huán)境問(wèn)題。
①煤燃燒產(chǎn)生的煙氣含氮的氧化物,用CH4催化還原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH1=-867 kJ/mol
2NO2(g)??N2O4(g) ΔH2=-56.9 kJ/mol
寫(xiě)出CH4(g)催化還原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的熱化學(xué)方程式:________________________________________________________________________。
②將燃煤產(chǎn)生的二氧化碳回收利用,可達(dá)到低碳排放的
目的。如圖是通過(guò)人工光合作用,以CO2和H2O為原料制備HCOOH和O2的原理示意圖。催化劑b表面發(fā)生的電極反應(yīng)式為_(kāi)_________________________。
③常溫下,0.1 mol·L-1的HCOONa溶液pH為10,則HCOOH的電離常數(shù)Ka=________。
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:填空題
硫在地殼中主要以硫化物、硫酸鹽等形式存在,其單質(zhì)和化合物在工農(nóng)業(yè)生產(chǎn)中有著重要的應(yīng)用。
(1)已知:重晶石(BaSO4)高溫煅燒可發(fā)生一系列反應(yīng),其中部分反應(yīng)如下:
BaSO4(s)+4C(s)=BaS(s)+4CO(g) △H=" +" 571.2 kJ?mol—1
BaS(s)= Ba(s)+S(s) △H=" +460" kJ?mol—1
已知:2C(s)+O2(g)=2CO(g) △H=" -221" kJ?mol—1
則:Ba(s)+S(s)+2O2(g)=BaSO4(s) △H= 。
(2)雄黃(As4S4)和雌黃(As2S3)是提取砷的主要礦物原料。已知As2S3和HNO3有如下反應(yīng):
As2S3+10H++ 10NO3-=2H3AsO4+3S+10NO2↑+ 2H2O
當(dāng)反應(yīng)中轉(zhuǎn)移電子的數(shù)目為2mol時(shí),生成H3AsO4的物質(zhì)的量為 。
(3)向等物質(zhì)的量濃度Na2S、NaOH混合溶液中滴加稀鹽酸至過(guò)量。其中主要含硫各物種(H2S、HS—、S2—)的分布分?jǐn)?shù)(平衡時(shí)某物種的濃度占各物種濃度之和的分?jǐn)?shù))與滴加鹽酸體積的關(guān)系如下圖所示(忽略滴加過(guò)程H2S氣體的逸出)。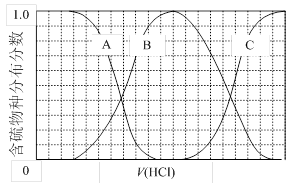
①含硫物種B表示 。在滴加鹽酸過(guò)程中,溶液中c(Na+)與含硫各物種濃度的大小關(guān)系為 (填字母)。
a.c(Na+)= c(H2S)+c(HS—)+2c(S2—)
b.2c(Na+)=c(H2S)+c(HS—)+c(S2—)
c.c(Na+)=3[c(H2S)+c(HS—)+c(S2—)]
②NaHS溶液呈堿性,若向溶液中加入CuSO4溶液,恰好完全反應(yīng),所得溶液呈強(qiáng)酸性,其原因是 (用離子方程式表示)。
(4)硫的有機(jī)物(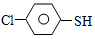 )與甲醛、氯化氫以物質(zhì)的量之比1:1:1反應(yīng),可獲得一種殺蟲(chóng)劑中間體X和H2O。
)與甲醛、氯化氫以物質(zhì)的量之比1:1:1反應(yīng),可獲得一種殺蟲(chóng)劑中間體X和H2O。 及X的核磁共振氫譜如下圖,其中 (填“Ⅰ”或“Ⅱ”)為
及X的核磁共振氫譜如下圖,其中 (填“Ⅰ”或“Ⅱ”)為 的核磁共振氫譜圖。寫(xiě)出X的結(jié)構(gòu)簡(jiǎn)式: 。
的核磁共振氫譜圖。寫(xiě)出X的結(jié)構(gòu)簡(jiǎn)式: 。
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:填空題
氨是氮循環(huán)過(guò)程中的重要物質(zhì),氨的合成是目前普遍使用的人工固氮方法。
(1)根據(jù)圖1提供的信息,寫(xiě)出該反應(yīng)的熱化學(xué)方程式: ,在圖1中曲線(xiàn) (填“a”或“b”)表示加入鐵觸媒的能量變化曲線(xiàn)。 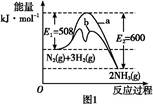
(2)在恒容容器中,下列描述中能說(shuō)明上述反應(yīng)已達(dá)平衡的是 。
A.3v(H2)正=2v(NH3)逆
B.單位時(shí)間內(nèi)生成n mol N2的同時(shí)生成2n mol NH3
C.混合氣體的密度不再改變
D.容器內(nèi)壓強(qiáng)不隨時(shí)間的變化而變化
(3)一定溫度下,向2 L密閉容器中充入1 mol N2和3 mol H2,保持體積不變,0.5 min后達(dá)到平衡,測(cè)得容器中有0.4 mol NH3,則平均反應(yīng)速率v(N2)= ,該溫度下的平衡常數(shù)K= 。若升高溫度,K值變化 (填“增大”、“減小”或“不變”)。
(4)為了尋找合成NH3的溫度和壓強(qiáng)的適宜條件,某同學(xué)設(shè)計(jì)了三組實(shí)驗(yàn),部分實(shí)驗(yàn)條件已經(jīng)填在下面實(shí)驗(yàn)設(shè)計(jì)表中。
| 實(shí)驗(yàn)編號(hào) | T(℃) | n(N2)/n(H2) | p(MPa) |
| ⅰ | 450 | 1/3 | 1 |
| ⅱ | | | 10 |
| ⅲ | 480 | | 10 |
 2NH3(g)的特點(diǎn),在給出的坐標(biāo)圖2中,畫(huà)出其在1 MPa和10 MPa條件下H2的轉(zhuǎn)化率隨溫度變化的趨勢(shì)曲線(xiàn)示意圖,并標(biāo)明各條曲線(xiàn)的壓強(qiáng)。
2NH3(g)的特點(diǎn),在給出的坐標(biāo)圖2中,畫(huà)出其在1 MPa和10 MPa條件下H2的轉(zhuǎn)化率隨溫度變化的趨勢(shì)曲線(xiàn)示意圖,并標(biāo)明各條曲線(xiàn)的壓強(qiáng)。
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:填空題
CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。該反應(yīng)可用于消除氮氧化物的污染。在130 ℃和180 ℃時(shí),分別將0.50 mol CH4和a mol NO2充入1 L的密閉容器中發(fā)生反應(yīng),測(cè)得有關(guān)數(shù)據(jù)如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。該反應(yīng)可用于消除氮氧化物的污染。在130 ℃和180 ℃時(shí),分別將0.50 mol CH4和a mol NO2充入1 L的密閉容器中發(fā)生反應(yīng),測(cè)得有關(guān)數(shù)據(jù)如下表:
| 實(shí)驗(yàn) 編號(hào) | 溫度 | 時(shí)間/min | 0 | 10 | 20 | 40 | 50 |
| 1 | 130 ℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180 ℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | | 0.15 |

 4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1 2N2(g)+CO2(g)+2H2O(g) ΔH2
2N2(g)+CO2(g)+2H2O(g) ΔH2查看答案和解析>>
國(guó)際學(xué)校優(yōu)選 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專(zhuān)區(qū) | 電信詐騙舉報(bào)專(zhuān)區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專(zhuān)區(qū) | 涉企侵權(quán)舉報(bào)專(zhuān)區(qū)
違法和不良信息舉報(bào)電話(huà):027-86699610 舉報(bào)郵箱:58377363@163.com