
人類活動產生的CO2長期積累,威脅到生態環境,其減排問題受到全世界關注。
(1)工業上常用高濃度的K2CO3溶液吸收CO2,得溶液X,再利用電解法使K2CO3溶液再生,其裝置示意圖如下: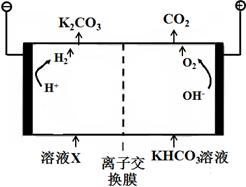
在陽極區發生的反應包括 和H ++ HCO3-=H2O+CO2↑。
簡述CO32-在陰極區再生的原理 。
(2)再生裝置中產生的CO2和H2在一定條件下反應生成甲醇等產物,工業上利用該反應合成甲醇。
已知:25 ℃,101 KPa下:
H2(g)+1/2 O2(g)=H2O(g) Δ H1=" -242" kJ/mol
CH3OH(g)+3/2 O2(g)=CO2 (g)+2 H2O(g) Δ H2=" -676" kJ/mol
寫出CO2和H2生成氣態甲醇等產物的熱化學方程式 。
下面表示合成甲醇的反應的能量變化示意圖,其中正確的是 (填字母序號)。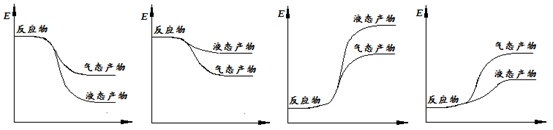
a b c d
(3)微生物燃料電池是一種利用微生物將化學能直接轉化成電能的裝置。已知某種甲醇
微生物燃料電池中,電解質溶液為酸性,示意圖如下: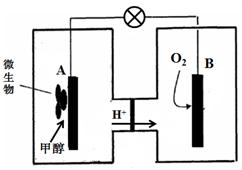
該電池外電路電子的流動方向為 (填寫“從A到B”或“從B到A”)。
工作結束后,B電極室溶液的pH與工作前相比將 (填寫“增大”、“減小”或“不變”,溶液體積變化忽略不計)。
A電極附近甲醇發生的電極反應式為 。
(1)①4OH--4e-=2H2O+O2↑(2分)
②答案1:HCO3 –存在電離平衡:HCO3 – H++CO32- (1分),陰極H+放電濃度減小平衡右移(1分)CO32-再生
H++CO32- (1分),陰極H+放電濃度減小平衡右移(1分)CO32-再生
答案2:陰極H+放電OH-濃度增大(1分),OH-與HCO3 –反應生成CO32-(1分)CO32-再生
(2)①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H="-50" kJ/mol(2分) ② a(2分)
(3)①從A到B(1分) ②不變(1分)
③CH3OH+H2O - 6e-=6H++ CO2↑(2分)
解析試題分析:(1)①陽極上H2O電離出的OH?失電子,電極方程式為:4OH - - 4e-=2H2O+O2↑
②陰極上H+放電發生得電子反應:2H++2e?=H2↑,HCO3?存在電離平衡:HCO3? CO32?+H+,H+濃度減小,使HCO3?電離平衡向右移動,CO32?濃度增大而再生。
CO32?+H+,H+濃度減小,使HCO3?電離平衡向右移動,CO32?濃度增大而再生。
(2)①首先寫出CO2與H2反應生成甲醇的化學方程式,并注明狀態,然后根據蓋斯定律求?H=3?H1—?H2= -50 kJ?mol?1,所以熱化學方程式為:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H="-50" kJ?mol?1。
②該反應為放熱反應,生成物為液態,放出的熱量更多,所以a項圖像正確。
(3) ①甲醇失去電子,為電池的負極,所以該電池外電路電子的流動方向為從A到B。
②B電極上O2得電子消耗H+,同時溶液中的H+移向B電極室,所以B電極室溶液的pH與工作前相比將不變。
③CH3OH失電子,生成CO2和H+,根據化合價變化和元素守恒配平方程式:CH3OH+H2O - 6e-=6H++ CO2↑
考點:本題考查電解原理、原電池原理、方程式的書寫、平衡移動、熱化學方程式的書寫。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:填空題
能源的開發利用與人類社會的可持續發展息息相關。
Ⅰ.已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g) ΔH1=a kJ·mol-1
CO(g)+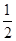 O2(g)=CO2(g) ΔH2=b kJ·mol-1
O2(g)=CO2(g) ΔH2=b kJ·mol-1
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH3=c kJ·mol-1
則C的燃燒熱ΔH=________ kJ·mol-1。
Ⅱ.(1)依據原電池的構成原理,下列化學反應在理論上可以設計成原電池的是________(填序號)。
A.C(s)+CO2(g)=2CO(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2H2O(l)=2H2(g)+O2(g)
D.2CO(g)+O2(g)=2CO2(g)
若以熔融的K2CO3與CO2為反應的環境,依據所選反應設計成一個原電池,請寫出該原電池的負極反應:______________________________________
_______________________________________________________________。
(2)某實驗小組模擬工業合成氨反應N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,開始他們將N2和H2混合氣體20 mol(體積比1∶1)充入5 L合成塔中,反應前壓強為p0,反應過程中壓強用p表示,反應過程中
2NH3(g) ΔH=-92.4 kJ·mol-1,開始他們將N2和H2混合氣體20 mol(體積比1∶1)充入5 L合成塔中,反應前壓強為p0,反應過程中壓強用p表示,反應過程中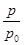 與時間t的關系如圖所示。
與時間t的關系如圖所示。
請回答下列問題: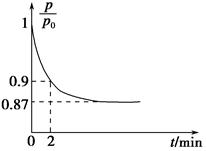
①反應達平衡的標志是(填字母代號)________。
A.壓強保持不變
B.氣體密度保持不變
C.NH3的生成速率是N2的生成速率的2倍
②0~2 min內,以c(N2)變化表示的平均反應速率為________。
③欲提高N2的轉化率,可采取的措施有________。
A.向體系中按體積比1∶1再充入N2和H2
B.分離出NH3
C.升高溫度
D.充入氦氣使壓強增大
E.加入一定量的N2
(3)25 ℃時,BaCO3和BaSO4的溶度積常數分別是8×10-9和1×10-10,某含有BaCO3沉淀的懸濁液中,c(CO32—)=0.2 mol·L-1,如果加入等體積的Na2SO4溶液,若要產生BaSO4沉淀,加入Na2SO4溶液的物質的量濃度最小是________ mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業上常利用CO和H2合成可再生能源甲醇。
(1)已知CO(g)、CH3OH(l)的燃燒熱分別為283.0 kJ·mol-1和726.5 kJ·mol-1,則CH3OH(l)不完全燃燒生成CO(g)和H2O(l)的熱化學方程式為 。
(2)合成甲醇的方程式為CO(g)+2H2(g) CH3OH(g) ΔH <0。
CH3OH(g) ΔH <0。
在230 ℃?270 ℃最為有利。為研究合成氣最合適的起始組成比n(H2):n(CO),分別在230 ℃、250 ℃和270 ℃進行實驗,結果如下左圖所示。其中270 ℃的實驗結果所對應的曲線是_____(填字母);當曲線X、Y、Z對應的投料比達到相同的CO平衡轉化率時,對應的反應溫度與投較比的關系是 。
(3)當投料比為1∶1,溫度為230 ℃,平衡混合氣體中,CH3OH的物質的量分數為 (保留1位小數);平衡時CO的轉化率 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
對大氣污染物SO2、NOx進行研究具有重要環保意義。請回答下列問題:
(1)為減少SO2的排放,常采取的措施是將煤轉化為清潔氣體燃料。
已知:H2(g)+ O2(g)=H2 O(g) △H=-241.8kJ·mol-1
O2(g)=H2 O(g) △H=-241.8kJ·mol-1
C(s)+ O2(g)=CO(g) △H=-110.5kJ·mol-1
O2(g)=CO(g) △H=-110.5kJ·mol-1
寫出焦炭與水蒸氣反應的熱化學方程式: 。
(2)已知汽缸中生成NO的反應為:N2(g)+O2(g) 2NO(g) △H
2NO(g) △H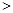 0,若1.0 mol空氣含0.80 mol N2和0.20 mol O2,1300oC時在1.0 L密閉容器內經過5s反應達到平衡,測得NO為8.0×10-4 mol。
0,若1.0 mol空氣含0.80 mol N2和0.20 mol O2,1300oC時在1.0 L密閉容器內經過5s反應達到平衡,測得NO為8.0×10-4 mol。
①5s內該反應的平均速率ν(NO) = (保留2位有效數字);在1300oC 時,該反應的平
衡常數表達式K= 。
②汽車啟動后,汽缸溫度越高,單位時間內NO排放量越大,原因是 。
(3)汽車尾氣中NO和CO的轉化。當催化劑質量一定時,增大催化劑固體的表面積可提高化學反應速率。右圖表示在其他條件不變時,反應2NO(g)+2CO(g) 2CO2(g)+N2(g) 中,NO的濃度
2CO2(g)+N2(g) 中,NO的濃度
c(NO)隨溫度(T)、催化劑表面積(S)和時間(t)的變化曲線。
①該反應的△H 0 (填“>”或“<”)。
②若催化劑的表面積S1>S2,在右圖中畫出c(NO) 在T1、S2條件下達到平衡過程中的變化曲線(并作相應標注)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氨在國民經濟中占有重要地位。
(1)工業合成氨時,合成塔中每產生1 mol NH3,放出46.1 kJ的熱量。
① 工業合成氨的熱化學方程式是 。
② 已知:
N2 (g)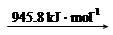 2N (g)
2N (g)
H2 (g)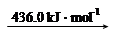 2H (g)
2H (g)
則斷開1 mol N-H鍵所需的能量是_______kJ。
(2)下表是當反應器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下,反應達到平衡時,混合物中NH3的物質的量分數隨壓強的變化曲線。
① 曲線a對應的溫度是 。
② 關于工業合成氨的反應,下列敘述正確的是 (填字母)。
A. 及時分離出NH3可以提高H2的平衡轉化率
B. 加催化劑能加快反應速率且提高H2的平衡轉化率
C. 上圖中M、N、Q點平衡常數K的大小關系是K(M)=" K(Q)" >K(N)
③ M點對應的H2轉化率是 。 (3)氨是一種潛在的清潔能源,可用作堿性燃料電池的燃料。電池的總反應為:
(3)氨是一種潛在的清潔能源,可用作堿性燃料電池的燃料。電池的總反應為:
4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g)。
則該燃料電池的負極反應式是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
I.已知:反應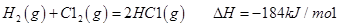
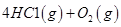
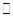
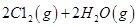

請回答: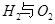 反應生成氣態水的熱化學方程式__________________________
反應生成氣態水的熱化學方程式__________________________
II.實施以減少能源浪費和降低廢氣排放為基本內容的節能減排政策,是應對全球氣候問題、建設資源節約型、環境友好型社會的必然選擇。化工業的發展必須符合國家節能減排的總體要求。試運用所學知識,解決下列問題:
(1)已知某反應的平衡表達式為: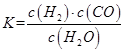
它所對應的化學方程式為:_________________________________________________
(2)已知在400℃時,反應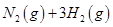
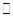
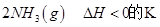 =0.5,則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應
=0.5,則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應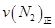 ____________
____________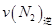 (填:>、<、=、不能確定);
(填:>、<、=、不能確定);
欲使得該反應的化學反應速率加快,同時使平衡時NH3的體積分數增加,
可采取的正確措施是____________(填序號)
A.加催化劑 B.升高溫度 C.縮小體積增大壓強 D.使氨氣液化移走
(3)在一定體積的密閉容器中,進行如下化學反應:
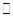
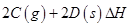 ,其化學平衡常數K與溫度T的關系如下表:
,其化學平衡常數K與溫度T的關系如下表:
請完成下列問題:
①判斷該反應的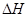 ___________0(填“>”或“<”)
___________0(填“>”或“<”)
②在一定條件下,能判斷該反應一定達化學平衡狀態的是___________(填序號)。
A. B.容器內壓強保持不變
B.容器內壓強保持不變
C.A和B的轉化率相等 D.混合氣體的密度保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)請回答下列問題:
①已知:①CO(g) + 1/2O2(g) = CO2(g) △H= -283.0kJ·mol-1
②CH3OH(l) + 3/2O2(g) = CO2(g)+2H2O(l) △H= -726.5kJ·mol-1
請寫出甲醇不完全燃燒生成一氧化碳和液態水的熱化學方程式:____________________________________________________________________;
②已知拆開1molH-H鍵、1molCl-Cl鍵、1molH—Cl鍵分別需要的能量是436kJ、243kJ、432kJ,則反應則反應:H2(g)+ Cl2(g)=2HCl (g) 的△H= 。
(2)已知25℃、101 kPa下,稀的強酸與稀的強堿溶液反應的中和熱為 -57.3 kJ/mol。
①則表示稀硫酸與稀燒堿溶液中和反應的熱化學方程式為: 。
②測定中和熱實驗時所需的玻璃儀器有燒杯、量筒、 、 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
由于溫室效應和資源短缺等問題,如何降低大氣中的CO2含量并加以開發利用,引起了各國的普遍重視。目前工業上有一種方法是用CO2生產燃料甲醇。一定條件下發生反應:
CO2(g)+3H2(g) CH3OH(g)+H2O(g),圖1表示該反應過程中能量(單位為kJ·mol—1)的變化。
CH3OH(g)+H2O(g),圖1表示該反應過程中能量(單位為kJ·mol—1)的變化。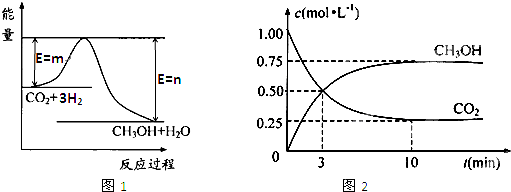
(1)寫出該反應的熱化學方程式 。
(2)關于該反應的下列說法中,正確的是 。
A.△H>0,△S>0 B.△H>0,△S<0 C.△H<0,△S<0 D.△H<0,△S>0
(3)該反應的平衡常數K的表達式為: 。
(4)溫度降低,平衡常數K (填“增大”、 “不變”或“減小”)。
(5)為探究反應原理,現進行如下實驗:在體積為1 L的密閉容器中,充入1 molCO2和3 molH2,測得CO2和CH3OH(g)的濃度隨時間變化如圖2所示。從反應開始到平衡,用氫氣濃度變化表示的平均反應速率v (H2)= 。
(6)下列措施中能使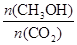 增大的有 。
增大的有 。
A.升高溫度
B.加入催化劑
C.將H2O(g)從體系中分離
D.體積不變,充入He(g)使體系總壓強增大
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知H2(g)和CO(g)的燃燒熱△H分別為-285.8kJ·mol-1、-283.0kJ·mol。
則一氧化碳與液態水反應,生成二氧化碳和氫氣的熱化學方程式為
________________________________________________________;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com