
“低碳循環”引起各國的高度重視,而如何降低大氣中CO2的含量及有效地開發利用CO2,引起了全世界的普遍重視。所以“低碳經濟”正成為科學家研究的主要課題。
(1)用電弧法合成的儲氫納米碳管常伴有大量的碳納米顆粒(雜質),這種顆粒可用如下氧化法提純,請完成該反應的化學方程式,并在方框內填上系數。
□C+□KMnO4+□H2SO4 =□CO2↑+□MnSO4 +□K2SO4+□
(2)將不同量的CO(g)和H2O(g)分別通入到體積為2L的恒容密閉容器中,進行反應CO(g)+H2O(g) CO2(g)+H2(g),得到如下二組數據:
CO2(g)+H2(g),得到如下二組數據:
| 實驗組 | 溫度℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
(16分)
(1)5 C+4KMnO4 +6 H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O(3分,物質1分,配平2分)
(2)①0.13mol/(L·min) (2分) ②0.17(2分); 放熱(2分)
(3)2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g) ΔH=—709.6kJ/mol或CH3OH(l)+O2(g)= CO(g)+2H2O(g)ΔH=—354.8kJ/mol(3分)
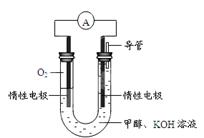
(4)①O2 + 4e-+ 2 H2O = 4OH-(2分) ②負(2分)
解析試題分析:(1)觀察化學方程式,先找變價元素,再根據化合價變化,用最小公倍數法先配氧化劑和還原劑的系數,最后用觀察法配平各物質的系數;碳元素由0價升為+4價,錳元素由+7價降為+2價,二者升降數分別為4、5,則最小公倍數為20,所以該反應為5C+4KMnO4 +6H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O;(2)①讀表中信息,先由定義式求v(CO),再由系數比求v(CO2),即v(CO)=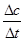 =
=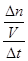 =
=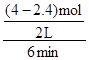 = 0.13mol/(L·min)(保留兩位有效數字),由于
= 0.13mol/(L·min)(保留兩位有效數字),由于 =
= ,則v(CO2)=v(CO)=0.13mol/(L·min);②表中實驗2有關組分的起始物質的量、平衡物質的量已知,容器體積為2L,由于c=n/V,則:
,則v(CO2)=v(CO)=0.13mol/(L·min);②表中實驗2有關組分的起始物質的量、平衡物質的量已知,容器體積為2L,由于c=n/V,則:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始濃度(mol/L) 1 0.5 0 0
變化濃度(mol/L) 0.2 0.2 0.2 0.2
平衡濃度(mol/L) 0.8 0.3 0.2 0.2
K=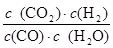 =
=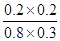 =0.17
=0.17
若用表中實驗1有關組分的起始物質的量、平衡物質的量已知,容器體積為2L,由于c=n/V,則:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始濃度(mol/L) 2 1 0 0
變化濃度(mol/L) 0.8 0.8 0.8 0.8
平衡濃度(mol/L) 1.2 0.2 0.8 0.8
K`=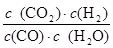 =
=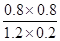 =2.67
=2.67
650℃→900℃,升高溫度,平衡向吸熱反應方向移動;平衡常數由2.67減少為0.17,說明平衡向逆反應方向移動,則逆反應是吸熱反應,所以正反應是放熱反應;
(3)觀察3個熱化學方程式,發現①—②可以約去2CO2(g),根據蓋斯定律,則2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g) ΔH=—709.6kJ/mol,若系數減半,則CH3OH(l)+O2(g)=CO(g)+2H2O(g) ΔH=—354.8kJ/mol;(4)①甲烷燃料電池的正極反應物是氧氣,由于KOH溶液顯堿性,根據電子、電荷、原子守恒原理,則正極反應式為O2+4e-+ H2O=4OH-;②電子帶負電,電極材料本身不帶電,負極流出電子帶正電,因此溶液中帶負電的氫氧根離子移向負極;而正極流入電子帶負電,因此溶液中帶正電的陽離子移向正極。
考點:考查化學反應原理,涉及氧化還原反應反應方程式的配平、平均反應速率的計算、化學平衡常數的計算與比較、溫度對平衡移動的影響規律的應用、放熱反應和吸熱反應、蓋斯定律、燃料電池的正極反應式、離子定向移動規律的應用等。


科目:高中化學 來源: 題型:問答題
[15分]甲烷自熱重整是先進的制氫方法,包含甲烷氧化和蒸汽重整。向反應系統同時通入甲烷、氧氣和水蒸氣,發生的主要化學反應有:
| 反應過程 | 化學方程式 | 焓變△H (kJ/mol) | 活化能Ea (kJ/mol) |
| 甲烷氧化 | CH4(g)+2O2(g) CO2(g)+2H2O(g) CO2(g)+2H2O(g) | -802.6 | 125.6 |
CH4(g)+O2(g) CO2(g)+2H2(g) CO2(g)+2H2(g) | -322.0 | 172.5 | |
| 蒸汽重整 | CH4(g)+H2O(g) CO(g)+3H2(g) CO(g)+3H2(g) | 206.2 | 240.1 |
CH4(g)+2H2O(g) CO2(g)+4H2(g) CO2(g)+4H2(g) | 165.0 | 243.9 |
 CO2(g)+H2(g)的△H= kJ/mol。
CO2(g)+H2(g)的△H= kJ/mol。 CO(g)+3H2(g)的KP= ;
CO(g)+3H2(g)的KP= ;
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
在2L容器中3種物質間進行反應,X、Y、Z的物質的量隨時間的變化曲線如圖。反應在t時到達平衡,依圖所示:
①該反應的化學方程式是 。
②反應起始至t,Y的平均反應速率是 。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
(1)將不同量的CO(g)和H2O(g)分別通入體積2L的恒容密閉容器中,進行反應CO(g)+H2O(g) CO2(g)+H2(g),得到如下兩組數據:
CO2(g)+H2(g),得到如下兩組數據:
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |

查看答案和解析>>
科目:高中化學 來源: 題型:計算題
已知:將KI、鹽酸、試劑X和淀粉四種溶液混合,無反應發生。若再加入雙氧水,將發生反應:H2O2+2H++2I—→2H2O+I2,且生成的I2立即與試劑X反應而被消耗。一段時間后,試劑X將被反應生成的I2完全消耗。由于溶液中的I—繼續被H2O2氧化,生成的I2與淀粉作用,溶液立即變藍。因此,根據試劑X的量、滴入雙氧水至溶液變藍所需的時間,即可推算反應H2O2+2H++2I—→2H2O+I2的反應速率。
下表為某同學依據上述原理設計的實驗及實驗記錄(各實驗均在室溫條件下進行):
| 編號 | 往燒杯中加入的試劑及其用量(mL) | 催化劑 | 開始變藍時間(min) | ||||
| 0.1 mol·Lˉ1 KI溶液 | H2O | 0.01 mol·Lˉ1 X溶液 | 0.1 mol·Lˉ1 雙氧水 | 1 mol·Lˉ1 稀鹽酸 | |||
| 1 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 無 | 1.4 |
| 2 | 20.0 | m | 10.0 | 10.0 | n | 無 | 2.8 |
| 3 | 10.0 | 20.0 | 10.0 | 20.0 | 20.0 | 無 | 2.8 |
| 4 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 5滴Fe2(SO4)3 | 0.6 |
 2AlI3(s)。含I—傳導有機晶體合成物作為電解質,該電池負極的電極反應為:______________________________,充電時Al連接電源的___________極。
2AlI3(s)。含I—傳導有機晶體合成物作為電解質,該電池負極的電極反應為:______________________________,充電時Al連接電源的___________極。查看答案和解析>>
科目:高中化學 來源: 題型:計算題
(1)N2(g)+3H2(g) 2NH3(g) △H=-94.4kJ·mol-1。恒容時,體系中各物質濃度隨時間變化的曲線如圖示。
2NH3(g) △H=-94.4kJ·mol-1。恒容時,體系中各物質濃度隨時間變化的曲線如圖示。
①在1L容器中發生反應,前20min內,v(NH3)= ,放出的熱量為 ;
②25min時采取的措施是 ;
③時段III條件下,反應的平衡常數表達式為 (用具體數據表示)。
(2)電廠煙氣脫氮的主反應①:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) △H<0,副反應②:2NH3(g)+8NO(g)
5N2(g)+6H2O(g) △H<0,副反應②:2NH3(g)+8NO(g) 5N2O(g)+3H2O(g) △H>0。平衡混合氣中N2與N2O含量與溫度的關系如右圖。請回答:在400K~600K時,平衡混合氣中N2含量隨溫度的變化規律是 ,導致這種規律的原因是 (任答合理的一條原因)。
5N2O(g)+3H2O(g) △H>0。平衡混合氣中N2與N2O含量與溫度的關系如右圖。請回答:在400K~600K時,平衡混合氣中N2含量隨溫度的變化規律是 ,導致這種規律的原因是 (任答合理的一條原因)。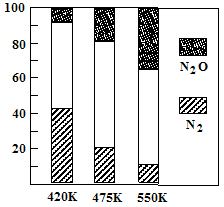
(3)直接供氨式燃料電池是以NaOH溶液為電解質的。電池反應為:4NH3+3O2=2N2+6H2O,則負極電極反應式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
控制變量法是研究化學變化規律的重要思想方法。請仔細觀察下表中50ml稀鹽酸和1g碳酸鈣反應的實驗數據:
| 實驗 序號 | 碳酸鈣狀態 | c(HCl)/mol·L-1 | 溶液溫度/oC | 碳酸鈣消失時間/s | |
| 反應前 | 反應后 | ||||
| 1 | 粒狀 | 0.5 | 20 | 39 | 400 |
| 2 | 粉末 | 0.5 | 20 | 40 | 60 |
| 3 | 粒狀 | 0.6 | 20 | 41 | 280 |
| 4 | 粒狀 | 0.8 | 20 | 40 | 200 |
| 5 | 粉末 | 0.8 | 20 | 40 | 30 |
| 6 | 粒狀 | 1.0 | 20 | 40 | 120 |
| 7 | 粒狀 | 1.0 | 30 | 50 | 40 |
| 8 | 粒狀 | 1.2 | 20 | 40 | 90 |
| 9 | 粒狀 | 1.2 | 25 | 45 | 40 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
草酸(H2C2O4)溶液與酸性KMnO4溶液反應時,溶液褪色總是先慢后快。某學習小組結合化學反應原理提出猜想與假設,并設計了一系列實驗進行探究。
實驗Ⅰ:在2支試管中分別加入5 mL等濃度的H2C2O4溶液,在其中一支試管中先加入少量MnSO4固體再各加入5滴0.1 mol·L-1 KMnO4溶液。記錄溶液褪色時間,如表1:
| 試 管 | 未加MnSO4的試管 | 加有MnSO4的試管 |
| 褪色時間 | 30 s | 2 s |
| 試 管 | 未滴加稀硫酸的試管 | 滴加了稀硫酸的試管 |
| 褪色時間 | 100 s | 90 s |
| 試 管 | 滴入10滴稀硫酸的試管 | 加入1 mL稀硫酸的試管 | 加入2 mL稀硫酸的試管 |
| 褪色時間 | 70 s | 100 s | 120 s |

查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下,Na2CO3溶液中存在平衡:CO32-+H2O HCO3-+OH-,下列有關該溶液的說法正確的是
HCO3-+OH-,下列有關該溶液的說法正確的是
| A.離子濃度:c(Na+)>c(CO32-)>c(OH-)>c(H+) | B.升高溫度,平衡向右移動 |
| C.滴入CaCl2濃溶液,溶液的pH增大 | D.加入NaOH固體,溶液的pH減小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com