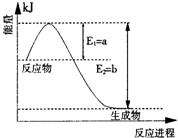
運(yùn)用化學(xué)反應(yīng)原理研究氮、硫、氯、碘等單質(zhì)及其化合物的反應(yīng)有重要意義.
Ⅰ.硫酸生產(chǎn)中,SO
2催化氧化生成SO
3:2SO
2(g)+O
2(g)?2SO
3(g),混合體系中SO
3的百分含量和溫度的關(guān)系如圖1所示(曲線上任何一點(diǎn)都表示平衡狀態(tài)).
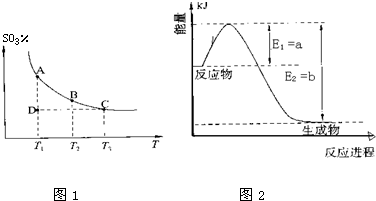
根據(jù)圖示回答下列問題:
①2SO
2(g)+O
2(g)?2SO
3(g)的△H
<
<
0.若溫度為T
1、T
2,反應(yīng)的平衡常數(shù)分別為K
1、K
2,則K
1>
>
K
2;若反應(yīng)進(jìn)行到狀態(tài)D時(shí),v
正>
>
v
逆(填“>”、“<”或“=”).
②若在恒溫、恒容條件下向上述平衡體系中通He,V
正不變
不變
(填“增大”、“減小”或“不變”);平衡
不
不
移動(dòng)(填“向左”、“向右”或“不”).
③若在恒溫、恒壓條件下向上述平衡體系中通入氦氣,V
正減小
減小
,V
逆減小
減小
;平衡
向左
向左
移動(dòng).
Ⅱ.氮是地球上含量豐富的一種元素,氮及其化合物在工農(nóng)業(yè)生產(chǎn)、生活中有著重要作用.
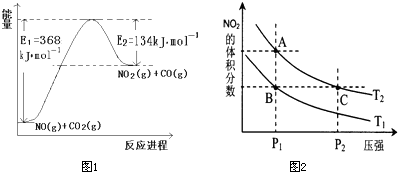
①如圖2是一定的溫度和壓強(qiáng)下是N
2和H
2反應(yīng)生成1molNH
3過程中能量變化示意圖,請(qǐng)寫出工業(yè)合成氨的熱化學(xué)反應(yīng)方程式:
N2(g)+3H2(g)═2NH3(g)△H=-2(b-a)kJ?mol-1
N2(g)+3H2(g)═2NH3(g)△H=-2(b-a)kJ?mol-1
(△H的數(shù)值用含字母a、b的代數(shù)式表示).
②工業(yè)合成氨的反應(yīng)為N
2(g)+3H
2(g)
2NH
3(g).在一定溫度下,將一定量的N
2和H
2通入到體積為1L的密閉容器中達(dá)到平衡后.改變下列條件,能使平衡向正反應(yīng)方向移動(dòng)且平衡常數(shù)不變的是
AB
AB
.
A、增大壓強(qiáng) B、增大反應(yīng)物的濃度 C、使用催化劑 D、降低溫度
③工業(yè)合成氨的反應(yīng)為N
2(g)+3H
2(g)
2NH
3(g).設(shè)在容積為2.0L的密閉容器中充入0.60mol N
2(g)和1.60mol H
2(g).反應(yīng)在一定條件下達(dá)到平衡時(shí),NH
3的體積分?jǐn)?shù)為
.計(jì)算:該條件下N
2(g)+3H
2(g)
2NH
3(g)的平衡常數(shù)為
200
200
;N
2的平衡轉(zhuǎn)化率為
66.7%
66.7%
.
④已知化學(xué)反應(yīng):N
2(g)+3H
2(g)?2NH
3(g);其化學(xué)平衡常數(shù)K與溫度T的關(guān)系如下表:
| T/℃ |
200 |
300 |
400 |
| K |
K1 |
K2 |
0.5 |
400℃時(shí),在2L的密閉容器中2NH
3(g)?N
2(g)+3H
2(g) 的化學(xué)平衡常數(shù)K的值為
2
2
.當(dāng)測(cè)得NH
3和N
2、H
2的物質(zhì)的量分別為12mol和8mol、4mol時(shí),則該反應(yīng)的v
正(N
2)
大于
大于
v
逆(N
2)(填“大于”、“小于”或“等于”)

 氮是地球上含量豐富的元素,氮及其化合物的研究在生產(chǎn)、生活中有著重要意義.
氮是地球上含量豐富的元素,氮及其化合物的研究在生產(chǎn)、生活中有著重要意義.

 心算口算巧算一課一練系列答案
心算口算巧算一課一練系列答案 應(yīng)用題作業(yè)本系列答案
應(yīng)用題作業(yè)本系列答案