
 2CO(g) ��H1��
2CO(g) ��H1�� H2(g)+CO2(g) ��H2����C(s)+H2O(g)
H2(g)+CO2(g) ��H2����C(s)+H2O(g) CO(g)+H2(g) ��H3��
CO(g)+H2(g) ��H3�� 4CO(g)��4H2O(g) ��H=��1038kJ/mol�����I(y��)��Ҫ�x����m�Ĵ������քe��(du��)X��Y��Z���N�����M(j��n)������(sh��)�(y��n)�������l����ͬ����
4CO(g)��4H2O(g) ��H=��1038kJ/mol�����I(y��)��Ҫ�x����m�Ĵ������քe��(du��)X��Y��Z���N�����M(j��n)������(sh��)�(y��n)�������l����ͬ���� CH3OH(g) ��H=��90.8kJ��mol��1��T���´˷���(y��ng)��ƽ�ⳣ��(sh��)��160��
CH3OH(g) ��H=��90.8kJ��mol��1��T���´˷���(y��ng)��ƽ�ⳣ��(sh��)��160��| ���|(zh��) | H2 | CO | CH3OH |
| ���/��mol��L��1�� | 0.20 | 0.10 | 0.40 |
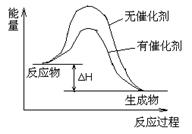


 ͨ�njW(xu��)��Ĭ������ϵ�д�
ͨ�njW(xu��)��Ĭ������ϵ�д� ���ƽ��o����(y��u)��(y��u)�x����ĩ�_��100��ϵ�д�
���ƽ��o����(y��u)��(y��u)�x����ĩ�_��100��ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}
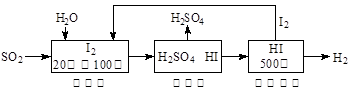
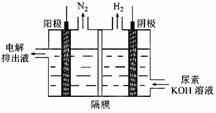
 Ni(OH)2��M
Ni(OH)2��M�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ��Ɣ��}
 X��g������H����dJ��mol��1��d��0��X��A��B��C���NԪ�ؽM�ɵ�һ�N���������ʼͶ���c�������_(d��)��ƽ��r(sh��)�����P(gu��n)��(sh��)��(j��)���£�
X��g������H����dJ��mol��1��d��0��X��A��B��C���NԪ�ؽM�ɵ�һ�N���������ʼͶ���c�������_(d��)��ƽ��r(sh��)�����P(gu��n)��(sh��)��(j��)���£�| ��(sh��)�(y��n) | �� | �� | �� |
| ��ʼͶ�� | 2 molA2��1 molBC | 1 molX | 4 molA2��2 molBC |
| ƽ��r(sh��)n��X�� | 0.5mol | n2 | n3 |
| ����(y��ng)������׃�� | �ų�Q1kJ | ����Q2kJ | �ų�Q3kJ |
| �wϵ�ĉ���(qi��ng) | P1 | P2 | P3 |
| ����(y��ng)����D(zhu��n)���� | ��1 | ��2 | ��3 |

�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�Ӌ(j��)���}
 2NH3(g) ��H<0��ij��(sh��)�(y��n)��3.0 mol N2(g)��4. 0 mol H2(g)�����ݷe��10L�����]�����У��ڜض�T1�·���(y��ng)���y(c��)��H2�����|(zh��)�����S����(y��ng)�r(sh��)�g��׃�����D��ʾ��
2NH3(g) ��H<0��ij��(sh��)�(y��n)��3.0 mol N2(g)��4. 0 mol H2(g)�����ݷe��10L�����]�����У��ڜض�T1�·���(y��ng)���y(c��)��H2�����|(zh��)�����S����(y��ng)�r(sh��)�g��׃�����D��ʾ��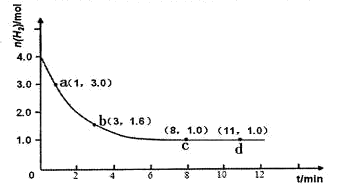

 CH3COO[Cu(NH3)3]?CO ��H<0���������CO�����ʵ�����һ�(xi��ng)��ʩ�� ��
CH3COO[Cu(NH3)3]?CO ��H<0���������CO�����ʵ�����һ�(xi��ng)��ʩ�� ���鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�Ӌ(j��)���}
 Fe3O4(s)+4H2(g) ��H=akJ/mol ��I��
Fe3O4(s)+4H2(g) ��H=akJ/mol ��I�� 6FeO(s)+O2(g) ��H=bkJ/mol ��II��
6FeO(s)+O2(g) ��H=bkJ/mol ��II��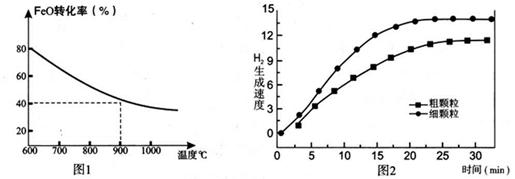
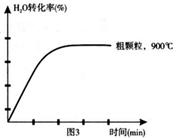
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
| A���Ҝ��£�pH=5.6��NaHSO3��Һ��c( SO32-)-c( H2SO3)= 10-5.6-10-8.4 |
| B��ͬ��ͬ���£�����(y��ng)H2(g)��Cl2(g)��2HCl(g)�ڹ��պ��c(di��n)ȼ�l���µĦ�H��ͬ |
| C�����ᷴ��(y��ng)ֻ���ڼӟ�l���²��ܰl(f��)������ˮ���ӟ��x |
| D���^���İ�ˮ���}�ᷴ��(y��ng)������Һ�����ܞ����ԣ������ܞ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
| A����A2��B2�Ŀ�����֮�ʹ������ɵ�2AB�Ŀ��������t����(y��ng)�ş� |
| B����A2��B2�Ŀ�����֮��С�����ɵ�2AB�Ŀ��������t����(y��ng)�ş� |
| C����ԓ����(y��ng)��şᷴ��(y��ng)���tQ1��Q2 < Q3 |
| D����ԓ����(y��ng)�����ᷴ��(y��ng)���tQ1��Q2 < Q3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
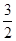 O2(g)=SO2(g)+H2O(g) ��H1
O2(g)=SO2(g)+H2O(g) ��H1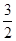 S2(g)+2H2O(g) ��H2
S2(g)+2H2O(g) ��H2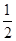 O2(g)=S(g)+H2O(g) ��H3
O2(g)=S(g)+H2O(g) ��H3| A����H4=2/3����H1+��H2-3��H3�� |
| B����H4=2/3��3��H3-��H1-��H2�� |
| C����H4=3/2����H1+��H2-3��H3�� |
| D����H4=3/2����H1-��H2-3��H3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
| A��431 kJ��mol��1 | B��945.6 kJ��mol��1 |
| C��649 kJ��mol��1 | D��896 kJ��mol��1 |
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com