
| 弱酸化學式 | HSCN | CH3COOH | HCN | H2CO3 |
| 電離平衡常數 | 1.3×10 -1 | 1.7×10 -5 | 6.2×10 -10 | K1=4.3×10-7 K2=5.6×10-11 |

分析 (1)依據碳酸的電離平衡常數書寫;
(2)酸性溶液的pH<7、中性溶液的pH=7、堿性溶液的pH>7,且酸性越強,溶液的pH越小,堿性越強,溶液的pH越大;先根據溶液酸堿性對各物質進行分類,然后根據電解質的電離,鹽的水解程度大小判斷溶液中氫離子、氫氧根離子濃度,再判斷溶液pH大小;
(3)CH3COOH溶液加水稀釋過程,促進電離,c(H+)減小,c(OH-)增大,Kw不變;
(4)由生成二氧化碳的曲線斜率可知HSCN反應較快,則可知HSCN中中c(H+)較大,說明HSCN酸性較強,再利用鹽類水解的規律來分析離子濃度的關系;
(5)根據pH=-lgc(H+)計算出氫離子濃度,再根據Kw計算氫氧根濃度;由圖可知,稀釋相同的倍數,HX的pH變化程度大,則酸性HX強,電離平衡常數大;
(6)25℃時,混合液pH=6,c(H+)=1.0×10-6mol/L,則由Kw可知,c(OH-)=1.0×10-8mol/L,由電荷守恒可知,c(CH3COO-)-c(Na+)=c(H+)-c(OH-),根據緩沖溶液中的緩沖公式來計算$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$;
(7)次氯酸酸性大于HCO3-,小于碳酸,少量CO2通入次氯酸鈉溶液中反應生成碳酸氫鈉和次氯酸.
解答 解:(1)碳酸的第一級電離平衡常數表達式:K1=$\frac{[HC{{O}_{3}}^{-}]•[{H}^{+}]}{[{H}_{2}C{O}_{3}]}$;
故答案為:$\frac{[HC{{O}_{3}}^{-}]•[{H}^{+}]}{[{H}_{2}C{O}_{3}]}$;
(2)等物質的量濃度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液,依據酸的電離平衡常數比較酸性強弱為:HSCN>CH3COOH>H2CO3>HCN>HCO3-;水解程度SCN-<CH3COO-<HCO3-<CN-<CO32-;
溶液的pH由大到小的順序為cbda;
故答案為:cbda;
(3)A.CH3COOH溶液加水稀釋過程,雖促進電離,但c(H+)減小,故A不選;
B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$=$\frac{n({H}^{+})}{n(C{H}_{3}COOH)}$,CH3COOH溶液加水稀釋過程,促進電離,氫離子物質的量增大,醋酸物質的量減小,則稀釋過程中比值變大,故B選;
C.稀釋過程,c(H+)減小,c(OH-)增大,c(H+)•c(OH-)=Kw,Kw只受溫度影響所以不變,故C不選;
D.稀釋過程,c(H+)減小,c(OH-)增大,則$\frac{c(O{H}^{_})}{c({H}^{+})}$變大,故D選;
故答案為:BD;
(4)由Ka(CH3COOH)=1.8×10-5和Ka(HSCN)=0.13可知,CH3COOH的酸性弱于HSCN的,即在相同濃度的情況下HSCN溶液中H+的濃度大于CH3COOH溶液中H+的濃度,濃度越大反應速率越快;又酸越弱,反應生成的相應的鈉鹽越易水解,即c(CH3COO-)<c(SCN-),
故答案為:HSCN的酸性比CH3COOH強,其溶液中c(H+)較大,故其溶液與NaHCO3溶液的反應速率快;<.
(5)根據pH=-lgc(H+)=2,則氫離子濃度為10-2,又Kw=c(H+)c(OH-)=10-14,所以氫氧根濃度為10-12;由圖可知,稀釋相同的倍數,pH變化大的酸酸性強,由圖可知,HX的pH變化程度小,則HX酸性弱,電離平衡常數小,醋酸酸性強,電離程度大,則HX的電離平衡常數 小于CH3COOH的電離平衡常數.
故答案為:小于;
(6)CH3COOH與CH3COONa的混合溶液中,存在電荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),所以c(CH3COO-)-c(Na+)=c(H+)-c(OH-)=10-6mol/L-10-8mol/L=9.9×10-7mol/L;
根據緩沖公式pH=pKa-lg($\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$),25℃時CH3COOH的 Ka=1.8×10-5,pKa(CH3COOH)=4.76,所以lg($\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$)=-1.24,即$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18,
故答案為:9.9×10-7;18;
(7)次氯酸酸性大于HCO3-,小于碳酸,少量CO2通入次氯酸鈉溶液中反應生成碳酸氫鈉和次氯酸,反應的離子方程式為:CO2+H2O+ClO-=HCO3-+HClO;
故答案為:CO2+H2O+ClO-=HCO3-+HClO.
點評 本題考查弱電解質的電離、鹽類水解的關系,酸堿混合的定性判斷,注意平衡常數K只與溫度有關,題目以圖象題的形式較好的訓練學生利用信息來分析問題、解決問題的能力,注意把握題目的分析,題目難度中等.


 中考解讀考點精練系列答案
中考解讀考點精練系列答案科目:高中化學 來源: 題型:選擇題
| A. | C6H6 | B. | CH3CHO | C. | CH3COOH | D. | CH2=CH-COOH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 第一電離能 | 電負性 | 穩定性 | 酸性 |
| N>O | C<N | H2S<H2O | H2SO4<HClO4 |
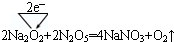 .
.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3COOH | B. | HNO3 | C. | CH3CH2OH | D. | NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2SiO3$\stackrel{△}{→}$SiO2$\stackrel{HCl(aq)}{→}$SiCl4 | |
| B. | S$→_{催化劑/△}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | Ca(ClO)2(aq)$\stackrel{CO_{2}}{→}$HClO(aq)$\stackrel{光照}{→}$HCl(aq) | |
| D. | Fe$→_{△}^{少量Cl_{2}}$FeCl2$\stackrel{NaOH溶液}{→}$Fe(OH)2$\stackrel{空氣中放置}{→}$Fe(OH)3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 第一份 | 第二份 | 第三份 | |
| 樣品的質量/g | 6.830 | 13.660 | 30.000 |
| 二氧化硫氣體的體積/L | 0.672 | 1.344 | 2.688 |
| 硫的質量/g | 0.800 | 1.600 | 3.200 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com