
�X���Ҋ�Ľ���֮һ��
��1�������ᡢ��������A�����X��������ԭ���� ��
��2���{���X��Ҫ��(y��ng)���ڻ�����M(j��n)�������I(y��)�����ßoˮ�Ȼ��X�c�仯�X䇣�LiAlH4�����ЙC(j��)�܄��з���(y��ng)�Ƶü{���X�����W(xu��)����ʽ���£�3LiAlH4+AlCl3="4Al" + 3LiCl + 6H2��
ԓ����(y��ng)���������� ��
��3���仯�X�c��NaAlH4����һ�N��Ҫ�ă�(ch��)����ϣ���֪��
NaAlH4(s)=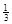 Na3AlH6 (s)+
Na3AlH6 (s)+ 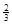 Al (s) + H2(g) ��H��+ 37 kJ��mol��1
Al (s) + H2(g) ��H��+ 37 kJ��mol��1
Na3AlH6(s)="3NaH(s)+" Al (s) + 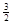 H2(g) ��H��+ 70.5 kJ��mol��1
H2(g) ��H��+ 70.5 kJ��mol��1
�tNaAlH4(s)=" NaH(s)" + Al (s) +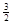 H2(g) ��H�� ��
H2(g) ��H�� ��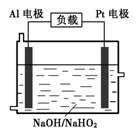
��4����֪H2O2��һ�N���ᣬ�ڏ�(qi��ng)�A����Һ����Ҫ��HO2����ʽ ���ڡ�Ŀǰ�о����^���T��Al��H2O2ȼ��늳أ���ԭ�����҈D��ʾ��늳ؿ�����(y��ng)���£�
2Al+3HO2��+3H2O =2[Al(OH) 4]��+OH��
�����O����(y��ng)ʽ�� ��
���c��ͨ�\�i��늳���ȣ���(d��ng)������ͬ�|(zh��)����ؓ(f��)�O�������|(zh��)�r(sh��)��Al��H2O2ȼ��늳ص���Փ������s����ͨ�\�i��늳ص�______����
��Al늘O�ױ�NaOH��Һ���W(xu��)���g���@��ԓ늳�Ŀǰδ���ƏVʹ�õ�ԭ��֮һ������(y��ng)���x�ӷ���ʽ�� ��
��9�֣���1�������£��X�ױ������ᡢ�������g��
��2��LiAlH4��AlCl3 ��3��+ 60.5 kJ��mol��1
��4���� 3HO2��+3H2O+6e��=9OH������HO2��+H2O+2e��=3OH����
�� 3.6 ��2�֣� �� 2Al+6H2O+2OH��=2[Al(OH) 4]��+3H2��
����ԇ�}��������1�������£��X�ױ������ᡢ�������g�������ԝ����ᡢ��������A�����X�������С�
��2������(j��)����(y��ng)�ķ���ʽ��֪���XԪ�صĻ��σr(ji��)�ģ�3�r(ji��)���͵�0�r(ji��)���õ���ӣ��l(f��)��߀ԭ����(y��ng)��������������LiAlH4��AlCl3 ��
��3������(j��)�w˹���ɿ�֪���٣��ڡ�1/3�����õ�����(y��ng)ʽNaAlH4(s)=" NaH(s)" + Al (s) +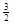 H2(g)������ԓ����(y��ng)�ġ�H����37 kJ/mol��70.5 kJ/mol��3����60.5 kJ/mol.
H2(g)������ԓ����(y��ng)�ġ�H����37 kJ/mol��70.5 kJ/mol��3����60.5 kJ/mol.
��4����ԭ늳������O�õ���ӣ��t����(j��)���ķ���(y��ng)ʽ��֪Alʧȥ��ӣ���ؓ(f��)�O���������O����(y��ng)ʽ��3HO2��+3H2O+6e��=9OH������HO2��+H2O+2e��=3OH������
����ͨ�\�i��늳���ؓ(f��)�O���\��65g�\ʧȥ2mol��ӣ���65g�Xʧȥ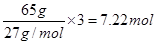 ��ӣ�����Al��H2O2ȼ��늳ص���Փ������s����ͨ�\�i��늳ص�7.22��2��3.6����
��ӣ�����Al��H2O2ȼ��늳ص���Փ������s����ͨ�\�i��늳ص�7.22��2��3.6����
���X�͚ܺ������c��Һ����(y��ng)����ƫ�X���c�͚�⣬����(y��ng)���x�ӷ���ʽ��2Al+6H2O+2OH��=2[Al(OH) 4]��+3H2����
���c(di��n)�������X�����|(zh��)����;������(y��ng)�ᡢ늘O����(y��ng)ʽ�ĕ����Լ����P(gu��n)Ӌ(j��)��
�c(di��n)�u(p��ng)��ԓ�}���е��y�ȵ�ԇ�}��ԇ�}�O(sh��)Ӌ(j��)�·f�����A(ch��)�ԏ�(qi��ng)���������{(di��o)��(d��ng)�W(xu��)���ČW(xu��)��(x��)�dȤ�͌W(xu��)��(x��)�e�O�ԣ����l(f��)�W(xu��)���ČW(xu��)��(x��)��֪����Ҳ���������B(y��ng)�W(xu��)����Ҏ(gu��)�����}������߉������������ߌW(xu��)���ČW(xu��)��(x��)Ч�ʡ�


 С�W(xu��)�n�r(sh��)���I(y��)ȫͨ����ϵ�д�
С�W(xu��)�n�r(sh��)���I(y��)ȫͨ����ϵ�д� ����n���n�r(sh��)Ӗ(x��n)��ϵ�д�
����n���n�r(sh��)Ӗ(x��n)��ϵ�д� ��Ԫȫ�ܾ�����ϵ�д�
��Ԫȫ�ܾ�����ϵ�д� ���S�������ܾ�ϵ�д�
���S�������ܾ�ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�F���仯����֮�g����D(zhu��n)��������ʽ��ʾ��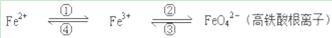
�ش��������P(gu��n)���}��
��1���FԪ�������ڱ��е�λ����___________________________��
��2��Fe�c�^��ϡ���ᷴ��(y��ng)������ȡFeSO4�����÷���(y��ng)���õ�������Һ����(sh��)�F(xi��n)�����ٵ��D(zhu��n)����Ҫ��a(ch��n)�#�������x�õ�ԇ����________���x����̖(h��o)����
A��Cl2 B��Fe C��HNO3 D��H2O2
��3�������D(zhu��n)���õ��������F������늻������S�~�V���V��ˇ�����V���(y��ng)�O�����ķ���(y��ng)���^��(f��)�s��������һ��Ҫ����(y��ng)CuFeS2+4Fe3+��Cu2++5Fe2++2S��CuFeS2��S��-2�r(ji��)���������f�����_����________���x����̖(h��o)����
A�������|(zh��)��ĽǶȿ����S�~�V���ںϽ�
B������(y��ng)�У������FԪ�ؾ���߀ԭ
C������(y��ng)�У�CuFeS2��������������߀ԭ��
D����(d��ng)�D(zhu��n)��1 mol��ӕr(sh��)��46 g CuFeS2���ӷ���(y��ng)
��4����������(y��ng)�У���FeSO4��O2��ϵ��(sh��)�Ȟ�2�U1��ԇ��ƽ���з���ʽ��
FeSO4 + K2O2 �� K2FeO4 + K2O + K2SO4 + O2��
��5����ijϡHNO3��Fe(NO3)3�Ļ����Һ����u�����F�ۣ��a(ch��n)���oɫ���w�� ԓ���w���՚�׃�t��ɫ����Һ��Fe2+��Ⱥͼ���Fe�۵����|(zh��)����֮�g���P(gu��n)ϵ���҈D��ʾ���t�����Һ��HNO3��Fe(NO3)3�����|(zh��)�������֮�Ȟ�__________��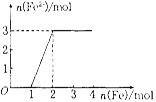
��6��ijͬ�W(xu��)���F�cˮ����ߜط���(y��ng)��Ĺ��w���|(zh��)�ܽ����^���}���У�����Д�������Һ���Ƿ���Fe3+�� ___________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�V�X�⾧ʯ(MgAl2O4)�����ͻ���ϡ��������Ƃ�⾧ʯ�ķ����ǣ���AlCl3��MgCl2�Ļ����Һ(��a��ʾ)�c�^���İ�ˮ(��b��ʾ)����(y��ng)���ٌ��õ��ij����ߜر��������������գ�
��1����ʹMg2+��Al3+ͬ�r(sh��)���ɳ�������(y��ng)ԓ�� ���a����b����������һ��Һ�С�
��2���������Ƃ䷴��(y��ng)�в���Ԫ�صĺ�(ji��n)���x�ӣ�Al3+��Cl�C��Mg2+��H+��O2�C���돽�ɴ�С���������
�����x�ӷ�̖(h��o)��ʾ����
��3��AlCl3�c��ˮ����(y��ng)�ķ���(y��ng)����������У������x�ӻ���������ʽ�� �������y�������x����ʽ ��
��4�������f����Ԫ�صķǽ����Աȵ�Ԫ�؏�(qi��ng)����(sh��)��_________��
a. H2O��NH3��(w��n)�� b. ������ӌ�(du��)ƫ��H-O��H-N
c. ���c(di��n)��H2O��NH3 d. NO���+2�r(ji��)������-2�r(ji��)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
̼���c��̼����c�������г�Ҋ�����|(zh��)��Ո(q��ng)�ش����І��}��
��1��̼����c�Ļ��W(xu��)ʽ�� ���Q ��
��2��̼����c���ί�θ�ᣨ0.2%��0.4%���}�ᣩ�^�࣬����(y��ng)���x�ӷ���ʽ�� �������|(zh��)������̼���c��̼����c�c�����}�ᷴ��(y��ng)�r(sh��)����CO2������ǰ�� ���ߣ����������������������
��3����ȥ̼���c���w��̼����c�ķ���(y��ng)�Ļ��W(xu��)����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
���(du��)����������N���ӵ���;���F(xi��n)�����﹤�̌W(xu��)����������ĵVʯ����ȡ���١��~��һ�N���Ѓr(ji��)ֵ�Ľ��٣����ԏ��~�V����ȡ������Dz���ijЩ��(x��)�����ÿ՚��е������������~�Vʯ���Ѳ����Ե����~�D(zhu��n)���ɿ��ܵ������~�����ü�(x��)����ȡ�~�����a(ch��n)�^�̣������м�(x��)�����ڵĎrʯ���Vʯ���У�������ˮ�Դ��M(j��n)��(x��)�����L(zh��ng)�������������L(zh��ng)�^���У��������ɵ������~�γɵ͝�ȵ���Һ�����Vʯ�ѵĵײ�����?g��u)��@�N��Һ����ȡ�����~��ˮѭ�h(hu��n)ʹ�ã��ٻص��Vʯ���С�������(gu��)��10%���~�����@�N�������a(ch��n)�ġ�
ԇ�ش����І��}��
��1����(x��)�������~�����������~���^��������ʲô���ã� ��
��2���������~��Һ����ȡ�~����(ji��n)�����(j��ng)��(j��)�ķ����� ������(y��ng)�Ļ��W(xu��)����ʽ�飺 ��
��3����ͨ���a(ch��n)�~�ķ������ڿ՚���ȼ�����~���a(ch��n)������һ�N��B(t��i)�������ԇ���^�ɷN�����ă�(y��u)ȱ�c(di��n)��
��
��4����һ�������F�c������ϡH2SO4��������CuO�ƳɆ��|(zh��)�~�������O(sh��)Ӌ(j��)���ɷN��������Fe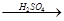 H2
H2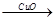 Cu����CuO
Cu����CuO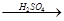 CuSO4
CuSO4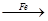 Cu
Cu
������(sh��)�(y��n)ԭ�t�M(j��n)�в������t�����ƵÆ��|(zh��)�~�����ı��^�У����_���� (����)
| A���ٶ� | B���ڶ� | C����� | D���o���Д� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ������}
��15�֣��y�~�Ͻ��V�����ں��չ��I(y��)�����и�U���л����y���Ƃ��~�����a(ch��n)Ʒ�Ĺ�ˇ���£�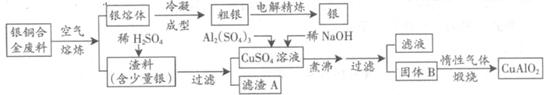
��ע��Al(OH)3��Cu(OH)2�_ʼ�ֽ�Ĝضȷքe��450���80�棩
��1��늽⾫���y�r(sh��)��ꎘO����(y��ng)ʽ�� ���V��A�cϡHNO3����(y��ng)���a(ch��n)���Ě��w�ڿ՚���Ѹ��׃?y��u)�t��ɫ��ԓ���w׃ɫ�Ļ��W(xu��)����ʽ�� ��
��2�����w�����B�ĽM�ɞ� �������ɹ��wB���^���У������NaOH�ļ���������NaOH�^�����t���^������ķ���(y��ng)���x�ӷ���ʽ�� ��
��3������џ��^����һ��(g��)����(y��ng)�Ļ��W(xu��)����ʽ�� CuO+ Al2O3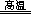 CuAlO2 + ����
CuAlO2 + ����
��4�����y�~�Ͻ����~���|(zh��)����?j��n)?sh��)��63.5%����Փ��5.0kg�U���е��~����ȫ�D(zhu��n)���� mol CuAlO2��������Ҫ1.0mol?L��1��Al2(SO4)3��Һ L��
��5��CuSO4��ҺҲ�������Ƃ�đ�\������������� ���^�V��ϴ����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ������}
.�����}16�֣����(y��n)�C�����ԣ�Cl2>Fe3+>SO2��ijС�M���D��ʾ�b���M(j��n)�Ќ�(sh��)�(y��n)���A�փx���ͼ��мӟ��b�����ԣ��������љz�(y��n)����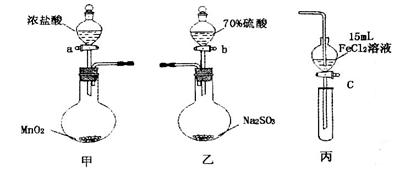
��(sh��)�(y��n)���E��
1.�ڼ��b���У����_����a���ӟᣬ���b���г�M�S�Gɫ���w�r(sh��)���c���b���B�ӡ�
2.��(d��ng)���b����FeC12��Һ׃�S�r(sh��)��ֹͣ�ӟᡣ
3.���_����c��ʹ�s2mL����Һ����ԇ���У��z�(y��n)��Һ�е��x�ӡ�
4.�����b���У����_����b�����՚��űM�����Юa(ch��n)���Ě��wͨ���������b��׃�S�����Һ�У�һ�Εr(sh��)�g��ֹͣ��
5.���±���ԇ�ܣ����_����c��ʹ�s2mL����Һ����ԇ���У��z�(y��n)��Һ�е��x�ӡ�
�ش����І��}��
��1�����аl(f��)������(y��ng)�Ļ��W(xu��)����ʽ��___________________________________________��
��2����70%��������ȡSO2������(y��ng)���ʱ���98%������죬ԭ����__________________��
��3����(sh��)�(y��n)�У��C��������Fe3+��SO2���x�ӷ���ʽ��_____________________________��
��4����I��II��III���Mͬ�W(xu��)�քe�����������(sh��)�(y��n)����(sh��)�(y��n)�Y(ji��)�����£�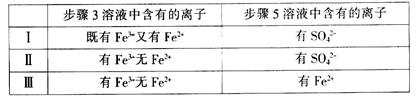
������(sh��)�(y��n)�Y(ji��)��һ���܉��C��������:Cl2>Fe3+>SO2����___________���á�I������II������III����̖(h��o)�ش𣩡�
��5����Ҫ�����ϼͱ��b���C�������Ԟ飺Cl2> Fe3+> I2�ĽY(ji��)Փ���t���E�飺
��������©���м���ɷNԇ��_________��_________��һ�N�܄�__________��
�ڌ����b���Юa(ch��n)����Cl2����ͨ����У��^�����©������Һ�ɫ׃����
������^�쵽������Һ_______________________________________�t�Y(ji��)Փ���_��
��ֹͣͨ��Cl2��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�Ӌ(j��)���}
�����}��15�֣�
��4�N�|(zh��)���ȿ�����ͬ��ͬ���V�X�Ͻ��Ʒ�١��ڡ��ۡ��ܡ��ס��ҡ�������4λͬ�W(xu��)��ȡ1�N��Ʒ���M(j��n)�����Ќ�(sh��)�(y��n)���y(c��)���Ͻ����V���|(zh��)����?j��n)?sh��)��
52����ͬ�W(xu��)ȡ��Ʒ��m1 g���^���Ě������c��Һ����(y��ng)��Ȼ���^�V�������VҺ��ͨ���^���Ķ�����̼?x��)��w�������ó����^�V��ϴ�졢��ɡ��Ɵ����õ����w�|(zh��)���Ԟ�m1 g���t��Ʒ�ٺϽ����V���|(zh��)����?j��n)?sh��)��_____________��
53����ͬ�W(xu��)ȡ��Ʒ��m2 g���������}�ᷴ��(y��ng)��Ȼ��μ��^���Ě������c��Һ���������^�V��ϴ�졢��ɡ��Ɵ����õ����w�|(zh��)���Ԟ�m2 g���t��Ʒ�ںϽ����V���|(zh��)����?j��n)?sh��)��____________��
54����ͬ�W(xu��)ȡ��Ʒ��m3 g��������ϡ���ᷴ��(y��ng)���l(f��)�F(xi��n)���w��ȫ�ܽ⣬��(bi��o)��(zh��n)��r�µõ����w�w�e��V L���t��Ʒ����m3��ȡֵ������___________________________________________��
��ͬ�W(xu��)ȡ��ͬ�|(zh��)���Ę�Ʒ�ܷքe��30 mLͬ��ȵ��}�ᷴ��(y��ng)����ȡ�Ͻ��|(zh��)���c�a(ch��n)�����w�w�e�����D(zhu��n)�����(bi��o)��(zh��n)��r�����£�
| ��(sh��)�(y��n)��̖(h��o) | a | b | c |
| �Ͻ��|(zh��)��/mg | 510 | 765 | 918 |
| ���w�w�e/mL | 560 | 672 | 672 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���(sh��)�(y��n)�}
����̽���^�����c�ď�(qi��ng)�����ԣ�ij�о��ԌW(xu��)��(x��)С�M�O(sh��)Ӌ(j��)����D��ʾ�Č�(sh��)�(y��n)�b�á�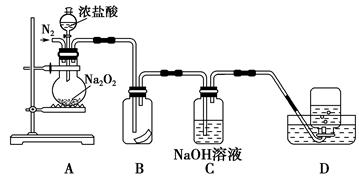
��(sh��)�(y��n)���E���F(xi��n)�����£�
�ٙz���b�Ú����Ժ��b��ˎƷ���B�Ӄx����
�ھ���ͨ��һ������N2���b��D�B�Ӻ�(��(d��o)��ĩ��δ���뼯��ƿ��)������A�ן�ƿ�о����μӝ��}�ᣬ���ҷ���(y��ng)���К��w�a(ch��n)����
��һ�Εr(sh��)�g����(d��o)��ĩ�����뼯��ƿ���ռ����w���b��D���ռ�����ʹ�����ǵ�ľ�l��(f��)ȼ�ğoɫ���w��
�ܷ���(y��ng)�Y(ji��)�����P(gu��n)�]��Һ©���Ļ�������ͨ��һ������N2�����b���К��w�oɫ��
�ش����І��}��
(1)�b��B�Н�(r��n)�ļtɫ���l��ɫ���C��A�з���(y��ng)�� (��W(xu��)ʽ)���ɡ���B�иķŝ�(r��n)�ĵ���KIԇ�����H�{ԇ��׃�{(l��n)�ĬF(xi��n)�����C�������Y(ji��)Փ��Ո(q��ng)���x�ӷ���ʽ�f��ԭ�� ��
(2)�b��C�������� ��
(3)��ͬ�W(xu��)�J(r��n)��O2��Na2O2���}���е�HCl߀ԭ���á���ͬ�W(xu��)�J(r��n)��˽Y(ji��)Փ�����_�������ܵ����ɞ�� ���� ��
(4)��(sh��)�(y��n)�C����Na2O2�c�����HCl�ܷ���(y��ng)����ɲ���ƽԓ���W(xu��)����ʽ�� Na2O2��
Na2O2�� HCl=
HCl= Cl2��
Cl2�� NaCl��
NaCl�� ԓ����(y��ng) (��ܡ����ܡ�)���ڌ�(sh��)�(y��n)�ҿ�����ȡ������Cl2�������� (Ҫ�������c(di��n))��
ԓ����(y��ng) (��ܡ����ܡ�)���ڌ�(sh��)�(y��n)�ҿ�����ȡ������Cl2�������� (Ҫ�������c(di��n))��
�鿴�𰸺ͽ���>>
��(gu��)�H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com