
【題目】某學生利用以下裝置探究氯氣與氨之間的反應。其中A、F分別為氨氣和氯氣的發生裝置,C為純凈干燥的氯氣與氨反應的裝置。請回答下列問題:

(1)裝置A中發生反應的化學方程式為_________________________________;
(2)裝置E中盛裝的溶液是___________;
(3)裝置B能否用裝置D替換,原因是____________________________________;
(4)裝置C內出現濃厚的白煙并在容器內壁凝結,另一生成物是空氣的主要成分之一。寫出反應的化學方程式________________________________________,在標準狀況下,448 mL NH3參加反應,則轉移的電子數為__________。(用NA代表阿伏加德羅常數)
【答案】 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 飽和食鹽水 不能,硫酸與氨氣反應 8NH3+3Cl2=6NH4Cl+N2 0.015 NA
CaCl2+2NH3↑+2H2O 飽和食鹽水 不能,硫酸與氨氣反應 8NH3+3Cl2=6NH4Cl+N2 0.015 NA
【解析】分析:(1)氯化銨和氫氧化鈣在加熱條件下能反應生成氯化鈣、氨氣和水;
(2)依據濃鹽酸具有揮發性,可知制取的氯氣中含有氯化氫、水蒸氣,要收集干燥純凈的氯氣,應除去氯化氫、水蒸氣;
(3)氨氣為堿性氣體應選擇堿性干燥劑;氯氣為酸性氣體應選擇酸性干燥劑;
(4)由題意可知發生反應為氨氣和氯氣生成氯化銨和氮氣,依據原子個數、得失電子守恒寫出反應方程式并計算注意電子數。
詳解:(1)氯化銨和氫氧化鈣在加熱條件下能反應生成氯化鈣、氨氣和水,反應的化學方程式為2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(2)濃鹽酸具有揮發性,所以制備的氯氣中含有氯化氫和水蒸氣,依次通過盛有飽和食鹽水洗氣瓶E、盛有濃硫酸洗氣瓶D可以除去氯化氫和水蒸氣,即裝置E中盛裝的溶液是飽和食鹽水;
(3)氨氣為堿性氣體應選擇堿性干燥劑,濃硫酸為酸性干燥劑,能夠與氨氣反應,不能干燥氨氣,因此裝置B不能用裝置D替換;
(4)氨氣和氯氣反應生成白煙氯化銨和空氣的主要成分之一氮氣,反應的化學方程式為8NH3+3Cl2=6NH4Cl+N2;448mL氨氣的物質的量是0.448L÷22.4L/mol=0.02mol,反應中每消耗8mol氨氣生成1mol氮氣,轉移6mol電子,所以消耗0.02mol氨氣,轉移電子是![]() ,個數是0.015 NA。
,個數是0.015 NA。


科目:高中化學 來源: 題型:
【題目】對下列有機化學的認識中,錯誤的是
A. 反應 ![]() 屬于取代反應
屬于取代反應
B. 淀粉和纖維素屬于多糖,在人體內水解轉化為葡萄糖,為人類提供能量
C. 分枝酸結構簡式如圖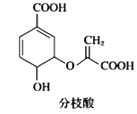 ,可與乙醇、乙酸反應,也可使溴的四氯化碳溶液、酸性高錳酸鉀溶液褪色
,可與乙醇、乙酸反應,也可使溴的四氯化碳溶液、酸性高錳酸鉀溶液褪色
D. 取蔗糖水解液少許,先滴加過量的NaOH溶液,再滴入新制的氫氧化銅懸濁液,加熱,有紅色沉淀生成,證明其水解產物具有還原性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于鐵及其化合物的說法正確的是( )
A.將Fe(NO3)2樣品溶于稀H2SO4后,滴加KSCN溶液,觀察溶液是否變紅,可以檢驗Fe(NO3)2晶體是否已氧化變質
B.濃氨水中滴加FeCl3飽和溶液可制得Fe(OH)3膠體
C.1 mol FeI2與足量氯氣反應時轉移的電子數為2NA
D.水溶液中Fe2+、H+、SO ![]() 、ClO﹣不能大量共存
、ClO﹣不能大量共存
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向含Fe2+、I-、Br-的溶液中通入過量的氯氣,溶液中四種粒子的物質的量變化如圖所示,已知:b-a=5,線段Ⅳ表示一種含氧酸,且Ⅰ和Ⅳ表示的物質中含有相同的元素。下列說法不正確的是
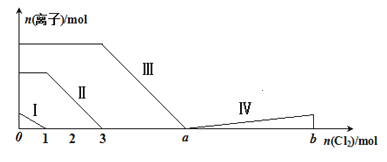
A. 線段Ⅱ表示Fe2+的變化情況
B. 線段Ⅳ發生反應的離子方程式為:I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O
C. 根據圖象可計算a=6
D. 原溶液中c(Fe2+)∶c(I-)∶c(Br-)=2∶1∶3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關氧化還原反應的敘述,正確的是( )
A.一定有氧元素參加B.還原劑本身發生還原反應
C.氧化劑本身發生氧化反應D.一定有電子轉移(得失或偏移)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中學常見單質A、B和甲、乙、丙三種化合物有如圖所示的轉換關系(部分產物未列出).單質A常作為食品包裝材料,甲是兩性氧化物. 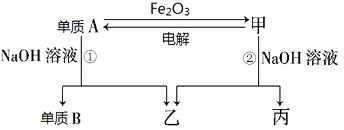
根據圖示轉化關系回答:
(1)寫出下列物質的化學式:單質A , 乙 .
(2)寫出單質A與Fe2O3反應的化學方程式: , 利用該反應的原理,可用于
(3)用單質A做成的容器可以儲存和運輸濃硫酸的原因是 .
(4)寫出反應①的離子方程式: .
(5)工業上冶煉下列物質通常 不采用電解法的是 .
a.Na b.Mg c.Fe d.Ag
(6)用鋁粉和Fe2O3做鋁熱反應實驗,需要的試劑還有
a.KCl b.KClO 3 c.MnO2 d.Mg.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】龍膽酸酯對體外培養的黑素細胞產生黑素的能力有明顯的抑制效應,且沒有細胞毒性和誘變力。是—種高效無毒的藥物皮膚美白劑。合成龍膽酸烷基酯類路線如下:
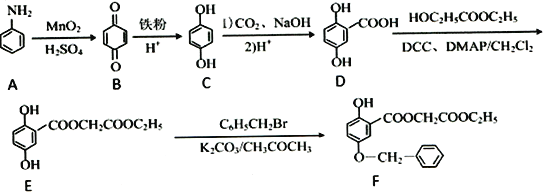
(1)F中含氧官能團的名稱為羥基、_____________、_____________。
(2)E→F的反應類型是_______________。
(3)寫出D→E反應的化學方程式:_________________________________。
(4)寫出滿足下列條件的龍膽酸乙酯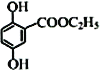 的任意一種同分異構體的結構簡式:__________。
的任意一種同分異構體的結構簡式:__________。
Ⅰ.能發生銀鏡反應,與FeCl3不發生顯色反應但其水解產物之一能與FeCl3發生顯色反應
Ⅱ.核磁共振氫譜有四組峰,且峰面積之比為6 : 2 : 1 : 1
(5)已知: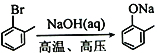 。水楊酸乙酯(
。水楊酸乙酯( )廣泛應用于日用香皂等,根據已有知識并結合相關信息,寫出以苯、乙醇為原料制備水楊酸乙酯的合成路線流程圖(無機試劑任用,合成路線流程圖示例見本題題干)___________________。
)廣泛應用于日用香皂等,根據已有知識并結合相關信息,寫出以苯、乙醇為原料制備水楊酸乙酯的合成路線流程圖(無機試劑任用,合成路線流程圖示例見本題題干)___________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com