
(1)��֪0.5 mol CH4(g)�c0.5 mol ˮ������t �桢p kPa�r����ȫ����(y��ng)����CO��H2�Ļ�Ϛ��w��������a kJ������ԓ����(y��ng)�ğữ�W(xu��)����ʽ��
________________________________________________________________________��
(2)��֪���Пữ�W(xu��)����ʽ
Zn(s)��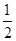 O2(g)===ZnO(s)����H1����Q1 kJ/mol��
O2(g)===ZnO(s)����H1����Q1 kJ/mol��
Hg(l)��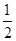 O2(g)===HgO(s)�� ��H2����Q2 kJ/mol��
O2(g)===HgO(s)�� ��H2����Q2 kJ/mol��
Zn(s)��HgO(s)===Hg(l)��ZnO(s) ��H3����Q3 kJ/mol��
�tQ3�cQ1��Q2���P(gu��n)ϵʽ�飺Q3��________��
(1)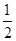 CH4(g)��
CH4(g)��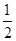 H2O(g)===
H2O(g)===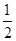 CO(g)��H2(g)����H(t �棬p kPa)����a kJ/mol
CO(g)��H2(g)����H(t �棬p kPa)����a kJ/mol
(2)Q1��Q2
����ԇ�}��������1��0.5 mol CH4(g)�c0.5 mol ˮ������t �桢p kPa�r����ȫ����(y��ng)����CO��H2�Ļ�Ϛ��w��������a kJ�������tԓ����(y��ng)�ğữ�W(xu��)����ʽ��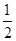 CH4(g)��
CH4(g)��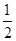 H2O(g)===
H2O(g)===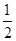 CO(g)��H2(g)����H(t �棬p kPa)����a kJ/mol��
CO(g)��H2(g)����H(t �棬p kPa)����a kJ/mol��
��2������(j��)�w˹���ɿ�֪���٣��ڼ��õ� Zn(s)��HgO(s)===Hg(l)��ZnO(s)������ԓ����(y��ng)�ķ���(y��ng)�ᦤH3����H1����H2������Q3��Q1��Q2��
���c������ữ�W(xu��)����ʽ���Д࣬�w˹���ɵđ�(y��ng)��
�c�u��ԓ�}�ǻ��A(ch��)��ԇ�}�Ŀ��飬ԇ�}�y���m�У�ע�ػ��A(ch��)���������p�飬���������B(y��ng)�W(xu��)����(y��n)֔(j��n)?sh��)�߉������������ߌW(xu��)���������}����Q���}��������



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�������^(q��)2007��4��ģ�M��ԇ���W(xu��)ԇ�} �}�ͣ�058
| |||||||||||||||||||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ���L������2007��߿����W(xu��)����A(y��)�y�} �}�ͣ�058
| |||||||||||||||||||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2011-2012���|��ʡ�߶��όW(xu��)�ڵ�һ�ο�ԇ���W(xu��)ԇ�� �}�ͣ�����}
��6�֣���һ���̶��ݷe�����]�����У�����һ���ض��M(j��n)�����·���(y��ng)��H2(g)��Br2(g)  2HBr(g)����֪����0.5 mol H2��1 mol Br2�r���_(d��)��ƽ�������0.5a mol HBr(Ҋ����֪�)����ͬ�l���£��ұ���ƽ��r���M�ֵ��w�e��?j��n)?sh��)��׃�������о�̖(1)��(3)�Ġ�B(t��i)������еĿհס�
2HBr(g)����֪����0.5 mol H2��1 mol Br2�r���_(d��)��ƽ�������0.5a mol HBr(Ҋ����֪�)����ͬ�l���£��ұ���ƽ��r���M�ֵ��w�e��?j��n)?sh��)��׃�������о�̖(1)��(3)�Ġ�B(t��i)������еĿհס�
|
��̖ |
��ʼ��B(t��i)/ mol |
ƽ��rHBr�����|(zh��)���� / mol |
||
|
H2 |
Br2 |
HBr |
||
|
��֪ |
0.5 |
1 |
0 |
0.5a |
|
(1) |
2 |
4 |
0 |
�� |
|
(2) |
�� |
�� |
1 |
0.5a |
|
(3) |
m |
n(n��2m) |
�� |
�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��ģ�M�} �}�ͣ�����}
 P(g)+Q(g) ��H>0��Ո�ش����І��}��
P(g)+Q(g) ��H>0��Ո�ش����І��}�� �鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
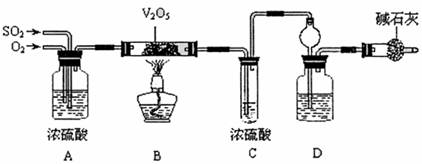
ijУ���С�M���D��ʾ�b�ü����oˎƷ���D�ЊA�փx������ȥ��̽�����I(y��)��������|���еķ���(y��ng)�����y���˗l���¶���������D(zhu��n)���ʡ���֪C�еĝ����Ậ���|(zh��)m mol�����O(sh��)���w�M(j��n)��C��D�r�քe����ȫ���գ��Һ����b�Ã�(n��i)�՚��е�CO2��
Ո�ش����І��}��
��1����֪0.5 mol SO2��O2�����ɚ�B(t��i)SO3���ų�49.15kJ����������(y��ng)�ğữ�W(xu��)����ʽ�� ��
��2���z�����b�õĚ������Ҽ���ˎƷ���_ʼ�M(j��n)�Ќ��˕r���ȑ�(y��ng)�M(j��n)�еIJ�����
��
��3�����rA�����⌧(d��o)ð���Ě����c��������?q��)���ð���Ě��������������Ŀ���?u> ���b��C�Н���������Þ� ���b��D��ʢ�ŵ���Һ�������� ���x����ĸ����
a��BaCl2��Һ b��NaOH��Һ c��NaHSO3���Һ
��4��ֹͣͨ��SO2��Ϩ��ƾ���ʹ�������b���е�SO2��SO3��������գ����������� ��
��5�����Y(ji��)����ϡ��b��C�е���Һ���������м���������BaCl2��Һ���õ��ij����|(zh��)����wg�����b��D���ӵ��|(zh��)����ag���t�˗l���¶���������D(zhu��n)������
���ú���ĸ�Ĵ���(sh��)��ʾ���Y(ji��)���ɲ���������
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com