
(15分)化學(xué)學(xué)科中的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理。請(qǐng)回答下列問題:
Ⅰ.有甲、乙兩個(gè)容積相等的恒容密閉容器,
發(fā)生反應(yīng)3A(g)+B(g)  xC(g)
△H = QKJ/mol
xC(g)
△H = QKJ/mol
回答下列問題:
(1)下列各項(xiàng)能作為判斷該反應(yīng)達(dá)到化學(xué)平衡狀態(tài)的依據(jù)是 (填序號(hào))
① 化學(xué)反應(yīng)速率:v(A)=3v(B) ② 混合氣體的密度保持不變
③ 有3molA消耗的同時(shí)有1molB生成 ④ C的濃度保持不變
(2)根據(jù)試驗(yàn)測(cè)得的數(shù)據(jù)可知,溫度越高該反應(yīng)的化學(xué)平衡常數(shù)越大,則Q 0(填“大于”或“小于”)
(3)向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC,將兩容器的溫度恒定在770K,使反應(yīng)3A(g)+B(g)  xc(g)達(dá)到平衡,此時(shí)測(cè)得甲、乙兩容器中C的體積分?jǐn)?shù)均為0.2 。
xc(g)達(dá)到平衡,此時(shí)測(cè)得甲、乙兩容器中C的體積分?jǐn)?shù)均為0.2 。
① 若平衡時(shí),甲、乙兩容器中A的物質(zhì)的量相等,則x= ;
② 平衡時(shí)甲中A的體積分?jǐn)?shù)為 ;
③ 若平衡時(shí)兩容器的壓強(qiáng)不相等,則兩容器中壓強(qiáng)之比為
Ⅱ.(1)pH=3的鹽酸a L,分別與下列3種溶液混合,充分反應(yīng)后溶液呈中性:
①pH=11的氨水b L; ②物質(zhì)的量濃度為1×10-3 mol/L 氨水c L;
③c(OH-)=1×10-3 mol/L的Ba(OH)2溶液d L;
試判斷a、b、c、d的大小關(guān)系正確的是
A.a(chǎn)=b>c>d B.b>a=d>c C.c>a>d>b D.c>a=d>b
(2)已知室溫的條件下,pH均為5的H2SO4溶液和NH4Cl溶液, 兩溶液中c(H+) • c(OH-)=___________;各取5mL上述溶液,分別加水稀釋至50mL,pH較大的是________溶液;各取5mL上述溶液,分別加熱到90℃,pH較小的是________溶液。
(3)同濃度的下列溶液:①NH4Al(SO4)2;②NH4Cl;③NH3·H2O;④CH3COONH4,其中c(NH4+) 由大到小的順序是: (填編號(hào))。
Ⅲ.一定溫度下的難溶電解質(zhì)AmBn在水溶液中達(dá)到沉淀溶解平衡時(shí),其平衡常數(shù)Ksp=cm(An+)×cn(Bm—),稱為難溶電解質(zhì)的溶度積。
(1)在25℃,AgCl的白色懸濁液中,依次加入等濃度的KI溶液和Na2S溶液,觀察到的現(xiàn)象是 ;
(2) 下列敘述不正確的是 (填字母)
A.溶度積小的沉淀可以轉(zhuǎn)化為溶度積更小的沉淀
B.25℃時(shí),AgCl固體在等物質(zhì)的量濃度NaCl、CaCl2溶液中的溶度積相同。
C.25℃時(shí),飽和AgCl、AgI、Ag2S溶液中所含Ag+的濃度相同
 激活思維優(yōu)加課堂系列答案
激活思維優(yōu)加課堂系列答案 活力試卷系列答案
活力試卷系列答案 課課優(yōu)能力培優(yōu)100分系列答案
課課優(yōu)能力培優(yōu)100分系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:閱讀理解
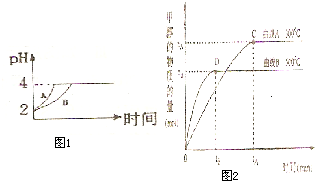 化學(xué)學(xué)科中的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理.請(qǐng)回答下列問題:
化學(xué)學(xué)科中的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理.請(qǐng)回答下列問題:| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
| c2(CO) |
| c(CO2) |
| c2(CO) |
| c(CO2) |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
 化學(xué)學(xué)科中的平衡理論主要內(nèi)容包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡等四種.且均符合勒夏特列原理.請(qǐng)回答下列問題.
化學(xué)學(xué)科中的平衡理論主要內(nèi)容包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡等四種.且均符合勒夏特列原理.請(qǐng)回答下列問題.查看答案和解析>>
科目:高中化學(xué) 來源: 題型:閱讀理解
 化學(xué)學(xué)科中的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理.請(qǐng)回答下列問題:
化學(xué)學(xué)科中的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理.請(qǐng)回答下列問題:| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
| O | 2- 3 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
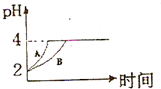 化學(xué)學(xué)科中的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理.請(qǐng)回答下列問題:常溫下,取 pH=2的鹽酸和醋酸溶液各100mL,向其中分別加入適量的Zn粒,反應(yīng)過程中兩溶液的pH變化如圖所示.則圖中表示醋酸溶液中pH變化曲線的是
化學(xué)學(xué)科中的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理.請(qǐng)回答下列問題:常溫下,取 pH=2的鹽酸和醋酸溶液各100mL,向其中分別加入適量的Zn粒,反應(yīng)過程中兩溶液的pH變化如圖所示.則圖中表示醋酸溶液中pH變化曲線的是查看答案和解析>>
國(guó)際學(xué)校優(yōu)選 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com