
 CO2(g) + H2(g)��H1=" +" 41.2kJ/mol
CO2(g) + H2(g)��H1=" +" 41.2kJ/mol CO2(g) + H2(g)��H1=" +" 41.2kJ/mol
CO2(g) + H2(g)��H1=" +" 41.2kJ/mol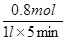 ��0.16mol/��L��min-1 ��������(j��)�ữ�W(xu��)����ʽ��֪������(y��ng)�^��������ğ�����41.2kJ/mol��0.8mol��32.96kJ��
��0.16mol/��L��min-1 ��������(j��)�ữ�W(xu��)����ʽ��֪������(y��ng)�^��������ğ�����41.2kJ/mol��0.8mol��32.96kJ��

 ��У�n��ϵ�д�
��У�n��ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}




| A���ױ�ʾH2�cO2�l(f��)������(y��ng)�^���е�����׃�����tH2�ğ����483.6kJ��mol��1 |
| B���ұ�ʾCu�γɽ��پ��w�r�Ķѷe��ʽ |
| C�����b���П���a�е���ҺpH���� |
| D�����b���д���F��Ʒ��(y��ng)�c�Դ���O���B |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
| A������(y��ng)NH3(g)��HCl(g)=NH4Cl(s)�͜������l(f��)�M�У��f��ԓ����(y��ng)�ġ�H<0 |
| B��Mg�ڿ՚���ȼ���r�l(f��)��ҫ�۵İ⣬������������̖�� |
| C�����A���ڟ�ˮ��ȥ��Ч���������f�����A��ˮ�������ᷴ��(y��ng) |
| D������(y��ng)N2(g)��3H2(g)=2NH3(g)����H��0���_ƽ����͜ضȣ�������(y��ng)���������淴��(y��ng)���ʜpС��ƽ����������(y��ng)�����Ƅ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ������}
 CH3OH(g) ��H1����116 kJ��mol-1
CH3OH(g) ��H1����116 kJ��mol-1| A���S�r��CH3OH�c����(y��ng)�������x |
| B�����ͷ���(y��ng)�ض� |
| C�������wϵ���� |
| D��ʹ�ø�Ч���� |


 CH3OH(g) ��ƽ�ⳣ��(sh��)K = ��
CH3OH(g) ��ƽ�ⳣ��(sh��)K = ���鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
| A�����Ƿşᷴ��(y��ng)�����l(f��)�ġ� |
| B���y��늽��|(zh��)���ܽ�ƽ����һ�N�ӑB(t��i)ƽ�� |
| C�����ó�������(y��ng)���s�r����ʹ�s�|(zh��)�x����ȫ���� |
| D��pH��5���}��ϡ�1000������Һ��pH����8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
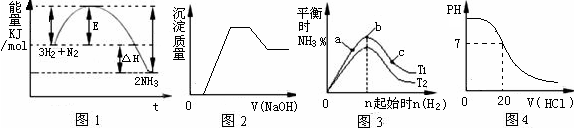
| A���ɈD1��֪�ϳɰ�����(y��ng)���l(f��)����(y��ng)�������m��(d��ng)?sh��)Ĵ�����E�͡�H���pС |
| B���D2��ʾ����H+��Mg2+��Al3+��NH4+�м���NaOH��Һ�c�a(ch��n)�������|(zh��)����׃���P(gu��n)ϵ |
| C���D3��ʾ�ϳɰ�����(y��ng)�������l����׃����r�£���׃��ʼ��n��H2�����˷���(y��ng)ƽ���Ӱ푡���֪����(y��ng)��N2���D(zhu��n)������ߵ���b�c��T1��T2��K2�� K1��T1��T2��ʾ�ضȣ�K1��K2��ʾ����(y��ng)�ض���ƽ�ⳣ��(sh��)�� |
| D���D4��ʾ25��r����0.1 mol��L-1�}��ζ�20 mL 0.1 mol��L-1��ˮ��pH�S�����}���w�e��׃�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}
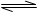 2NH3��g���ġ�H= ��
2NH3��g���ġ�H= ��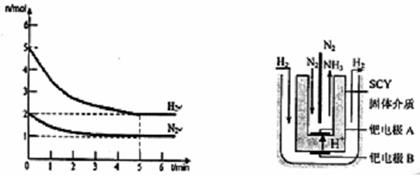
| | H2C2O4 | KHC2O4 | K2C2O4 |
| pH | 2.0 | 3.1 | 8.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}
 CH3CH2OH(g)+H2O(g) ��H=��256.1kJ��mol��1��
CH3CH2OH(g)+H2O(g) ��H=��256.1kJ��mol��1�� CO2(g)+H2(g) ��H=��41.2kJ��mol��1
CO2(g)+H2(g) ��H=��41.2kJ��mol��1 CH3CH2OH(g)+3H2O(l) ��H= ��
CH3CH2OH(g)+3H2O(l) ��H= �� CO+3H2��ԓ����(y��ng)�ڲ�ͬ�ض��µĻ��W(xu��)ƽ�ⳣ��(sh��)���±���
CO+3H2��ԓ����(y��ng)�ڲ�ͬ�ض��µĻ��W(xu��)ƽ�ⳣ��(sh��)���±���| �ض�/�� | 800 | 1000 | 1200 | 1400 |
| ƽ�ⳣ��(sh��) | 0.45 | 1.92 | 276.5 | 1771.5 |
 CO+3H2��ƽ�ⳣ��(sh��)K= ��
CO+3H2��ƽ�ⳣ��(sh��)K= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}
 CH3OH(g)
CH3OH(g) CO+3H2�����Q�ϳɚ���H2�^����CO����Ć��}��ԭ�Ϛ���������CO2��CO3+H2=CO+H2O������ʹ�ϳɚ������ѣ���Փ��ԭ�Ϛ��м����c������̼�w�e�Ȟ�____________________________________��
CO+3H2�����Q�ϳɚ���H2�^����CO����Ć��}��ԭ�Ϛ���������CO2��CO3+H2=CO+H2O������ʹ�ϳɚ������ѣ���Փ��ԭ�Ϛ��м����c������̼�w�e�Ȟ�____________________________________�� �����|(zh��)����׃�����҈D��ʾ�������ϳɼ״��ğữ�W(xu��)����ʽ__________________��
�����|(zh��)����׃�����҈D��ʾ�������ϳɼ״��ğữ�W(xu��)����ʽ__________________��
 ��300��r����(y��ng)�_ʼ10��犃�(n��i)��H2��ƽ������(y��ng)���ʞ�__________��
��300��r����(y��ng)�_ʼ10��犃�(n��i)��H2��ƽ������(y��ng)���ʞ�__________���鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com