
(16分)工業上可以在恒容密閉容器中采用下列反應制備甲醇:
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(1)下列情況可以作為判斷反應達到平衡狀態的依據的是(填序號) 。
A.生成CH3OH 的速率與消耗H2的速率之比為1︰2
B.混合氣體的平均相對分子質量保持不變
C.混合氣體的密度保持不變
D.體系內的壓強保持不變
(2)下表所列數據為該反應在不同溫度下的化學平衡常數:
| 溫度/℃ | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 投料方式 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡數據 | C(CH3OH)/(mol/L) | c1 | c2 | c3 |
| 體系壓強(Pa) | p1 | p2 | p3 | |
| 反應的能量變化 | akJ | bkJ | ckJ | |
| 原料轉化率 | α1 | α2 | α3 | |
(1)BD(答對一個給1分)
(2)① < 增大
< 增大
②80% 250℃
(3)DF(答對一個給1分)
(4)AC(答對一個給1分,見錯不給分)
解析試題分析:(1)A、同一方向,錯誤;B、反應中氣體的總物質的量變化,氣體的質量不變,所以相對分子質量是變量,當不變時達到平衡,正確;C、密度是定值,錯誤;D、氣體的壓強與物質的量成正比,壓強是變量,當不變時達到平衡,正確。(2)溫度升高,K變小,反應放熱;升高溫度正逆反應速率均增大;通過平衡計算的三步法直接計算可得;(3)A、升溫平衡逆向移動,轉化率降低,錯誤;B、催化劑不改變平衡狀態,錯誤;C、加入CO,其轉化率降低,錯誤;D、加入氫氣,增加CO轉化率,正確;E、恒容條件下通入不反應的氣體不能不移動,錯誤;F、降低生成物濃度,平衡正向移動,反應物轉化率提高,正確;
(4)根據題意,把丙設置為丁,則甲乙丁為等效平衡,把丁壓縮到一個容器中,增大壓強,平衡向生成甲醇的方向移動,故有2c1<c3 ,壓強2 p1>p3;甲乙是從兩個不同方向進行到同一個平衡,故有
|a|+|b|=90.8 ,α1+α2 =1,丙中甲醇轉化率小,故有α1+α3<1。
考點:考查化學平衡有關問題。


 小學生10分鐘口算測試100分系列答案
小學生10分鐘口算測試100分系列答案科目:高中化學 來源: 題型:填空題
(1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示_____________,K值大小與溫度的關系是:溫度升高,K值______________(填“一定增大”、“一定減小”、或“可能增大也可能減小”)。
(2)在一體積為10L的容器中,通人一定量的CO和H2O,在850℃時發生如下反應:CO(g)十H2O(g) 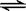 CO2(g)十H2 (g) △H < 0 ;CO和H2O濃度變化如下圖,則 0—4min的平均反應速率v(CO)=______ mol/(L·min)
CO2(g)十H2 (g) △H < 0 ;CO和H2O濃度變化如下圖,則 0—4min的平均反應速率v(CO)=______ mol/(L·min)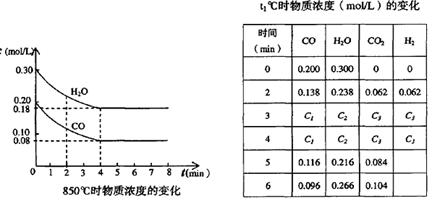
(3)t℃(高于850℃)時,在相同容器中發生上述反應,容器內各物質的濃度變化如上表。
①表中3min—4min之間反應處于_________狀態; C1數值_________0.08 mol/L (填大于、小于或等于)。
②反應在4min—5min問,平衡向逆方向移動,可能的原因是________(單選), 表中5min—6min之間數值發生變化,可能的原因是__________(單選)。
| A.增加水蒸氣 | B.降低溫度 |
| C.使用催化劑 | D.增加氫氣濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一定條件下,可逆反應A2(g)+B2(g)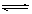 2C(g)在一個密閉容器中達到平衡時,測得c(A2)=0.5mol·L-1,c(B2)=0.1mol·L-1,c(C)=1.6mol·L-1。若
2C(g)在一個密閉容器中達到平衡時,測得c(A2)=0.5mol·L-1,c(B2)=0.1mol·L-1,c(C)=1.6mol·L-1。若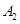 、
、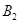 、C的起始濃度分別為a mol·L-1、b mol·L-1、g mol·L-1請確定:
、C的起始濃度分別為a mol·L-1、b mol·L-1、g mol·L-1請確定:
(l)a、g應滿足的關系式為_____________。
(2)若反應從正反應方向開始進行,當g=_________,a有最大值為__________。
(3)若反應從逆反應方向開始進行,當b=_________,a有最小值為_________.
(4)b的取值范圍為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
能源短缺是人類社會面臨的重大問題。甲醇是一種可再生能源,具有廣泛的開發和應用前景。工業上合成甲醇的反應為:CO(g)+2H2(g) CH3OH(g);ΔH
CH3OH(g);ΔH
(1)已知,該反應在300℃,5MPa條件下能自發進行,則ΔH 0,△S 0(填“<,>或=”)。
(2)在300℃,5MPa條件下,將0.20mol的 CO與0.58mol H2的混合氣體充入2L密閉容器發生反應,反應過程中甲醇的物質的量濃度隨時間的變化如圖所示。
①在0~2min內,以H2表示的平均反應速率為 mol·L-1·s-1 ,CO的轉化率為 。
②列式計算300℃時該反應的平衡常數K= 。
③300℃時,將0.50mol CO、1.00mol H2和1.00 mol CH3OH充入容積為2L的密閉容器中,此時反應將 。
A.向正方向移動 B.向逆方向移動 C.處于平衡狀態 D.無法判斷
④下列措施可增加甲醇產率的是 。
A.壓縮容器體積 B.將CH3OH(g)從體系中分離
C.充入He,使體系總壓強增大 D.再充入0.20mol CO和0.58mol H2
(3)若其它條件不變,使反應在500℃下進行,在圖中作出甲醇的物質的量濃度隨時間的變化的示意圖。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)某化學反應2A(g) B(g)+D(g)在四種不同條件下進行,B、D起始濃度為零,反應物A的濃度(mol/L)隨反應時間(min)的變化情況,根據下述數據,完成下列填空:
B(g)+D(g)在四種不同條件下進行,B、D起始濃度為零,反應物A的濃度(mol/L)隨反應時間(min)的變化情況,根據下述數據,完成下列填空:
| 實驗 序號 | 溫度/℃ | 時間/min | ||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c 3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(8分)一定條件下,在體積為3 L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)。根據題意完成下列問題:
CH3OH(g)。根據題意完成下列問題: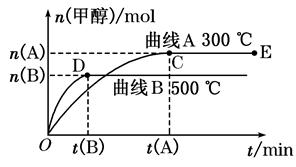
(1)反應達到平衡時,平衡常數表達式K=_________________,升高溫度,K值___________(填“增大”、“減小”或“不變”),平衡向 方向移動。
(2)在500℃,從反應開始到平衡,氫氣的平均反應速率v(H2)=________________。
(3)在其他條件不變的情況下,將處于E點的體系體積壓縮到原來的1/2,下列有關該體系的說法正確的是________(選填選項字母)。
| A.氫氣的濃度減少 |
| B.正反應速率加快,逆反應速率也加快 |
| C.甲醇的物質的量增加 |
D.重新平衡時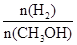 增大 增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
I.高爐煉鐵的主要反應為Fe2O3+3CO2Fe+3CO2。
已知該反應的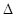 H,在1000℃時,K=64。在1000℃的條,在容積10 L的密閉容器中,加入Fe、Fe2O3、CO、CO2各1.OmoI,反應經10 min后達到平衡。
H,在1000℃時,K=64。在1000℃的條,在容積10 L的密閉容器中,加入Fe、Fe2O3、CO、CO2各1.OmoI,反應經10 min后達到平衡。
(1)該時間范圍內的平均反應速率v(CO2)=_________mol/L min
min
(2) 的最大轉化率_________________。
(3)欲提高CO的平衡轉化率,可采取的措施是_______________。
| A.減少Fe的量 | B.增加Fe2O3的量 |
| C.升高反應溫度 | D.移出部分CO2 |
 FeO(s)+CO(g),其平衡常數為K1;化學反應②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常數為K1;化學反應②:Fe(s)+H2O(g) FeO(s)+H2(g),其平衡常數K2.在溫度973K和1173K情況下,K1、K2的值分別如下:
FeO(s)+H2(g),其平衡常數K2.在溫度973K和1173K情況下,K1、K2的值分別如下:| 溫度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
科學家一直致力于“人工固氮”的新方法研究。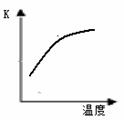
(1)最新“人工固氮”的研究報道:常溫常壓.光照條件下,N2在催化劑表面與水發生反應:2N2 (g)+6H2O(l)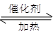 4NH3 (g)+3O2 (g)+ Q
4NH3 (g)+3O2 (g)+ Q
已知該反應的平衡常數K與溫度的關系如右圖,則此反應的 Q 0 (填“>”“<”或“=”)。
(2)常溫下,如果上述反應在體積不變的密閉容器中發生,當反應達到平衡時, (選填編號)。
A.容器中氣體的平均分子量不隨時間而變化 B.v(N2)/ v(O2)=2:3
C.容器中氣體的密度不隨時間而變化 D.通入稀有氣體能提高反應的速率
(3)將反應生成的混合氣體通入水中即可得氨水。用水稀釋0.1mol·L-1氨水,溶液中隨著水量的增加而增大的是 (填字母標號)。
A.c(H+)×c(NH3·H2O)/c(OH-) B.c(NH4+)×c(OH-)/c(NH3·H2O)
C.c(H+)·c(OH-) D.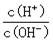
(4)常溫下,在恒壓密閉容器中上述反應達到平衡后,在其他條件不變時,通入2mol N2,請在右圖中畫出正(v正).逆(v逆)反應速率隨時間t變化的示意圖。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知可逆反應CO+H2O(g)  CO2+H2,達到平衡時,K=
CO2+H2,達到平衡時,K=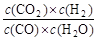 ,K是常數,只與溫度有關,與濃度無關。
,K是常數,只與溫度有關,與濃度無關。
(1)830K時,若起始時:c(CO)=2mol/L,c(H2O)=3mol/L,平衡時CO的轉化率為60%,水蒸氣的轉化率為 ;K值為 。
(2)830K,若只將起始時c(H2O)改為6mol/L,則水蒸氣的轉化率為 。
(3)若830K時,起始濃度c(CO)=a mol/L,c(H2O)=b mol/L,H2的平衡濃度c(H2)=c mol/L,a、b、c之間的關系式是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com