



 智趣寒假作業云南科技出版社系列答案
智趣寒假作業云南科技出版社系列答案科目:高中化學 來源: 題型:閱讀理解
| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 室溫下,將1.00mol/L鹽酸滴入20.00mL 1.00mol/L氨水中,溶液pH和溫度(℃)
室溫下,將1.00mol/L鹽酸滴入20.00mL 1.00mol/L氨水中,溶液pH和溫度(℃)+ 4 |
| 離子濃度的關系 | 溶質 | 溶液的pH | 物料守恒關系 | |
| ① | C(NH4+)>C(Cl-)>C(OH-)>C(H+) | NH4Cl、NH3?H2O NH4Cl、NH3?H2O |
pH>7 | / |
| ② | NH4Cl | / | c(NH4+)+c(NH3?H2O)=c(Cl-) c(NH4+)+c(NH3?H2O)=c(Cl-) | |
| ③ | C(Cl-)>C(H+)>C(NH4+)>C(OH-) | NH4Cl、HCl NH4Cl、HCl |
pH<7 | / |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
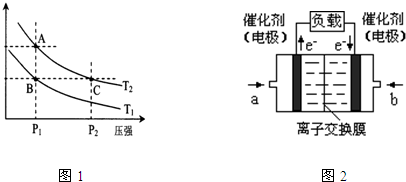
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
| 3 |
| 2 |
| 4 |
| 7 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
火力發電廠釋放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等氣體會造成環境污染。對燃煤廢氣進行脫硝、脫硫和脫碳等處理,可實現綠色環保、節能減排、廢物利用等目的。
(1)脫硝。利用甲烷催化還原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160 kJ·mol-1
甲烷直接將NO2還原為N2的熱化學方程式為__________。
(2)脫碳。將CO2轉化為甲醇的熱化學方程式為:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
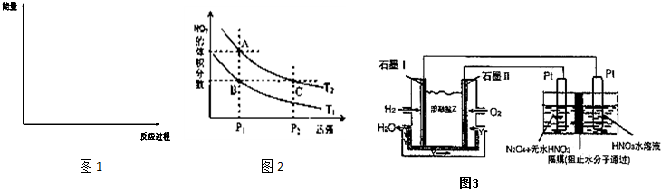
①取五份等體積CO2和H2的混合氣體(物質的量之比均為1∶3),分別加入溫度不同、容積相同的恒容密閉容器中,發生上述反應,反應相同時間后,測得甲醇的體積分數φ(CH3OH) 與反應溫度T的關系曲線如右圖所示,則上述CO2轉化為甲醇的反應的△H3__________0(填“>”、“<”或“=”)。

②在一恒溫恒容密閉容器中充入1 mol CO2和3 mol H2,進行上述反應。測得CO2和CH3OH(g)的濃度隨時間變化如右下圖所示。下列說法正確的是__________(填字母代號)。

A.第10 min后,向該容器中再充入1 mol CO2和3 mol H2,則再次達到平衡時c(CH3OH)=1.5 mol/L
B.0~10 min內,氫氣的平均反應速率[為0.075 mol/(L·min)
C.達到平衡時,氫氣的轉化率為0.75
D.該溫度下,反應的平衡常數的值為3/16
E.升高溫度將使n(CH3OH)/n(CO2)減小
③直接甲醇燃料電池結構如右下圖所示。其工作時正極的電極反應式可表
示為 。

(3)脫硫。某種脫硫工藝中將廢氣經處理后,與一定量的氨氣、空氣反應,生成硫酸銨和硝酸銨的混合物作為副產品化肥。硫酸銨和硝酸銨的水溶液的pH<7,其中原因可用一個離子方程式表示為: ;在一定物質的量濃度的硝酸銨溶液中滴加適量的NaOH溶液,使溶液的pH=7,則溶液中c(Na+)+c(H+)__________c(NO3-)+c(OH-)(填寫“>”“=”或“<”)
查看答案和解析>>
科目:高中化學 來源:同步題 題型:填空題


查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com