
鐵元素是重要的金屬元素,單質鐵在工業和生活中使用得最為廣泛。鐵還有很多重要的化合物及其化學反應。如鐵與水反應:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g) △H
(1)上述反應的平衡常數表達式K=_______。
(2) 已知:①3Fe(s)+2O2(g)=Fe3O4(s) △H1=-1118.4kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H2=-483.8kJ/mol
③2H2(g)+O2(g)=2H2O(l) △H3=-571.8kJ/mol
則△H=_______。
(3)在t0C時,該反應的平衡常數K=16,在2L恒溫恒容密閉容器甲和乙中,分別按下表所示加入物質,反應經過一段時間后達到平衡。
| | Fe | H2O(g) | Fe3O4 | H2 |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
| | Fe | H2O(g) | Fe3O4 | H2 |
| 起始/mol | 3.0 | 4.0 | 0 | 0 |
| 平衡/mol | m | n | p | q |
| | Fe | H2O(g) | Fe3O4 | H2 |
| A/mol | 3.0 | 4.0 | 0 | 0 |
| B/mol | 0 | 0 | 1 | 4 |
| C/mol | m | n | p | q |
(每空2分,最后兩空每空3分,共計14分)(1)K=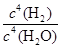 (2)-150.8kJ/mol
(2)-150.8kJ/mol
(3)①33.3% ②BC (4)B>C>A (5)2.79×10-6
解析試題分析:(1)化學平衡常數是在一定條件下,當可逆反應達到平衡狀態時,生成物濃度的冪之積和反應物濃度的冪之積的比值,所以根據該反應的化學方程式可知,平衡常數表達式K=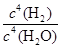 。
。
(2)根據蓋斯定律可知,①-②×2即得到反應3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g),所以該反應的反應熱△H=-1118.4kJ/mol+483.8kJ/mol×2=-150.8kJ/mol。
(3)① 3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g)
起始濃度(mol/L) 0.5 0.5
轉化濃度(mol/L) x x
平衡濃度(mol/L) 0.5-x 0.5+x
則根據平衡常數K=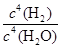 可知
可知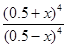 =16
=16
解得x=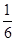 ,所以水蒸氣的轉化率=
,所以水蒸氣的轉化率=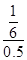 ×100%=33.3%
×100%=33.3%
②A、反應前后體積不變,壓強始終不變,所以若容器壓強恒定,則反應不一定達到平衡狀態,A不正確;B、密度是混合氣的質量和容器容積的比值,在反應過程中容器容積不變,氮氣體的質量是變化的,所以若容器內氣體密度恒定,則反應達到平衡狀態,B正確;C、乙容器相當于是在甲容器的基礎上增加水蒸氣的濃度,平衡向正反應方向移動,但水蒸氣的轉化率降低,即甲容器中H2O的平衡轉化率大于乙容器中H2O的平衡轉化率,C正確;D、四氧化三鐵是固體,所以增加Fe3O4不能提高H2O的轉化率,D不正確,答案選BC。
(4)A相當于是在原平衡的基礎上增大壓強平衡不移動,但反應放熱多。由于是絕熱容器,溫度升高,使平衡向逆反應方向移動,氫氣含量降低;B也相當于是在原平衡的基礎上增大壓強平衡不移動,但反應吸熱。由于是絕熱容器,溫度降低,使平衡向正反應方向移動,氫氣含量增大;C相當于是等效平衡,氫氣含量不變,所以各裝置中H2的百分含量按由大到小的順序排列的關系是B>C>A。
(5)FeCl3溶液的pH為3,則溶液中c(OH-)=10-11mol/L,所以Fe(OH)3的Ksp=2.79×10-39可知,溶液中c(Fe3+)=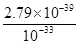 =2.79×10-6mol/L。
=2.79×10-6mol/L。
考點:考查平衡常數、蓋斯定律的應用、外界條件對平衡狀態的影響、轉化率以及溶度積常數的有關計算


科目:高中化學 來源: 題型:填空題
(11分)研究燃料的燃燒和對污染氣體產物的無害化處理,對于防止大氣污染有重要意義。
(1)將煤轉化為清潔氣體燃料:
已知:H2(g)+1/2O2(g)=H2O(g)  H= ?241.8kJ/mol
H= ?241.8kJ/mol
C(s)+1/2O2(g)=CO(g)  H= ?110.5kJ/mol
H= ?110.5kJ/mol
寫出焦炭與水蒸氣反應制H2和CO的熱化學方程式 。
(2)一定條件下,在密閉容器內,SO2被氧化成SO3的熱化學方程式為:2SO2(g)+O2(g) 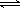 2SO3(g);
2SO3(g);
△H=?a kJ/mo1,在相同條件下要想得到2akJ熱量,加入各物質的物質的量可能是
A.4mo1 SO2和2mol O2 B.4mol SO2、2mo1 O2和2mol SO3
C.4mol SO2和4mo1 O2 D.6mo1 SO2和4mo1 O2
(3)汽車尾氣中NOx和CO的生成及轉化:
①已知氣缸中生成NO的反應為:N2(g)+O2(g)  2NO(g)
2NO(g)  H>0
H>0
在一定溫度下的定容密閉容器中,能說明此反應已達平衡的是
A.壓強不變 B.混合氣體平均相對分子質量不變
C.2v正(N2)=v逆(NO) D. N2的體積分數不再改變
②汽車燃油不完全燃燒時產生CO,有人設想按下列反應除去CO:2CO(g)=2C(s)+O2(g)  H>0,
H>0,
簡述該設想能否實現的依據 。
(4)燃料CO、H2在一定條件下可以相互轉化:CO(g)+H2O(g)  CO2(g)+H2(g)。在420℃時,平衡常數K=9。若反應開始時,CO、H2O的濃度均為0.1mol/L,則CO在此反應條件下的轉化率為 。
CO2(g)+H2(g)。在420℃時,平衡常數K=9。若反應開始時,CO、H2O的濃度均為0.1mol/L,則CO在此反應條件下的轉化率為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(8分)(1)肼(N2H4)是發射航天飛船常用的高能燃料。將NH3和NaClO按一定物質的量比混合反應,生成肼、NaCl和水,該反應的化學方程式是_____________________________。
(2)在火箭推進器中裝有強還原劑肼(N2H4)和強氧化劑過氧化氫,當它們混合時,即產生大量氣體,并放出大量熱。已知:H2O(l)H2O(g) ΔH=" +44" kJ/mol。12.8 g液態肼與足量過氧化氫反應生成氮氣和水蒸氣,放出256.65 kJ的熱量。
①請寫出液態肼與過氧化氫反應生成液態水的熱化學方程式______________________。
②則16 g液態肼與足量過氧化氫反應生成液態水時放出的熱量是___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)已知:2NO2(g) N2O4(g);△H<0。在恒溫恒容條件下,將一定量NO2和N2O4的混合氣體通入容積為2L的密閉容器中,反應過程中各物質的物質的量濃度c隨時間t的變化關系如下圖所示。
N2O4(g);△H<0。在恒溫恒容條件下,將一定量NO2和N2O4的混合氣體通入容積為2L的密閉容器中,反應過程中各物質的物質的量濃度c隨時間t的變化關系如下圖所示。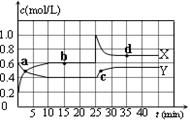
①a、b、c、d四個點中,表示化學反應處于平衡狀態的點是 。
②前10 min內用NO2表示的化學反應速率v(NO2)= mol·L-1·min-1。反應在第一個平衡點的平衡常數K(1)= (可用分數表示)。反應在第二個平衡點的平衡常數K(2)與第一個平衡點的平衡常數K(1)的關系:K(2) K(1)(填“>”、“=”或“<”)。
③請在右圖坐標中畫出1 mol N2O4通入2L的密閉容器中反應發生過程中的能量變化示意圖,并在虛線上分別標出反應物和生成物的化學式。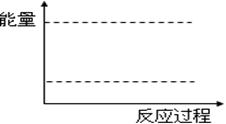
(2)右圖中a、b、c、d分別代表氧族元素(ⅥA族):Te(碲)、Se(硒)、S、O氫化物的反應熱的數據示意圖。試回答下列問題: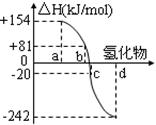
①請你歸納:非金屬元素氫化物的穩定性與形成氫化物的反應熱△H的關系 。
②寫出硒化氫發生分解反應的熱化學反應方程式: 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2013年初,霧霾天氣多次肆虐天津、北京等地區。其中,燃煤和汽車尾氣是造成空氣污染的原因之一。
(1)汽車尾氣凈化的主要原理為:2NO(g) + 2CO(g)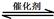 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
①該反應平衡常數表達式
②若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是 (填代號)。
(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題。
煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOX可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
2NO2(g)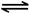 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
寫出CH4催化還原N2O4(g)生成N2和H2O(l)的熱化學方程式: 。
(3)甲烷燃料電池可以提升能量利用率。下圖是利用甲烷燃料電池電解100mL1mol/L食鹽水,電解一段時間后,收集到標準狀況下的氫氣2.24L(設電解后溶液體積不變).
①甲烷燃料電池的負極反應式: 。
②電解后溶液的pH= (忽略氯氣與氫氧化鈉溶液反應)
③陽極產生氣體的體積在標準狀況下是 L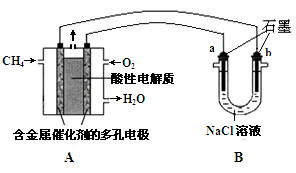
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
SO2和NOx在化學工業上有重要用途,也是大氣污染的主要來源,開發和利用并重,預防和治理并舉是當前工業上和環境保護領域研究的主要課題之一。
(1)在接觸法制硫酸的過程中,發生2SO2(g)+O2(g)  2SO3(g) △H<0反應,某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖所示,根據圖示回答下列問題:
2SO3(g) △H<0反應,某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖所示,根據圖示回答下列問題:
①平衡狀態由A到B時,平衡常數K(A) K(B)(填“>”、“<”或“=”);
②將2.0molSO2和1.0molO2置于10L的密閉容器中,若40s后反應達到平衡,此時體系總壓強為0.10MPa,這一段時間內SO2的平均反應速率為 。
該反應的平衡常數為 。
(2)用CH4催化還原NOx可消除氮的氧化物的污染,例如:
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=—574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=—1160kJ·mol—1
取標準狀況下4.48LCH4并使之完全反應:
①若將NO2還原至N2,整個過程中轉移電子的物質的量為 ;
②若還原NO2和NO的混合物,放出的總熱量Q的取值范圍是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知反應:3I-(aq)+S2O82-(aq)  I3-(aq)+2SO42-(aq)+Q
I3-(aq)+2SO42-(aq)+Q
(1)寫出反應的平衡常數表達式:K= 。
(2)如圖表示反應過程中有關物質的能量,則反應過程中的Q 0(填>、<、=);(I)、(II)兩曲線中,使用催化劑的是 曲線。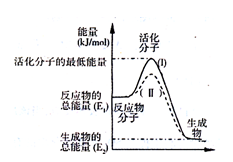
(3)反應的速率可以用I3-與加入的淀粉溶液反應顯藍色的時間t來度量,t越小,反應速率越大。下表是在20℃進行實驗時所記錄的數據
| 實驗編號 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-)/mol·L-1 | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
利用海水資源進行化工生產的部分工藝流程如圖: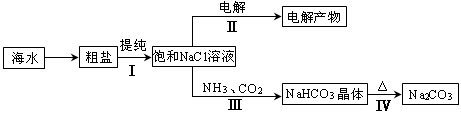
(1)流程I中,欲除去粗鹽中含有的Ca2+、Mg2+、SO42-等離子,需將粗鹽溶解后,按序加入藥品進行沉淀、過濾等。加入藥品和操作的順序可以是 。
a.Na2CO3、NaOH、BaCl2、過濾、鹽酸 b.NaOH、BaCl2、Na2CO3、過濾、鹽酸
c.NaOH、Na2CO3、BaCl2、過濾、鹽酸 d.BaCl2、Na2CO3、NaOH、過濾、鹽酸
(2)流程II中,電解飽和NaCl溶液的離子方程式為 。通電開始后,陽極區產生的氣體是 ,陰極附近溶液pH會 (填“增大”、“減小”或“不變”)。
(3)流程III中,通過反應得到NaHCO3晶體。下圖為NaCl、NH4Cl、NaHCO3、NH4HCO3的溶解度曲線,其中能表示NaHCO3溶解度曲線的是 ,化學反應方程式是 。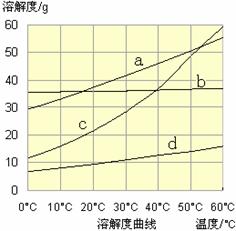
(4)流程IV中,所得純堿常含有少量可溶性雜質,提純它的過程如下:將碳酸鈉樣品加適量水溶解、 、 、過濾、洗滌2-3次,得到純凈Na2CO3?10H2O,Na2CO3?10H2O脫水得到無水碳酸鈉,已知:
Na2CO3·H2O(s)==Na2CO3(s)+H2O(g) ΔH1=+58.73kJ·mol-1
Na2CO3·10H2O(s)==Na2CO3·H2O(s)+9H2O(g) ΔH2=" +473.63" kJ·mol-1
把該過程產生的氣態水完全液化釋放的熱能全部用于生產Na2CO3所需的能耗(不考慮能量損失),若生產1molNa2CO3需要耗能92.36kJ,由此得出:H2O(g)==H2O(l) △H = 。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(10分)拆開1mol H—H鍵,1mol N—H鍵,1mol N≡N鍵分別需要吸收的能量為436kJ,391kJ,946kJ:則(1)1mol N2完全反應生成NH3 熱量(填:吸收或放出) kJ;(2)理論上,每生成1mol NH3, 熱量(填:吸收或放出) kJ;(3)事實上,反應的熱量總小于理論值,為什么? 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com