
 2SO3(g) ��H��0����(y��ng)��ij�ض��£�SO2��ƽ���D(zhu��n)���ʣ������c�wϵ������(qi��ng)��p�����P(gu��n)ϵ���D��ʾ������(j��)�Dʾ�ش����І��}��
2SO3(g) ��H��0����(y��ng)��ij�ض��£�SO2��ƽ���D(zhu��n)���ʣ������c�wϵ������(qi��ng)��p�����P(gu��n)ϵ���D��ʾ������(j��)�Dʾ�ش����І��}��
 2SO3��g��
2SO3��g��


| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}
 H++CN����x�Ħ�H�� kJ��mol��1
H++CN����x�Ħ�H�� kJ��mol��1�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}
 2SO3��g�� ��H="-197" kj��mol���_ʼ�r(sh��)��10 L�����]�����м���4��0 mol SO2��g����10��0 mol O2��g������(d��ng)����(y��ng)�_(d��)��ƽ��r(sh��)���ų�197kJ�ğ�����ԓ�ض��µ�ƽ�ⳣ��(sh��)K= �����ߜض�K�� ������pС��׃������
2SO3��g�� ��H="-197" kj��mol���_ʼ�r(sh��)��10 L�����]�����м���4��0 mol SO2��g����10��0 mol O2��g������(d��ng)����(y��ng)�_(d��)��ƽ��r(sh��)���ų�197kJ�ğ�����ԓ�ض��µ�ƽ�ⳣ��(sh��)K= �����ߜض�K�� ������pС��׃������ 2SO2��g��+O2��g�� 2SO3��g�����_(d��)��ƽ���׃�����l����SO2��O2��SO3��ƽ���ȶ���ԭ��������� ������ĸ����
2SO2��g��+O2��g�� 2SO3��g�����_(d��)��ƽ���׃�����l����SO2��O2��SO3��ƽ���ȶ���ԭ��������� ������ĸ����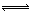 2SO3��g�������W(xu��)�dȤС�M��ͬ�W(xu��)̽���������l����׃�r(sh��)����׃ijһ�l���r(sh��)��(du��)��������(y��ng)��Ӱ푣�������(j��)��(sh��)�(y��n)��(sh��)��(j��)�����������P(gu��n)ϵ�D�������Д������_���� ������ĸ����
2SO3��g�������W(xu��)�dȤС�M��ͬ�W(xu��)̽���������l����׃�r(sh��)����׃ijһ�l���r(sh��)��(du��)��������(y��ng)��Ӱ푣�������(j��)��(sh��)�(y��n)��(sh��)��(j��)�����������P(gu��n)ϵ�D�������Д������_���� ������ĸ����
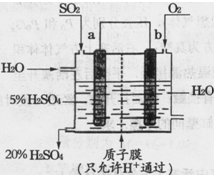
 2SO3��g�� ��H1="-197" kJ��mol��
2SO3��g�� ��H1="-197" kJ��mol���鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}
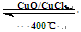 2Cl2(g)+2H2O(g) ��H=" ��115.6" kJ/mol
2Cl2(g)+2H2O(g) ��H=" ��115.6" kJ/mol 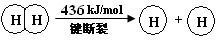

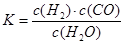 ��������(du��)��(y��ng)�Ļ��W(xu��)����ʽ�飺
��������(du��)��(y��ng)�Ļ��W(xu��)����ʽ�飺  2NH3(g) ��H<0 ��K=0.5���t400��r(sh��)����0.5L�ķ���(y��ng)�������M(j��n)�кϳɰ�����(y��ng)��һ�Εr(sh��)�g�y(c��)��N2��H2��NH3�����|(zh��)�����քe��2mol��1mol��2mol���t�˕r(sh��)����(y��ng)v(N2)�� v(N2)��������������������ܴ_������1�֣�
2NH3(g) ��H<0 ��K=0.5���t400��r(sh��)����0.5L�ķ���(y��ng)�������M(j��n)�кϳɰ�����(y��ng)��һ�Εr(sh��)�g�y(c��)��N2��H2��NH3�����|(zh��)�����քe��2mol��1mol��2mol���t�˕r(sh��)����(y��ng)v(N2)�� v(N2)��������������������ܴ_������1�֣� 2C(g) + D��s�� ��H���仯�W(xu��)ƽ�ⳣ��(sh��)K�c�ض�t���P(gu��n)ϵ���±���
2C(g) + D��s�� ��H���仯�W(xu��)ƽ�ⳣ��(sh��)K�c�ض�t���P(gu��n)ϵ���±���| t/K | 300 | 400 | 500 | �� |
| K/(mol��L��1)2 | 4��106 | 8��107 | K1 | �� |
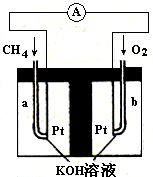
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}


 CH3OH(g)��CO��ƽ���D(zhu��n)�����c�ضȡ�����(qi��ng)���P(gu��n)ϵ���D��ʾ���t��
CH3OH(g)��CO��ƽ���D(zhu��n)�����c�ضȡ�����(qi��ng)���P(gu��n)ϵ���D��ʾ���t��
 CH3OH(g)����(y��ng)��ƽ�ⳣ��(sh��)��________(�ú�a��V�Ĵ���(sh��)ʽ��ʾ)��
CH3OH(g)����(y��ng)��ƽ�ⳣ��(sh��)��________(�ú�a��V�Ĵ���(sh��)ʽ��ʾ)��
 CH3OH(g)��H2O(g)���y(c��)��CO2(g)��CH3OH(g)�ĝ���S�r(sh��)�g׃����������D��ʾ��
CH3OH(g)��H2O(g)���y(c��)��CO2(g)��CH3OH(g)�ĝ���S�r(sh��)�g׃����������D��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
| A��N2H4(l)��2H2O2(l)=N2(g)��4H2O(g) ��H��128.326 kJ��mol��1 |
| B��N2H4(l)��2H2O2(l)=N2(g)��4H2O(g) ��H����128.326 kJ��mol��1 |
| C��N2H4(l)��2H2O2(l)=N2(g)��4H2O(g) ��H����641.63 kJ��mol��1 |
| D��N2H4(l)��2H2O2(l)=N2(g)��4H2O(g) ��H����256.625 kJ��mol��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}


�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com