硫酸工業在國民經濟中占有極其重要的地位.
(1)硫酸的最大消費渠道是化肥工業,用硫酸制造的常見化肥有
硫酸銨或硫酸氫銨或硫酸鋅或硫酸鉀
硫酸銨或硫酸氫銨或硫酸鋅或硫酸鉀
(任寫一種).
(2)硫酸生產中,根據化學平衡原理來確定的條件或措施有
D
D
(填寫序號).
A.礦石加入沸騰爐之前先粉碎 B.使用V
2O
5作催化劑
C.轉化器中使用適宜的溫度 D.凈化后的爐氣中要有過量的空氣
E.催化氧化在常壓下進行 F.吸收塔中用98.3%的濃硫酸吸收SO
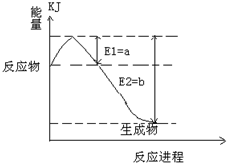
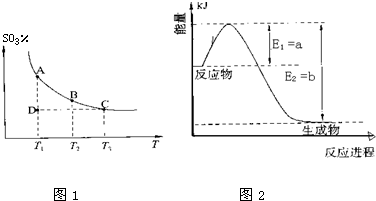
3(3)在硫酸工業中,通過下列反應使二氧化硫轉化為三氧化硫:
2SO
2(g)+O
2(g)
2SO
3(g)△H=-98.3kJ?mol
-1在實際工業生產中,常采用“二轉二吸法”,即將第一次轉化生成的SO
2分離后,將未轉化的SO
2進行二次轉化,假若兩次SO
2的轉化率均為95%,則最終SO
2的轉化率為
99.75%
99.75%
.
(4)硫酸的工業制法過程涉及三個主要的化學反應及相應的設備(沸騰爐、轉化器、吸收塔).
①三個設備分別使反應物之間或冷熱氣體間進行了“對流”.請簡單描述吸收塔中反應物之間是怎樣對流的.
從接觸室中出來的熱氣體SO2、O2、N2、SO3,在吸收塔的底部進入,從下向上運動;
從吸收塔頂部噴灑冷的濃硫酸,從上向下運動;熱氣體SO3與冷的濃硫酸相對流動,進行熱量交換.
從接觸室中出來的熱氣體SO2、O2、N2、SO3,在吸收塔的底部進入,從下向上運動;
從吸收塔頂部噴灑冷的濃硫酸,從上向下運動;熱氣體SO3與冷的濃硫酸相對流動,進行熱量交換.
.
②工業生產中常用氨-酸法進行尾氣脫硫,以達到消除污染、廢物利用的目的.用化學方程式表示其反應原理.(只寫出2個方程式即可)
SO2+2NH3?H2O═(NH4)2SO3,(NH4)2SO3+H2SO4═(NH4)2SO4+SO2↑+H2O
SO2+2NH3?H2O═(NH4)2SO3,(NH4)2SO3+H2SO4═(NH4)2SO4+SO2↑+H2O
.

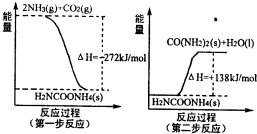


 (2011?松江區模擬)運用化學反應原理研究氮、硫、氯、碘等單質及其化合物的反應有重要意義.
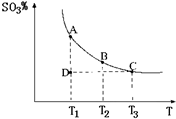
(2011?松江區模擬)運用化學反應原理研究氮、硫、氯、碘等單質及其化合物的反應有重要意義. 2SO3(g),混合體系中SO3的百分含量和溫度的關系如圖所示(曲線上任何一點都表示平衡狀態).根據圖示回答下列問題:
2SO3(g),混合體系中SO3的百分含量和溫度的關系如圖所示(曲線上任何一點都表示平衡狀態).根據圖示回答下列問題: 2SO3(g)是
2SO3(g)是