
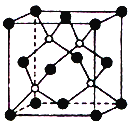
【題目】2013年綿陽科博會場館,大量的照明材料或屏幕都使用了發光的二極管(LED)。目前市售LED鋁片,材質基本以GaAs(砷化鎵)、AlGaInP(氮化銦鎵)為主。已知砷化鎵的晶胞結構如圖。試回答:
(1)鎵的基態原子的外圍電子排布式是_______________。
(2)鎵與鉀、鈣元素的第一電離能從大到小依次為_________________________,與其在同一周期的砷、硒和溴的電負性從大到小依次為_______________。(填元素符號)
(3)此晶胞中所含的砷原子(白色球)個數為_______,與同一個鎵原子相連的砷原子構成的立體構型為___________,鎵采取的雜化方式為________________。
(4)與鎵同主族的元素硼形成的最高價氧化物對應水化物化學式為_____________________,其結構式為_____________,硼酸是_______元酸。
(5)若砷和鎵兩元素的相對原子質量分別為a,b,GaAs晶體結構圖中相距最近的兩個原子的距離為dnm,晶胞參數為________cm,NA表示阿伏伽德羅常數,則該晶體的密度為________g/cm3。
【答案】 4s24p1 Ca>Ga>K Br>Se>As 4 正四面體 sp3 H3BO3 ![]() 一 4√3d/3×l0-7 3√3(a+b)×l021/16d3NA
一 4√3d/3×l0-7 3√3(a+b)×l021/16d3NA
【解析】(1)鎵的原子序數為31,位于周期表中第四周期第IIIA,故其核外價電子的電子排布式為:4s24p1;
(2)鎵與鉀、鈣元素為同周期元素,第一電離能隨核電荷數增大呈增大趨勢,但Ca的s軌道為全充滿形式,相對穩定,第一電離較大,則第一電離從大到小依次為Ca>Ga>K;同周期元素隨核電荷數增大,非金屬性增強,電負性增大,則同一周期的砷、硒和溴的電負性從大到小依次為Br>Se>As;
(3)根據“均攤法”:白色球個數為6×![]() +8×
+8×![]() =4.由晶胞圖可知與同一個鎵原子相連的砷原子構成的空間構型為正四面體,鎵采取的雜化方式為sp3;
=4.由晶胞圖可知與同一個鎵原子相連的砷原子構成的空間構型為正四面體,鎵采取的雜化方式為sp3;
(4)與鎵同主族的元素硼其最高價為+3價,形成的最高價氧化物對應水化物化學式為H3BO3,分子組成內含有3個羥基,其結構式為![]() ,硼酸因促進水的電離而顯酸性是一元酸;
,硼酸因促進水的電離而顯酸性是一元酸;
(5)晶胞中砷的原子個數為4,鎵原子個數為6×![]() +8×
+8×![]() =4,則每個晶胞中含有4個GaAs,每個晶胞的質量為
=4,則每個晶胞中含有4個GaAs,每個晶胞的質量為![]() g,設晶胞參數為xcm,則晶胞的體積為x3cm3,GaAs晶體結構圖中相距最近的兩個原子的距離為dnm=d×10-7cm,晶胞的對角線長為4d×10-7cm,則(4d×10-7)2=3x2,解得:x=
g,設晶胞參數為xcm,則晶胞的體積為x3cm3,GaAs晶體結構圖中相距最近的兩個原子的距離為dnm=d×10-7cm,晶胞的對角線長為4d×10-7cm,則(4d×10-7)2=3x2,解得:x=![]() ×10-7cm;晶胞的密度為
×10-7cm;晶胞的密度為![]() g÷x3cm3=
g÷x3cm3=![]() g/cm3。
g/cm3。


科目:高中化學 來源: 題型:
【題目】33.6g 含雜質的Na2CO3、NaHCO3均勻混合物平均分成兩份,向一份中加入250ml 1.00mol·L-1過量鹽酸反應,生成標準狀況下3.36L氣體。將另一份充分灼燒,干燥后稱得固體質量為13.7g。雜質不與酸反應,受熱也不分解。求:
(1)原混合物中含有Na2CO3的物質的量。
(2)Na2CO3、NaHCO3的質量比。(寫出計算過程)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是 ( )
A. 含多個電子的原子里,能量高的電子在離核近的區域運動
B. 每個電子層最多容納的電子數是2n2個
C. 最外層電子數不超過8個(K層為最外層時,電子數不超過2個)
D. 核外電子是分層排布的,元素的化學性質與原子的最外層電子排布密切相關
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知反應:2H2O2=2H2O+O2↑,若其他條件不變,下列措施不能加快該反應速率的是
A. 升高溫度 B. 加入少量MnO2
C. 加入濃度更高的H2O2溶液 D. 加水稀釋H2O2溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數,下列說法正確的是
① 18g D2O含有的電子數為10NA;
② 1mol Na2O2與水完全反應時轉移電子數為2NA ;
③ 12g石墨烯(單層石墨)中含有六元環的個數為0.5NA;
④ 在標準狀況下,22.4LSO3的物質的量為1mol;
⑤ 7.8g過氧化鈉中含有的離子數為0.3NA;
⑥ 28g 硅晶體中含有2NA個Si—Si鍵
⑦ 200mL1mol/LFe2(SO4)3溶液中,Fe3+和SO42-離子數的總和是NA
⑧ 在常溫常壓下,0.1mol鐵與0.1molCl2充分反應,轉移的電子數為0.3NA
⑨ 標準狀況下,22.4LNO和11.2LO2混合后氣體的分子總數為1.5NA
⑩ S2和S8的混合物共6.4g,其中所含硫原子數一定為0.2NA
A、①③⑤⑧ B、②④⑥⑦ C、③⑤⑥⑩ D、⑤⑧⑨⑩
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:硫酸銅溶液中滴入氨基乙酸鈉(H2N-CH2-COONa)即可得到配合物A。其結構如圖4所示:
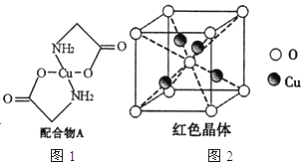
(1)Cu元素基態原子的外圍電子排布式為______________。
(2)元素C、N、O的第一電離能由大到小排列順序為_______________。
(3)配合物A中碳原子的軌道雜化類型為_______________________。
(4)1mol氨基乙酸鈉(H2N-CH2-COONa)含有![]() 鍵的數目為____________mol。
鍵的數目為____________mol。
(5)氨基乙酸鈉分解產物之一為二氧化碳。寫出二氧化碳的一種等電子體:____________(寫化學式)。
(6)已知:硫酸銅灼燒可以生成一種紅色晶體,其結構如圖2所示,則該化合物的化學式是_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】姜黃素是從姜科植物中提取的一種色素,它的主要藥理作用有抗氧化、保肝護肝、抑制腫瘤生長等,它具有對稱性結構。

己知:E、G能發生銀鏡反應![]() (R、R、R"表示烴基或氫原子)
(R、R、R"表示烴基或氫原子)
請根據以上信息回答下列問題:
(1)生成A的反應類型是______,試劑X的名稱是_________。
(2)寫出下列反應的化學方程式
A→B:_____________;E→F:_____________。
(3)G的核磁共振氫譜峰面積之比________。
(4)J(C8H8O3)的同分異構體中同時滿足如下條件:① 能與NaHCO3反應,② 能使FeCl3溶液顯色,共有______種(不考慮立體異構),其中苯環上的一氯代物有兩種的同分異構體的結構簡式是_______。
(5)姜黃素的結構簡式___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com