
�}Ŀ�б�(�����𰸺ͽ���)

| ||
| ||
��15�֣�
���F����ĝ��������ܰl(f��)���g����ij�dȤС�Mͬ�W(xu��)�l(f��)�F(xi��n)��һ�����ļ��F�c������ӟ�r���F��ȫ�ܽ⣬�õ���ҺA�����a(ch��n)���������wB����(sh��)�(y��n)�ҬF(xi��n)������ԇ���� 0.01mol/L ����KMnO4��Һ��0.1 mol/LKI��Һ��3��H2O2��Һ��������Һ�����sˮ��Ո��f(xi��)������̽��������Һ�͚��w�ijɷ֣��������P(gu��n)��(sh��)�(y��n)�������A(y��)�ڬF(xi��n)��ͽY(ji��)Փ�������б����С�
[�������]
��������Һ�еĽ����x�ӿ��ܺ���Fe2����Fe3���е�һ�N��ɷN��
�����Ú��w�п��ܺ��� �е�һ�N��ɷN��
�����⌑��һ���F�c������ӟ�r�����ܰl(f��)�������P(gu��n)����(y��ng)����ʽ
[��(sh��)�(y��n)̽��]
|
| ��(sh��)�(y��n)���� | �A(y��)�ڬF(xi��n)�� | �Y(ji��) Փ |
| �(y��n)�C����� | ���E�٣�ȡ������ҺA������0.01 mol/L ����KMnO4��Һ | [��Դ:�W(xu��)&��&�W(w��ng)Z&X&X&K] |
|
| ���E�ڣ� |
| ����Fe3�� | |
| �(y��n)�C����� | �����Ú��wBͨ�����D�b�� |
| ���ЃɷN���w |
[���}ӑՓ]
��ͬ�W(xu��)������������x��KSCN��Һ���t
�H����KSCN��H2O2�ɷN��Һ�������
����������̽����Ո��ԓ�^�c(di��n)�M(j��n)���u�r��
��
�F����ĝ��������ܰl(f��)���g����ij�dȤС�M��ͬ�W(xu��)�l(f��)�F(xi��n)��һ�������F�c������ӟ�r���^�쵽�F��ȫ�ܽ⣬���a(ch��n)���������w����(sh��)�(y��n)�ҬF(xi��n)������ԇ����0.01 mol/L����KMnO4��Һ��0.1 mol/L KI��Һ��3%H2O2��Һ��������Һ�����sˮ��Ո��f(xi��)������̽��������Һ�͚��w�ijɷ֡�
��������롿
��.������Һ�еĽ����x�ӿ��ܺ���Fe2����Fe3���е�һ�N��ɷN��
��.���Ú��w�п��ܺ���________�е�һ�N��ɷN��
| | ��(sh��)�(y��n)���� | �A(y��)�ڬF(xi��n)�� | �Y(ji��)Փ |
| �(y��n)�C����� | ���E�٣�ȡ����0.01 mol/L����KMnO4��Һ������������Һ | | |
| ���E�ڣ�________ | | ����Fe3 | |
| �(y��n)�C����� | �����Ú��wͨ�������b�� | | ���ЃɷN���w |
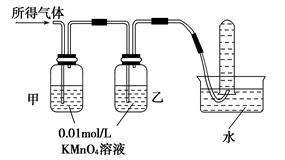
�F����ĝ��������ܰl(f��)���g����ij�dȤС�M��ͬ�W(xu��)�l(f��)�F(xi��n)��һ�������F�c������ӟ�r���^�쵽�F��ȫ�ܽ⣬���a(ch��n)���������w����(sh��)�(y��n)�ҬF(xi��n)������ԇ����0.01 mol/L����KMnO4��Һ��0.1 mol/L KI��Һ��3%H2O2��Һ��������Һ�����sˮ��Ո��f(xi��)������̽��������Һ�͚��w�ijɷ֡�
��������롿
��.������Һ�еĽ����x�ӿ��ܺ���Fe2����Fe3���е�һ�N��ɷN��
��.���Ú��w�п��ܺ���________�е�һ�N��ɷN��
| ��(sh��)�(y��n)���� | �A(y��)�ڬF(xi��n)�� | �Y(ji��)Փ |
�(y��n)�C������ | ���E����ȡ����0.01 mol/L����KMnO4��Һ������������Һ |
|
|
���E����________ |
| ����Fe3 | |
�(y��n)�C������ | �����Ú��wͨ�������b�� |
| ���ЃɷN���w |
����(sh��)�(y��n)̽����
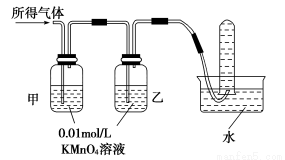
�����}ӑՓ��
��ͬ�W(xu��)������������x��KSCN��Һ���t�H����KSCN��H2O2�ɷN��Һ������ɲ�����������̽�����Д�ԓ�����Ƿ����_���M(j��n)���u�r��_____________________________
| ��(sh��)�(y��n)���� | �A(y��)�ڬF(xi��n)�� | �Y(ji��) Փ | |
| �(y��n)�C����� | ���E�٣�ȡ����0.01mol/L ����KMnO4��Һ������������Һ | ||
| ���E�ڣ� | ����Fe3+ | ||
| �(y��n)�C����� | �����Ú��wͨ�������b�� | ���ЃɷN���w |

һ�����(xi��ng)�x���}�����}����8С�}��ÿ�}3�֣���24�֡���
1��D 2��B 3��A 4��D 5��B 6��C 7��C 8��A
���������(xi��ng)�x���}�����}����6С�}��ÿС�}4�֣���24�֡���
9��AD 10��B 11��BC 12��AD 13��CD 14��C
�������x���}�����}����6С�}����60�֣�
15����10�֣�
��������롿 SO2��H2
����(sh��)�(y��n)̽����
�����
���E�� ��Һ�ϼtɫ��ȥ ����Fe2��
���E�� ��ȡ����������Һ���μ�KI�͵�����Һ ��Һ׃?y��u)��{(l��n)ɫ
�����
����KMnO4��Һ��ɫ������KMnO4��Һ�ɫ��׃��ԇ�����ռ������w
�����}ӑՓ��
�����_������Һ�к���Fe3���t�o���z�(y��n)��Һ���Ƿ���Fe2��
16����8�֣�
 �� HNO3
�� HNO3
�� 3CuO��2NH3 3Cu��N2��3H2O
�� 2Cu2����2Cl����SO2��2H2O��2CuCl����4H����SO42��

�� 6NO��4NH3 5N2��6H2O
17����10�֣�
��1��0.3 mol/(L?min) ���ߜض�
��2��

��3����41.2 kJ/mol a
18����10�֣�
�� ��׃�����㣨��S��0�� ���^�՚�
�� 10 TiO2����2H2O��TiO(OH)2����2H��
�� d
19����12�֣�
��1��4
��2�� ߀ԭ����(y��ng)
߀ԭ����(y��ng)
��3�� ��
��
��4��
20����10�֣�

�� ��
�� �⣺(C6H10O5)n��n C6H12O6��2nC2H5OH��nCH3COOC2H5
162n 88n
m(CH3COOC2H5)��374 kg
�� �⣺[(C6H7O2)(OH)3]n��[(C6H7O2)(OH)(3��x)(OOCCH3)x]n ��m
162n 162n��42nx 42nx
 ��
�� x��2
x��2
��ԓ�����w�S�ĽY(ji��)��(g��u)��ʽ��[(C6H7O2)(OH)(OOCCH3)2]n
�ġ��x���}�����}����1С�}����12�֣�
21����12�֣�
A���� O��N��C 1s22s22p63s23p63d84s2
�� ��K������ˮ����?y��n)����ǘO�Է��ӣ������ژO���܄�
�� 4
��
�� �� sp3��sp2
�� sp3��sp2
B���� ���������z�^�ι� ��г�ȥCO2��Ѹ����s
�� ��̪ �ζ��a(ch��n)��CH3COONa��Һ�ʉA�ԣ���(y��ng)�x���ډA�Է�����׃ɫ��ָʾ��
�� �û���̿Óɫ
�� 4.50
2009����ͨ�и����꼉��һ���{(di��o)�Мyԇ
���W(xu��)ԇ�}����
1�����О�Ŀ��(bi��o)�����}�ԭh(hu��n)�����o(h��)�鱳�������ѿ����P(gu��n)ע�r�¡��P(gu��n)ע�����
����(n��i)���I(l��ng)���W(xu��)��������ͻ�����Փ
�����}��ʾ���������mȻ���|(zh��)��(w��n)���������Ɖij����ӡ�
���� ����D
���y��ϵ��(sh��)��0.85���˽⣬�^���ף�
2�����О�Ŀ��(bi��o)���ܶ���r�£���ͬ�ķ���(y��ng)���ڝ�ȡ��ضȡ��������܄������l����ͬ�r���õ��Įa(ch��n)�ﲻͬ�����}���@һ�������W(xu��)��(sh��)�����}����������W(xu��)����Ԫ�ػ�����֪�R���ЙC(j��)���W(xu��)֪�R��������r��
����(n��i)���I(l��ng)��Ԫ�ؼ��仯����
�����}��ʾ���Ȼ��X��Һ�c��ˮ����(y��ng)����Al(OH)3����Al(OH)3�������^����ˮ��
���� ����D
���y��ϵ��(sh��)��0.75�����⣬�^���ף�
3�����О�Ŀ��(bi��o)����ͬ�Ļ��W(xu��)��(sh��)�(y��n)�F(xi��n)�l(f��)����׃����һ����ͬ���漰�ķ���(y��ng)ԭ��Ҳ��һ����ͬ�����}���@һ�����q�C�^������}�زģ�����W(xu��)����Ԫ�ػ�����֪�R���ЙC(j��)���W(xu��)֪�R��������r��
����(n��i)���I(l��ng)��Ԫ�ؼ��仯����
�����}��ʾ�������|(zh��)��Һ�м��������@��Һ�г����������l(f��)�����}����������׃���������������~��Һ�г����������l(f��)����׃�ԣ��ǻ��W(xu��)׃�����Ȼ��^��Һ��ͨ�����������w����ˮ�����������������������a(ch��n)�������^���������백ˮ�����������D(zhu��n)���遆��������l(f��)����(f��)�ֽⷴ��(y��ng)���Ɂ������^���������A�ͼ��A����Һ�ڟoɫ�������Ɵ������ǰl(f��)����ɫ����(y��ng)�������������ښ������c��Һ�������������c�A�ķ���(y��ng)���������������ښ����ķ���(y��ng)ԭ����ͬ��
���� ����C
���y��ϵ��(sh��)��0.75�����⣬�^���ף�
4�����О�Ŀ��(bi��o)���ĺ�������ȡ���Ǻ����YԴ�C�����õ�һ�N���������}�ԏĺ�������ȡ����^�̞����}��������������|(zh��)���x�c�ἃ�����P(gu��n)��(sh��)�(y��n)������
����(n��i)���I(l��ng)���W(xu��)��(sh��)�(y��n)
�����}��ʾ�������Ɵ��ɻґ�(y��ng)��������M(j��n)�У��^�V�r��(y��ng)�ò�������������ı���Һ�ڷ�Һ©����λ���όӣ���(y��ng)����Һ�w�ų�����Ͽڵ��������x�Ⲣ���ձ���(y��ng)�����s�ķ�������ˮԡ�ӟ��ܿ��ƜضȲ�����̫�߶���ֹ������A��
���� ����D
���y��ϵ��(sh��)��0.55�����⣬�е��y�ȣ�
5�����О�Ŀ��(bi��o)��DDT�������w��(n��i)�y�Խ��⣬��˿ƌW(xu��)�������˺ܶ�����a(ch��n)Ʒ�����}����һ�N���Ʒ���زģ������ЙC(j��)��ĽY(ji��)��(g��u)�����܈F(tu��n)�ͻ��W(xu��)���|(zh��)��
����(n��i)���I(l��ng)���ЙC(j��)���W(xu��)���A(ch��)
�����}��ʾ��������A�к��еĹ��܈F(tu��n)��̼̼�p�I��ȩ���ʹ��u�����]�б��h(hu��n)�Y(ji��)��(g��u)���������ܰl(f��)���ӳɷ���(y��ng)��ȡ������(y��ng)���y�R����(y��ng)�������c�Ȼ��F��Һ����(y��ng)�@��ɫ��������������5��̼ԭ�ӹ�ƽ�棬�c�����ȫ�ӳɕr�����|(zh��)����֮�Ȟ�1��3��
���� ����B
���y��ϵ��(sh��)��0.75�����⣬�^���ף���
6�����О�Ŀ��(bi��o)��ԓ�}�����ӵ��_����(sh��)�đ�(y��ng)�Þ��d�w������W(xu��)����ԭ늳ء��}�ˮ�⡢���淴��(y��ng)�Ȼ�����Փ֪�R�����Ց�(y��ng)�ú����P(gu��n)��Ӌ(j��)������������W(xu��)��˼�S�Ŀb���Ժ�˼�S���`���ԡ�
����(n��i)���I(l��ng)���W(xu��)Ӌ(j��)��
�����}��ʾ��NH4Cl��Һ������NH4����ˮ���ʹNH4���x�Ӕ�(sh��)Ŀ�p�٣�������Cu��Znԭ늳��Юa(ch��n)����
���� ����C
���y��ϵ��(sh��)��0.65�����⣬�е��y�ȣ�
7�����О�Ŀ��(bi��o)��ԓ�}�ԡ����ڱ���Ԫ�ص��Ɣࡱ���d�w������W(xu��)����Ԫ�����ڱ�����Ϥ�̶ȼ��䌦���и�Ԫ�����|(zh��)������(y��ng)ԭ�ӽY(ji��)��(g��u)���������f׃Ҏ(gu��)�ɵ��J(r��n)�R�����ճ̶ȡ�
����(n��i)���I(l��ng)���W(xu��)��������ͻ�����Փ
�����}��ʾ���}�е�X��Y��Z��W����(y��ng)��Ԫ����3�N���ܣ�C��N��Al��Si��N��O��Si��P��O��F��P��S��
���� ����C
���y��ϵ��(sh��)��0.55�����⣬�е��y�ȣ���
8�����О�Ŀ��(bi��o)�����}�ԎN��ͬ��A����Һ�е��x�ӹ��憖�}���d�w�����鳣Ҋ�x�ӵ����|(zh��)����Һ��pH��ˮ����x�Ȼ�����Փ֪�R��
����(n��i)���I(l��ng)��Ԫ�ؼ��仯����
�����}��ʾ���}��4���x�(xi��ng)���O(sh��)���ǽ�(j��ng)�^��˼��]�ģ�A��������Һ��B�ljA����Һ��C��D�ȿ�����������ҺҲ�����ljA����Һ��Aһ���ܴ������棬B��Cһ�����ܴ������棬D���ܴ������档���}���H��һ�����}��Ҳ��һ���ܺõď�(f��)��(x��)�}��
���� ����A
���y��ϵ��(sh��)��0.65�����⣬�е��y�ȣ�
9�����О�Ŀ��(bi��o)�����{(l��n)����F������һ�N���������}�Կ��{(l��n)�ķ���(y��ng)ԭ����d�w�������|(zh��)�ķ������߀ԭ����(y��ng)�����P(gu��n)���
����(n��i)���I(l��ng)���W(xu��)��������
�����}��ʾ������(y��ng)����ƽ��H2O�Ļ��W(xu��)Ӌ(j��)����(sh��)��5������(y��ng)�۲�������߀ԭ����(y��ng)��
���� ����AD
���y��ϵ��(sh��)��0.5�����⣬�^�y��
10�����О�Ŀ��(bi��o)�����}����һЩ��Ҋ�x�ӷ���(y��ng)����ʽ���`���Дࡣ�Д��x�ӷ���ʽ�����`��һ���4�������M(j��n)�У��Ƿ���Ͽ��^��(sh��)�����W(xu��)ʽ�IJ���Ƿ����_����ƽ�Ƿ����_���Ƿ���Ϸ���(y��ng)���g�����P(gu��n)ϵ�����}�r���������O(sh��)���e�`�x�(xi��ng)��
����(n��i)���I(l��ng)��Ԫ�ؼ��仯����
�����}��ʾ��A�������܌���2�r�F�ͣ�2�r��������������ֻ�l(f��)����(f��)�ֽⷴ��(y��ng)��C��HCO3������(y��ng)���_��D��ͨ���^��CO2��(y��ng)����HCO3����
���� ����B
���y��ϵ��(sh��)��0.6�����⣬�е��y�ȣ�
11�����О�Ŀ��(bi��o)�����}�ԃɂ�������(sh��)�(y��n)�̓ɂ��Ƃ䌍(sh��)�(y��n)���d�w�����黯�W(xu��)��(sh��)�(y��n)�Ļ���������
����(n��i)���I(l��ng)���W(xu��)��(sh��)�(y��n)
�����}��ʾ�����}��O�ד]�l(f��)�����ܾ��_����һ�����|(zh��)������ȵ���Һ����A�к͵ζ��У��ζ������ô��bҺ�w��ϴ���F��ƿ����Ҫ���ⰱˮ�м�����ʯ�ң���ʹ�ض�������������OH����ȣ����Եõ����⣬ͨ�^�Aʯ�Һ��ܵõ���������İ��⣻���Ȼ��F��Һ�м���������c��Һ���õ����ǚ������F�����������z�w��
���� ����BC
���y��ϵ��(sh��)��0.4�����⣬�^�y��
12�����О�Ŀ��(bi��o)�����}��늽�ԭ���ڹ��I(y��)�ϵđ�(y��ng)�á�
����(n��i)���I(l��ng)���W(xu��)������Փ
�����}��ʾ���~��늽⾫���r����(y��ng)�ô��~��ꖘO�����~��ꎘO���僕r����(y��ng)��僌ӽ�����ꖘO����僽�����ꎘO��
���� ����AD
���y��ϵ��(sh��)��0.65�����⣬�е��y�ȣ�
13�����О�Ŀ��(bi��o)��ԓ�}Ҫ��Ҫ��W(xu��)������(j��)��Һ���}��ˮ�⡢��늽��|(zh��)����x��늺��غ�Ȼ��W(xu��)׃����Ҏ(gu��)�ɣ��Д���Һ���x�ӝ�ȵ�������С���C�Ͽ���W(xu��)����늽��|(zh��)��Һ����ԭ����������r�;C�Ϸ�����Q���}��������
����(n��i)���I(l��ng)���W(xu��)��������ͻ�����Փ
�����}��ʾ��A��HCO3����CO32���ĝ�Ȳ����ܶ�����0.1 mol/L����t�������ʹ���0.2 mol/L��B�����û����Һ��(y��ng)�@���ԣ�C��(sh��)�H�������늺��غ㣬c(Na��)��0.1
mol/L��D�пɵ�늺��غ��ʽc(Na��)��c(H��)�� c(HCO3��)��
���� ����CD
���y��ϵ��(sh��)��0.45�����⣬�^�y��
14�����О�Ŀ��(bi��o)�����}�����P(gu��n)�ڻ����ĺ��λ��W(xu��)Ӌ(j��)�㡣
����(n��i)���I(l��ng)���W(xu��)Ӌ(j��)��
�����}��ʾ��n(SO42��)��b mol��n(NH4��)��c mol������(j��)늺��غ㣬n(Al3��)�� mol��
mol��
���� ����C
���y��ϵ��(sh��)��0.75�����⣬�^���ף�
15�����О�Ŀ��(bi��o)�����}��һ�l�C�����^��(qi��ng)�Ļ��W(xu��)��(sh��)�(y��n)�}���}Ŀ�Ԍ��ӟ�l�����F�c�����ᷴ��(y��ng)������Һ�͚��w�ijɷ�̽�����龰�زģ�����W(xu��)����������Լ���̽��������̽���^�̡�̽���Y(ji��)Փ���M(j��n)�з������u�r���ܜ�(zh��n)�_�ر���̽���Y(ji��)��������(y��ng)��̽���Y(ji��)����Q���P(gu��n)���}��������
����(n��i)���I(l��ng)���W(xu��)��(sh��)�(y��n)
�����}��ʾ���ӟ�l�����F�c�����ᷴ��(y��ng)�Ļ��W(xu��)ԭ�������Ը���(j��)�~�c�����ᷴ��(y��ng)��ԭ���w�ƣ���a(ch��n)���������F�Ͷ�������ͬ�rע��S������(y��ng)���M(j��n)�У�����ĝ��׃ϡ���F�cϡ���ᷴ��(y��ng)�������၆�F�͚�⡣�����(sh��)�H��Fe3����Fe2���ęz�(y��n)����?y��n)�o���ĽY(ji��)Փ�ЃɷN���w���У�����һ������Fe2�����������SO2��H2�ęz�(y��n)����Ҫע��ԇ�����������b�Ì��z�(y��n)���������ƣ�����H2�ęz�(y��n)���ܲ��ñ��Q��(sh��)�(y��n)���̲���Fe2���ęz�(y��n)���õ�ԇ����KSCN��Һ����ˮ����ԓ��������Fe3���ęz�(y��n)���ڵėl���²���ʹ�á�
���� ������������롿 SO2��H2
����(sh��)�(y��n)̽����
�����
���E�� ��Һ�ϼtɫ��ȥ ����Fe2��
���E�� ��ȡ����������Һ���μ�KI�͵�����Һ ��Һ׃?y��u)��{(l��n)ɫ
�����
����KMnO4��Һ��ɫ������KMnO4��Һ�ɫ��׃��ԇ�����ռ������w
�����}ӑՓ��
�����_������Һ�к���Fe3���t�o���z�(y��n)��Һ���Ƿ���Fe2��
���y��ϵ��(sh��)��0.55���C�ϑ�(y��ng)�ã��е��y�ȣ�
16�����О�Ŀ��(bi��o)�����}�ԟo�C(j��)��D�}����ʽ����N��S��Cu��Ԫ�؆��|(zh��)���仯����֮�g����D(zhu��n)���P(gu��n)ϵ��߉�������������W(xu��)���Z�ĕ���������ͬ�r�M(j��n)һ��Ӗ(x��n)���W(xu��)������(j��)�|(zh��)���غ㶨�ɡ�����߀ԭ����(y��ng)����ʽ����ƽ��������İ�����W(xu��)����ʽ�ļ��ܣ����һ������(d��o)�W(xu��)���P(gu��n)ע���c��Ȼ�ĺ��C�l(f��)չ��
����(n��i)���I(l��ng)��Ԫ�ؼ��仯����
�����}��ʾ�����}��E��tɫ���٣��ǽ��ٚ��w���|(zh��)A��B�������F�Ⱦ�����}ͻ�ƿڣ��Ƴ�A��D�����Ƴ�G��H�����}��H��K��׃���DZ��}���y�c(di��n)��J��K�njW(xu��)��δ֪֪�R����Ҫ�Y(ji��)�ϵڢdž��}��ʾ�Լ�����߀ԭ����(y��ng)֪�R�M(j��n)�����������W(xu��)����߉������������^��Ҫ��
���� ������
HNO3 �� 3CuO��2NH3 3Cu��N2��3H2O
3Cu��N2��3H2O
�� 2Cu2����2Cl����SO2��2H2O��2CuCl����4H����SO42�� �� 6NO��4NH3 5N2��6H2O
5N2��6H2O
���y��ϵ��(sh��)��0.6�����⑪(y��ng)�ã��е��y�ȣ�
17�����О�Ŀ��(bi��o)�����}�ԏļ���õ��ϳɚ��3������(y��ng)���d�w������W(xu��)�������W(xu��)����(y��ng)���ʡ����W(xu��)ƽ�ⳣ��(sh��)�����W(xu��)ƽ����Ƅӡ��w˹����Ӌ(j��)�㷴��(y��ng)��Ȼ�����Փ֪�R��������r���Լ���(y��ng)�����P(gu��n)֪�R��Q��(sh��)�H���}������������һ���ľC���ԡ�
����(n��i)���I(l��ng)���W(xu��)��������ͻ�����Փ
 �����}��ʾ���ő�(y��ng)����(j��)�D����Ӌ(j��)��CH4��ƽ������(y��ng)���ʣ���Ӌ(j��)��H2���������ʡ�10 min�r����׃�ėl�������������������w�e����t��׃�l����˲�gCH4��ȑ�(y��ng)�pС����׃�ėl�����������ߜضȣ������ˮ���⣩��
�����}��ʾ���ő�(y��ng)����(j��)�D����Ӌ(j��)��CH4��ƽ������(y��ng)���ʣ���Ӌ(j��)��H2���������ʡ�10 min�r����׃�ėl�������������������w�e����t��׃�l����˲�gCH4��ȑ�(y��ng)�pС����׃�ėl�����������ߜضȣ������ˮ���⣩��
��2������������(y��ng)�_ʼ��(qi��ng)��������������(qi��ng)��׃���w�e���ɿ������ɼ������p���õ����������ķ���(y��ng)��������CH4�D(zhu��n)���ʴ�
��3��������(y��ng)�ٜpȥ����(y��ng)�ڼ��ɵõ�����(y��ng)�۵ķ���(y��ng)�ᣬ����(j��)�����С��ƽ�ⳣ��(sh��)�����Д෴��(y��ng)��������(y��ng)�����M(j��n)�С�v(��)��v(��)
���� ������1��0.3 mol/(L?min) ���ߜضȣ������ˮ���⣩ ��2����D ��3����41.2 kJ/mol a
���y��ϵ��(sh��)��0.65���C�ϑ�(y��ng)�ã��е��y�ȣ�
18�����О�Ŀ��(bi��o)�����}ͨ�^⁼��仯������Ƃ��c��(y��ng)�Þ鱳���زģ�����W(xu��)���\(y��n)�û��W(xu��)��Փ֪�R��Q���I(y��)��(sh��)�H���}�������Լ����D�����Dʾ���^�졢�������\(y��n)�ú͔�(sh��)��(j��)̎��������
����(n��i)���I(l��ng)���W(xu��)������Փ
�����}��ʾ���Ż��W(xu��)����(y��ng)�İl(f��)�����ٱ�횝M�㡰��׃С���㡢��׃�����㡱�е�һ��������(y��ng)�����ڸ��^�՚⣨���ڶ��ԭh(hu��n)�����M(j��n)�У��ėl�����M(j��n)�У��ǿ��]�������V�c�՚������⡢��?d��)⡢������̼�ķ��?y��ng)��⁵����|(zh��)�����Ȼ�⁵�ˮ���֪�R�W(xu��)������Ϥ�����Ƶ�һ����Ҫ����Ksp�cpH�ĺ���Ӌ(j��)�㣬�ڶ�������TiO(OH)2��Ksp��С����������ˮ�⡣������(j��)M[BaTiO (C2O4)2?4H2O]��M(BaTiO3)��10.00��5.19����֪��ɫ���wA�Ļ��W(xu��)ʽ��BaTiO (C2O4)2?4H2O��
���� ������ ԓ����(y��ng)��׃�����㣨��S��0�� ���^�՚⣨���ڶ��ԭh(hu��n)�����M(j��n)�У�
�� 10 TiO2����2H2O��TiO(OH)2����2H��
�� d
���y��ϵ��(sh��)��0.6���C�ϑ�(y��ng)�ã��е��y�ȣ�
19�����О�Ŀ��(bi��o)�����}�Ծֲ����턩�����������}���}�ĺϳɞ鱳��������˴Ź�����V�y���ЙC(j��)��ĽY(ji��)��(g��u)���ЙC(j��)����(y��ng)����͡�����(y��ng)�a(ch��n)����Дࡢͬ�֮���(g��u)�w�Լ��ϳ�·�����O(sh��)Ӌ(j��)�����}��һ���ЙC(j��)��������Ɣ��c�ϳ��}���O(sh��)Ӌ(j��)������ЙC(j��)�ϳ��c��Ϣ�w���ں���һ�𣬼ȿ���W(xu��)�������}�O(sh��)��Ϣ���\(y��n)����ϳɷ�������Q�c�ЙC(j��)�ϳ����P(gu��n)�Č�(sh��)�H���}��������Ҳ����W(xu��)���O(sh��)Ӌ(j��)�ЙC(j��)�ϳɷ��������������^�ߌӴ��Ͽ����ˌW(xu��)������Ϣ���ܺ�̎�������J�̶Ⱥ�˼�S�����w�ԣ�ȫ�濼���ˌW(xu��)���ľC��������
����(n��i)���I(l��ng)���ЙC(j��)���W(xu��)���A(ch��)
�����}��ʾ����ͬ�����|(zh��)����������ͬ�ĺ˴Ź�����V���ױ���������4�в�ͬ���W(xu��)�h(hu��n)���Ě�ԭ�ӣ�ֻ�к˴Ź�����V���F(xi��n)4����r�����f���ױ��Ǽ����ġ�����(y��ng)���������Q����(y��ng)����ԇ�f���mδ���鿼�c(di��n)���}��Ҳδ�o�����P(gu��n)��Ϣ�����ɺϳ�·�������ơ���֪������(y��ng)���@Ȼ���c�}����}������(y��ng)���@Ȼ�nj�����߀ԭ�鰱�������y�Ƴ�B�ĽY(ji��)��(g��u)��ͬ�֮���(g��u)�w�ĕ����ɲ��á����뷨�������� ��C��C�I��C��H�I�в����������O(sh��)Ӌ(j��)�ϳ�·���r����(y��ng)����(j��)�}�O(sh��)��Ϣ����ֿ��]���h(hu��n)�ϵĶ�λҎ(gu��)�t���O(sh��)Ӌ(j��)��Ѻϳɾ�·��
��C��C�I��C��H�I�в����������O(sh��)Ӌ(j��)�ϳ�·���r����(y��ng)����(j��)�}�O(sh��)��Ϣ����ֿ��]���h(hu��n)�ϵĶ�λҎ(gu��)�t���O(sh��)Ӌ(j��)��Ѻϳɾ�·��
���� ������1��4 ��2�� ߀ԭ����(y��ng)
߀ԭ����(y��ng)
��3�� ��
��
��4��
���y��ϵ��(sh��)��0.65�����⑪(y��ng)�ã��е��y�ȣ�
20�����О�Ŀ��(bi��o)�����}�Ե��ۡ��w�S�صȿ������YԴ�ľC�����Þ鱳��������W(xu��)�������P(gu��n)ϵʽ���M(j��n)�л��W(xu��)����ʽ�����W(xu��)ʽӋ(j��)��ļ��ܣ�ͬ�r����W(xu��)���zȡ��Ϣ��������
����(n��i)���I(l��ng)���ЙC(j��)��ĽY(ji��)��(g��u)���ЙC(j��)����(y��ng)�����W(xu��)Ӌ(j��)��
�����}��ʾ����������ˮ��Һ�еĭh(hu��n)��Y(ji��)��(g��u)�������uȩ�s�ό�(d��o)�£��ɴˣ�����(j��)��Ԫ�h(hu��n)�Y(ji��)��(g��u)ʽ�Ɍ�����Ԫ�h(hu��n)�Y(ji��)��(g��u)ʽ������(j��)�����D(zhu��n)�����������������̈D��֪�����a(ch��n)�е��Ҵ�һ�������������������ᣬһ�������ں����ᷴ��(y��ng)��ȡ�����������Y(ji��)�����P(gu��n)���W(xu��)����ʽ���г������|(zh��)֮�g�Ķ����P(gu��n)ϵ��������������|(zh��)�����w�S����һ�������dž�Ԫ����3���u�����c���ᡢ������[(CH3CO)2O]�Ļ���������r��3�����Dz���ȫ�����ӷ���(y��ng)�������@�����R���ڢƾͲ��y��⡣
���� ���� �� ��
�� �⣺(C6H10O5)n��n C6H12O6��2nC2H5OH��nCH3COOC2H5
162n 88n
m(CH3COOC2H5)��374 kg
�� �⣺[(C6H7O2)(OH)3]n��[(C6H7O2)(OH)(3��x)(OOCCH3)x]n ��m
162n 162n��42nx 42nx
 ��
�� x��2
x��2
��ԓ�����w�S�ĽY(ji��)��(g��u)��ʽ��[(C6H7O2)(OH)(OOCCH3)2]n
���y��ϵ��(sh��)��0.45�����⑪(y��ng)�ã��^�y��
����(n��i)���I(l��ng)�����|(zh��)�Y(ji��)��(g��u)�c���|(zh��)
�����}��ʾ���ŷǽ�����Խ��(qi��ng)���ؓ(f��)��Խ�Y(ji��)��Ԫ�ص�ԭ����(sh��)��Ԫ�������ڱ��е�λ�õȿ��Ժܷ���ش_�����������Ų����M(j��n)������ԭ�Ӻ�������Ų�ʽ�������|(zh��)���ܽ��Զ���(sh��)���ϡ��������ܡ���Ҏ(gu��)�ɡ��ǽ����K�ľ����к����Kԭ�Ӕ�(sh��)��8�� ��6��
��6�� ��4�� �ȵڶ��������c���黥�������w�Ě�B(t��i)�仯�ﲻ���ڣ���(y��ng)ԓ�Ƀɂ�̼ԭ��(li��n)�뵽һ����ԭ�Ӻ�һ����ԭ�ӽM���c�������ƵĚ仯�����Bԭ���ṩ��܉����Nԭ���ṩ����ӣ�����(j��)������w�ĽY(ji��)��(g��u)���ƣ�X��Y�е�ԭ�ӡ���ԭ�ӵ�܉���s����ʽ�c��ϩ����Ȳ�е�̼ԭ�Ӿ���ͬ���f����Y�ĽY(ji��)��(g��u)��ʽ��H2B=NH2��
��4�� �ȵڶ��������c���黥�������w�Ě�B(t��i)�仯�ﲻ���ڣ���(y��ng)ԓ�Ƀɂ�̼ԭ��(li��n)�뵽һ����ԭ�Ӻ�һ����ԭ�ӽM���c�������ƵĚ仯�����Bԭ���ṩ��܉����Nԭ���ṩ����ӣ�����(j��)������w�ĽY(ji��)��(g��u)���ƣ�X��Y�е�ԭ�ӡ���ԭ�ӵ�܉���s����ʽ�c��ϩ����Ȳ�е�̼ԭ�Ӿ���ͬ���f����Y�ĽY(ji��)��(g��u)��ʽ��H2B=NH2��
���� ������O��N��C 1s22s22p63s23p63d84s2 ����K������ˮ����?y��n)����ǘO�Է��ӣ������ژO���܄� ��4 �Ȣ� ��sp3��sp2
��sp3��sp2
���y��ϵ��(sh��)��0.7���������⣬�^���ף�
21 B�����О�Ŀ��(bi��o)�����}����W(xu��)���\(y��n)���к͵ζ����y��ʳ���п������Č�(sh��)�(y��n)�Լ���Ʒ̎������(sh��)��(j��)̎����ָʾӋ(j��)�x�á���(sh��)�(y��n)�������M(j��n)���`������Ȍ�(sh��)�(y��n)���ܺͶ��������Ļ��W(xu��)˼�롣�y�Ȳ������С���(sh��)�(y��n)���W(xu��)��ģ�K�����c(di��n)��
����(n��i)���I(l��ng)��(sh��)�(y��n)���W(xu��)
�����}��ʾ�����sˮ�����е�CO2������NaOH������ȥ����ʹԇ�(y��n)�Y(ji��)��ƫ�ζ��a(ch��n)��NaAc��Һ�ʉA�ԣ���(y��ng)�x���ډA����Һ��׃ɫ��ָʾ������4��ӛ䛵Ĕ�(sh��)��(j��)������Ӌ(j��)��r��(y��ng)��ȥ��
���� ������ ��г�ȥCO2��Ѹ����s ���������z�^�ι� �� ��̪ �ζ��a(ch��n)��CH3COONa��Һˮ��ʉA�ԣ���(y��ng)�x���ډA����Һ��׃ɫ��ָʾ�� �� �û���̿Óɫ(��ζ��^����ʹ��pHӋ(j��)�y��pH) �� 4.50
���y��ϵ��(sh��)��0.7���������⣬�^���ף� www.ks5u.com
www.ks5u.com
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_ | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com