
題目列表(包括答案和解析)
某化學興趣小組進行研究性學習,探究熱水壺中的水垢。
【查閱資料】①天然水中一般都含有Ca2+、Mg2+、HCO3-等離子,在加熱時,這些離子反應生成溶解度更小的物質—水垢[Mg(OH)2和CaCO3]。
②堿石灰是氧化鈣和氫氧化鈉的固體混合物。
【實驗設計】
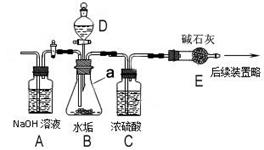
1、按圖組裝儀器,將10.8g水垢樣品放入裝置B中,在裝置D中加入一定量的稀鹽酸溶液;
2、將稀鹽酸溶液緩緩滴入裝置B中,與水垢充分反應;
3、待實驗不再產生氣泡時,打開AB間活塞,從左端緩緩鼓入一定量的空氣;
4、吹掃一段時間后,測定到裝置E質量增重了2.2g。
【分析數據】
(1)儀器a的名稱分別是___________;
(2)鼓入空氣的目的是______________ ___________________;裝置A的作用是______________________;裝置C中體現濃硫酸的__________性;
___________________;裝置A的作用是______________________;裝置C中體現濃硫酸的__________性;
(3)寫出實驗中產生氣體的化學反應方程式:_______________________;
(4)水垢中Mg(OH)2的質量為__________。
某校化學小組對熱水壺底部水垢的主要成分進行了'如下探究,請完成以下活動并回答相關問題。
【查閱資料】
天然水中含有![]() 、
、![]() 、
、![]() 等離子,在加熱條件下,這些離子趨于生成溶解度更小的物質――水垢(主要成分為碳酸鹽和堿)。有關物質的溶解性見下表:
等離子,在加熱條件下,這些離子趨于生成溶解度更小的物質――水垢(主要成分為碳酸鹽和堿)。有關物質的溶解性見下表:
部分鈣、鎂化合物溶解性表(20℃)
| 陰離子 陽離子 |
|
|
|
|
| 微溶 | 不溶 | 可溶 |
|
| 不溶 | 微溶 | 可溶 |
【提出猜想】
水垢的主要成分中一定含有 和 ,可能含有Ca(OH)2和MgCO3(填化學式)。
【設計方案】
實驗1:確定水垢中是否含Ca(OH)2和CaCO3。
| 實驗步驟 | 實驗現象 | 結論 |
| 在少量研碎的水垢中,加入適量的蒸餾水充分攪拌,過濾,在濾液里加入Na2CO3溶液 | 沒有白色沉淀產生 | _________________________ |
實驗2:確定水垢是否含MgCO3。
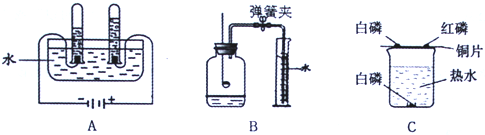
利用下列實驗裝置,完成實驗2探究。其主要實驗步驟如下:
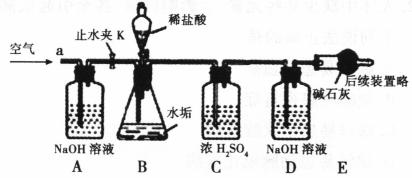
稱量D、E裝置總質量為600.00g,按上圖組裝后,將2.50g水垢試樣放入錐形瓶中,加入足量稀鹽酸溶液,待錐形瓶中不再產生氣泡時,打開止水夾K,從導管a處緩緩鼓入空氣,一段時間后稱量裝置D、E的總質量為601.25g(堿石灰主要成分為CaO和NaOH,不考慮裝置內空氣對實驗的影響)。
【實驗討論】
(1)加入樣品前還應 ,裝置B中盛放稀鹽酸的儀器名稱為 ,裝置C的作用是 ,反應結束后打開止水夾K,緩緩鼓入空氣的目的是 ,裝置A的作用是 。A、B裝置之間 設置干燥裝置(填“要”、“不要”),其理由是 。
(2)裝置B中生成氣體的化學反應方程式為 (只要求寫一種),裝置D中的化學反應方程式為 。
(3)裝置B中生成CO2的質量為 g。通過計算說明水垢中 含MgCO3(填字母)。
A.一定 B.一定不 C.可能 D.無法確定
計算過程(已知物質相對分子質量CaCO3:100,MgCO3:84):
實驗3:確定水垢中是否含有Mg(OH)2。
另取質量為2.50g水垢,加3.65%稀鹽酸與之反應,測得消耗稀鹽酸![]() g。結合以上實驗結論,判斷當
g。結合以上實驗結論,判斷當![]() 的值滿足 條件時,水垢中一定含有Mg(OH)2(請通過計算說明)。
的值滿足 條件時,水垢中一定含有Mg(OH)2(請通過計算說明)。
| 部分鈣、鎂化合物溶解性表(20℃) | |||
| OH- | CO32- | HCO3- | |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
| 實驗步驟 | 實驗現象 | 有關化學反應方程式 |
| 在少量研碎的水垢中加入適量的蒸餾水充分攪拌,過濾,在濾液中加入Na2CO3溶液. | 有白色沉淀產生 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com