
 2SO3(g),SO2的平衡轉化率與溫度、壓強的關系如右圖所示。
2SO3(g),SO2的平衡轉化率與溫度、壓強的關系如右圖所示。
| 氣體 | SO2 | O2 | SO3 |
| 濃度(mol/L) | 0.4 | 1.2 | 1.6 |
 。(已知該溫度下H2SO3的電離常數:Ka1=1.0×10-2 mol/L,Ka2=6.0×10-3 mol/L)
。(已知該溫度下H2SO3的電離常數:Ka1=1.0×10-2 mol/L,Ka2=6.0×10-3 mol/L)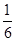 或0.17(2分)
或0.17(2分)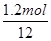 ×773kJ/mol=77.3kJ。
×773kJ/mol=77.3kJ。 SO32-+H+可知,Ka2=
SO32-+H+可知,Ka2=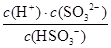 ,則
,則 =
= =
=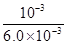 =
=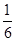 或0.17。
或0.17。

 千里馬走向假期期末仿真試卷寒假系列答案
千里馬走向假期期末仿真試卷寒假系列答案科目:高中化學 來源:不詳 題型:填空題
 2NO2(g) △H=+57.20kJ/mol。
2NO2(g) △H=+57.20kJ/mol。| 時間(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)/mol | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
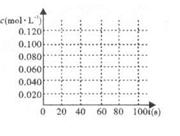
 N2O4(g)(g) △H=-57.20kJ/mol。恒溫恒容下反應相同時間后,分別測得體系中NO2的百分含量分別為a1和a2。巳知T1<T2,則a1____a2(選擇A、B、C、D填空)。
N2O4(g)(g) △H=-57.20kJ/mol。恒溫恒容下反應相同時間后,分別測得體系中NO2的百分含量分別為a1和a2。巳知T1<T2,則a1____a2(選擇A、B、C、D填空)。查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 H[CuCl2]。反應結束后將溶液倒入蒸餾水中有CuCl生成。實驗過程中加入濃鹽酸的目的是 。當c(Cl-)=2×10-3 mol·L—1時, c(Cu+-)= mol·L—1。已知:Ksp(CuCl)=1.7×10-7
H[CuCl2]。反應結束后將溶液倒入蒸餾水中有CuCl生成。實驗過程中加入濃鹽酸的目的是 。當c(Cl-)=2×10-3 mol·L—1時, c(Cu+-)= mol·L—1。已知:Ksp(CuCl)=1.7×10-7
查看答案和解析>>
科目:高中化學 來源:不詳 題型:計算題
 CH3OH(g) ΔH1
CH3OH(g) ΔH1 CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2  CO(g)+3H2(g)。
CO(g)+3H2(g)。

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題


查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.2個氫分子和1個氧分子反應生成2個水分子,放出熱量571.6 kJ |
| B.2 mol H2(g)和1 mol O2(g)反應生成2 mol H2O(l),吸收熱量571.6 kJ |
| C.2 mol H2O(l)分解為2 mol H2(g)和1 mol O2(g),吸收熱量571.6 kJ |
| D.2 mol H2(g)和1 mol O2(g)反應生成2 mol H2O(g),放出熱量571.6 kJ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2P2O5(s);ΔH1,
2P2O5(s);ΔH1, 2P2O5(s);ΔH2,則ΔH1和ΔH2的關系正確的是
2P2O5(s);ΔH2,則ΔH1和ΔH2的關系正確的是| A.ΔH1=ΔH2 | B.ΔH1<ΔH2 | C.ΔH1>ΔH2 | D.無法確定 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
A.H2(g) + I2(s) 2HI(g) - 26.5kJ 2HI(g) - 26.5kJ |
B.H2 + I2 2HI - 53kJ 2HI - 53kJ |
C.H2(g) + I2(s) 2HI(g) - 53kJ 2HI(g) - 53kJ |
D.0.5H2 + 0.5I2 HI - 26.5kJ HI - 26.5kJ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.CH4O(l)+3/2 O2(g)="=" CO2(g)+2H2O(l); △H=-725.76 kJ·mol-1 |
| B.2CH4O(l)+3 O2(g)="=" 2CO2(g)+4H2O(l); △H=+1451.6 kJ·mol-1 |
| C.2CH4O(l)+3 O2(g)="=" 2CO2(g)+4H2O(l); △H=-22.68 kJ·mol-1 |
| D.CH4O(l)+3/2 O2(g)="=" CO2(g)+2H2O(g); △H=-725.76 kJ·mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com