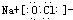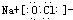元素X、Y、Z、M、N均為短周期主族元素,且原子序數依次增大.已知Y原子最外層電子數與核外電子總數之比為3:4;M原子最外層電子數與次外層電子數之比為3:4;N-、Z+、X+離子的半徑逐漸減小;化合物XN為分子晶體.據此回答:
(1)M、N的最高價氧化物的水化物中酸性較強的是(寫出化學式)______.
(2)用X的三種同位素與16O、18O構成的X2O所有分子,其相對分子質量的數值有______種.
(3)已知通常狀況下1g X2在Y2中完全燃燒放出a kJ的熱量,請寫出表示X2燃燒熱的熱化學方程式______.
(4)X與Y、X與M均可形成18電子分子,這兩種分子在水溶液中反應有黃色沉淀生成,寫出該反應的化學方程式______.
(5)化合物A、B均為由上述五種元素中的任意三種元素組成的強電解質,且兩種物質水溶液的酸堿性相同,組成元素的原子數目之比為1:1:1,A溶液中水的電離程度比在純水中小.則化合物A中的化學鍵類型為______;若B為常見家用消毒劑的主要成分,則B的電子式是______.
(6)向1.5L 0.1mol?L-1 Z的最高價氧化物對應水化物的水溶液中通入標況下2.24L CO2,充分反應.離子方程式是______.