
【題目】四種短周期元素在元素周期表中的位置如圖,其中Z的原子半徑最小。下列說法正確的是( )

A. M元素一定為金屬元素
B. X元素的最簡單氣態氫化物的熱穩定性比Z的強
C. 若Y元素存在最高價含氧酸,其酸性比X元素的最高價含氧酸弱
D. Z元素與氫元素能形成原子個數比為1∶1的共價化合物
 黎明文化寒假作業系列答案
黎明文化寒假作業系列答案科目:高中化學 來源: 題型:
【題目】以下說法中正確的是( )
A.所有△H<0的反應均是自發反應 B.自發進行的反應一定能迅速進行
C.冰在室溫下自動熔化成水,是熵增的過程 D.高錳酸鉀加熱分解是一個熵減小的過程
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上可以用廢鐵屑制備活性Fe3O4,流程如下圖:

(1)在制備過程中,要將塊狀固體原料粉碎、磨成粉末,作用是________________________
(2)在合成池里生成Fe3O4的離子方程式為__________________________
(3)根據流程可知,配料中心很可能使混合物中的Fe2O3與Fe物質的量之比接近________
(4)某同學利用廢鐵屑(含Fe和Fe2O3)來制取FeCl3·6H2O晶體,同時測定混合物中鐵的質量分數,裝置如圖(夾持裝置略,氣密性已檢驗):
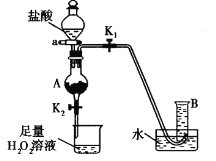
操作步驟如下:
I.打開彈簧夾K1、關閉彈簧夾K2,并打開活塞a,緩慢滴加鹽酸。
Ⅱ.當……時,關閉彈簧夾K1打開彈簧夾K2,當A中溶液完全進入燒杯后關閉活塞a。
Ⅲ.將燒杯中溶液蒸發濃縮、冷卻結晶、過濾后得到FeC13·6H2O晶體。
請回答:
① 操作Ⅱ中“……”的內容是______________,燒杯中的現象是_________________,并有氣泡產生。相應的方程式是________________、________________。(是離子反應的寫離子方程式)
②若混合物質量為m g,實驗結束后測得B中所得的氣體是V mL(標準狀況時),該同學由此計算出此廢鐵屑中鐵的質量分數是![]() ,該數值比實際數值偏低,若實驗過程操作無誤,偏低的原因是______________________。
,該數值比實際數值偏低,若實驗過程操作無誤,偏低的原因是______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是某工業生產過程。

溶解度表:
溫度℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
氯化銨 | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 55.2 | 65.6 | 71.3 | 77.3 |
硫酸銨 | 70.6 | 73 | 75.4 | 78 | 81 | 88 | 95 | 98 | 103 |
硫酸鉀 | 7.4 | 9.3 | 11.1 | 13 | 14.8 | 18.2 | 21.4 | 22.9 | 24.1 |
氯化鉀 | 28 | 31.2 | 34.2 | 37.2 | 40.1 | 45.8 | 51.3 | 53.9 | 56.3 |
(1)本工業生產過程的目標產品是____________________________________。(寫化學式)
(2)過濾Ⅰ操作所得固體中,除CaCO3外還有一種物質,該固體的用途有_________(試舉一例)。
(3)根據溶解度表轉化Ⅱ適宜的溫度是________
A、0~10℃ B、20~30℃ C、40~60℃ D、90~100℃
過濾Ⅱ操作所得濾渣是__________。
(4)我國著名的化學家也利用了轉化Ⅱ的反應原理制備了一種重要的堿,該制備的化學反應方程式為:___________________________________________________
(5)氯化鈣結晶水合物(CaCl2·6H2O)進行脫水處理可制得常用的干燥劑,根據下圖選擇最佳脫水的方法是__________

A、氯化氫氣流中加熱到174℃ B、直接加熱至174℃
C、直接加熱至260℃ D、氯化氫氣流中加熱到260℃
(6)上述工業流程實現了綠色化學的理念,其中__________________(填化學式)實現了循環利用,副產品_________________________(填化學式)可轉化為原料,整個流程基本實現了污染物零排放。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E為中學化學常見的單質或化合物,相互轉化關系如圖所示(部分產物略去)。

I.若A是能使濕潤紅色石蕊試紙變藍的氣體;C、D均為空氣的主要成分;E是一種常見無色無味的有毒氣體,B、E均為汽車尾氣成分。
(1)寫出反應①的化學方程式____________。
(2)寫出B和E在催化劑條件下生成C的化學方程式______________。
II.若A是淡黃色化合物;常溫下D是無色氣體;C中含有的陰、陽離子均為10電子粒子;E為澄清石灰水。
(1)寫出反應②的化學方程式_____________。
(2)將一定量的氣體D通入2L C的溶液中,在所得溶液中逐滴加入稀鹽酸至過量,并將溶液加熱,產生的氣體與HCl物質的量的關系如圖所示(忽略氣體的溶解和HCl的揮發)。

①O點溶液中所含溶質的化學式為_______,橫坐標3-5段發生的離子方程式為_____。
②標況下,通入氣體D的體積為______L,C溶液的物質的量濃度為_______mol/L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用CO合成甲醇(CH3OH)的化學方程式為CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0,按照相同的物質的量投料,測得CO在不同溫度下的平衡轉化率與壓強的關系如下圖所示。下列說法正確的是( )。
CH3OH(g) ΔH<0,按照相同的物質的量投料,測得CO在不同溫度下的平衡轉化率與壓強的關系如下圖所示。下列說法正確的是( )。

A. 溫度:T1>T2>T3
B. 正反應速率:v(b)>v(d) v(a)>v(c)
C. 平衡常數:K(a)>K(c) K(b)=K(d)
D. 平均摩爾質量:M(b)>M(d) M(a)<M(c)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用50mL 0.50 mol/L鹽酸與50 mL 0.55 mol/L NaOH溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱。回答下列問題:

(1)觀察實驗裝置,圖中尚缺少的一種玻璃用品是__________。
(2)燒杯間填滿碎紙條的作用是_________________________。
(3)大燒杯上口不蓋硬紙板,測得的中和熱數值 __________(填“偏大、偏小、無影響”)。
(4)實驗中改用55mL 0.50 mol/L鹽酸與55mL 0.55 mol/L NaOH溶液進行反應,與上述實驗相比,所放出的熱量__________ (填“相等、不相等”),所求中和熱__________ (填“相等、不相等”)。
(5)在中和熱測定實驗中,若用相同濃度和體積的氨水代替NaOH溶液進行實驗,測得的中和熱的數值會____(填“偏大”、“偏小”“不變”)原因是_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用下列實驗裝置進行相應實驗,能達到實驗目的的是( )

A.用圖1所示裝置(正放)可收集NO氣體
B.用圖2所示裝置可吸收多余氨氣且能防止倒吸
C.用圖3所示裝置可實現反應:Cu+2H2O![]() Cu(OH)2+H2↑
Cu(OH)2+H2↑
D.用圖4所示裝置可分離乙醇(沸點78.4 ℃)與二甲醚(沸點24.9 ℃)的混合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物結構簡式為: ,則用Na、NaOH、NaHCO3與等物質的量的該有機物恰好反應時,消耗Na、NaOH、NaHCO3的物質的量之比為 ( )
,則用Na、NaOH、NaHCO3與等物質的量的該有機物恰好反應時,消耗Na、NaOH、NaHCO3的物質的量之比為 ( )
A. 3∶3∶2 B. 3∶2∶1 C. 1∶1∶1 D. 3∶2∶2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com