
【題目】下列變化中,不存在化學鍵斷裂的是( )
A.氯化氫氣體溶于水
B.干冰氣化
C.氯化鈉固體溶于水
D.氫氣在氯氣中燃燒
 時刻準備著暑假作業原子能出版社系列答案
時刻準備著暑假作業原子能出版社系列答案 暑假銜接教材期末暑假預習武漢出版社系列答案
暑假銜接教材期末暑假預習武漢出版社系列答案 假期作業暑假成長樂園新疆青少年出版社系列答案
假期作業暑假成長樂園新疆青少年出版社系列答案科目:高中化學 來源: 題型:
【題目】清遠市某校的化學興趣小組經常做探究實驗:
(一)為了探究一氧化氮能否被Na2O2完全吸收,設計了如下實驗。裝置如下(加熱裝置省略):

查閱資料所知:①2NO+Na2O22NaNO2
②酸性條件下,NO或NO2都能與KMnO4溶液反應生成NO3- 。
回答下列問題:
(1)儀器a名稱:________。
(2)B瓶內裝的物質是:____。
(3)若NO能被Na2O2完全吸收,E裝置中的現象為___________________________。
(4)三頸燒瓶A中反應的化學方程式為_____________________________。
(5)C裝置的作用是_____________________________________。
(二)實驗室常用Na2SO3固體與濃硫酸反應制取SO2
(6)現有已制得SO2的飽和溶液,請設計一個簡單實驗,比較SO2與Fe2+ 還原性的
強弱(可供選擇的試劑有:SO2的飽和溶液、FeCl2溶液、氯水、FeCl3溶液、KSCN
溶液、Ba(NO3)2溶液、BaCl2溶液)【要求:簡要寫出實驗步驟、現象和結論】_________________________________________________________________。
(7)某同學測定部分變質的Na2SO3樣品樣品中Na2SO3的含量(已知在酸性條件下IO3-能將SO32-氧化為SO42-,自身還原為I-):
①用電子天平稱取16.00g Na2SO3固體配成l00 mL溶液,取25.00mL于錐形瓶中,并加入幾滴淀粉溶液。
②用0.1000 mol L-1酸性KIO3溶液(硫酸酸化)滴定,三次平行實驗測得標準液的體積為24.00mL。則滴定終點時錐形瓶中產生的現象為________________________,寫出與產生終點現象有關反應的離子方程式________________________________,樣品中Na2SO3的質量分數為_________。(計算結果保留四位有效數字)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中華文化源遠流長、博大精深。從化學的視角看,下列理解不正確的是
A | B | C | D |
千淘萬漉雖辛苦,吹盡黃沙始到金。劉禹錫《浪淘沙》詩句 |
司母戊鼎 |
侯德榜 |
瓷器(China) |
詩句中“淘”“漉”相當于分離提純操作中的“過濾”。 | 屬青銅制品,是我國古代科技光輝成就的代表之一。 | 我國化學工業的奠基人,主要成就: 侯氏制堿法,該堿指的是燒堿。 | 屬硅酸鹽產品,China一詞又指“瓷器”,這反映了在西方人眼中中國作為“瓷器故鄉”的形象。 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,用0.100 mol·L-1NaOH溶液分別滴定20.00 mL 0.100 mol·L-1的鹽酸和醋酸,滴定曲線如圖所示.下列說法正確的是( )
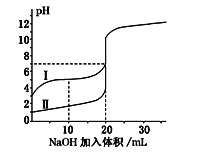
A. Ⅰ表示的是滴定鹽酸的曲線
B. pH=7時,滴定醋酸消耗的V(NaOH)小于20mL
C. V(NaOH)=20mL時,兩份溶液中c(Cl-)=c(CH3COO-)
D. V(NaOH)=10mL時,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面說法中,與鹽類水解無關的是( )
①NaHCO3做發酵粉時加入檸檬酸后效果更好
②FeCl2溶液中加入一定量的鐵粉
③實驗室配制AlCl3溶液,先把它溶解在鹽酸中,而后加水稀釋
④NH4F溶液不能保存在玻璃試劑瓶中
⑤實驗室盛放Na2CO3、Na2SiO3 等溶液的試劑瓶應用橡皮塞
⑥在NH4Cl或AlCl3 溶液中加入鎂條會產生氣泡
⑦Na2S溶液和AlCl3溶液反應得不到Al2S3
⑧室溫下NaHCO3飽和溶液pH約為8.4
⑨0.1 mol/L AlCl3溶液中c(Al3+)<0.1 mol/L
A. ②⑧ B. ①② C. ④⑧ D. 全有關
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦酸鋇(BaTiO3)在工業上有重要用途,主要用于制作電子陶瓷、PTC熱敏電阻、電容器等多種電子元件。以下是生產鈦酸鋇的一種工藝流程圖:
![]()
已知:①草酸氧化鈦鋇晶體的化學式為BaTiO(C2O4)2·4H2O;
②25℃時,BaCO3的溶度積Ksp=2.58×10-9;
(1)BaTiO3中Ti元素的化合價為:__________。
(2)用鹽酸酸浸時發生反應的離子方程式為: __________。
(3)流程中通過過濾得到草酸氧化鈦鋇晶體后,為提高產品質量需對晶體洗滌。
①過濾操作中使用的玻璃儀器有_____________________。
②如何證明晶體已洗凈?_______________________。
(4)TiO2具有很好的散射性,是一種有重要用途的金屬氧化物。工業上可用TiCl4水解來制備,制備時需加入大量的水,同時加熱,其目的是:_______________。
(5)某興趣小組取19.70gBaCO3模擬上述工藝流程制備BaTiO3,得產品13.98g,BaTiO3的產率為:________。
(6)流程中用鹽酸酸浸,其實質是BaCO3溶解平衡的移動。若浸出液中c(Ba2+)=0.1mol/L,則c(CO32-)在浸出液中的最大濃度為__________ mol/L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋁是當前應用最廣泛的金屬材料之一,鋁制品及其化合物在日常生活和工農業生產中也有著重要的用途。回答下列問題:
(1)基態鋁原子的核外電子排布式為____________。
(2)根據元素周期律等知識判斷,第一電離能Al____________Mg(填寫“大于”或“小于”)。
(3)Al2O3是常用的耐火材料,工業上也是用電解Al2O3方法制取金屬Al,據此判斷Al2O3的晶體類型是____________。
(4)LiAlH4是一種重要的有機合成試劑,AlH4-的立體構型為____________,LiAlH4中Al原子的雜化軌道類型為____________。
(5)金屬鋁的晶胞結構如圖1所示,原子之間相對位置關系的平面圖如圖2所示。
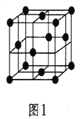
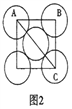
①晶體鋁中原子的堆積方式為____________。
②已知鋁原子半徑為acm,摩爾質量為Mg·mol-1,阿伏加德羅常數的值為NA,則晶體鋁的密度ρ=_______g·cm-3(用含a、M、NA的代數式來表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、X、Y和Z是原子序數依次遞增的短周期元素,其中A與Y同主族,X與Z同主族,B和X均可與A形成10電子的化合物;B與Z的最外層電子數之比為2:3,化合物Y2X2與水反應生成X的單質,所得溶液可使酚酞變紅。請回答下列問題。
(1)Z的原子結構示意圖為_______,化合物BA4的電子式為__________。
(2)化合物Y2X2中含有的化學鍵類型有________________________。
(3)化合物A2X和A2Z中,沸點較高的是_________(填化學式),其主要原因是______。
(4)A與X和A與Z均能形成18個電子的化合物,此兩種化合物發生反應的化學方程式為______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學上通常把原子數和電子數相等的分子或離子稱為等電子體,人們發現等電子體間的結構和性質相似(即等電子原理),B3N3H6被稱為無機苯,它與苯是等電子體,則下列說法中不正確的是
A. 無機苯是由極性鍵組成的非極性分子
B. 無機苯能發生加成反應和取代反應
C. 無機苯不能使KMnO4酸性溶液褪色
D. 無機苯的二氯取代物有3種同分異構體
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com