
有X、Y、Z、W四種物質的水溶液,它們分別是Na2CO3、NaOH、CH3COOH和NaCl中的一種。已知X、Y兩溶液中水的電離程度相同,X、Z兩溶液的pH相同,請回答下列問題:
(1)X是 ,Z是 ;
(2)Z、W兩溶液中水的電離程度由大到小的順序為 (用化學式表示);
(3)寫出Z溶液與過量Y溶液反應的離子方程式 ;
(4)X、Y兩溶液恰好完全反應后,溶液中各離子濃度由大到小的順序是
。
(1)NaOH、Na2CO3(共2分,各1分)
(2)Na2CO3>NaCl(2分,“>”用“、”也可)
(3)CO32—+2CH3COOH= 2CH3COO—+CO2↑+H2O(3分,沒配平扣1分)
(4)c(Na+)>c(CH3COO—)>c(OH—)>c(H+)(3分)
解析試題分析:NaOH、CH3COOH抑制水電離,有可能兩溶液中水的電離程度相同,又Na2CO3、NaOH溶液呈堿性,有可能兩溶液的pH相同,所以X是NaOH溶液,Y是CH3COOH,Z是Na2CO3,W是NaCl。⑴X是NaOH溶液,Z是Na2CO3,答案:NaOH、Na2CO3;⑵Na2CO3水解促進水電離,所以Na2CO3溶液中水的電離程度大于NaCl,答案;Na2CO3>NaCl; ⑶Na2CO3與過量的CH3COOH反應的離子方程式為:CO32—+2CH3COOH= 2CH3COO—+CO2↑+H2O,答案:CO32—+2CH3COOH= 2CH3COO—+CO2↑+H2O;⑷X、Y兩溶液恰好完全反應后,溶液實際上是CH3COONa溶液,CH3COO—少量水解,CH3COO―+H2O CH3COOH+OH―,水解后溶液呈堿性,所以溶液中各離子濃度由大到小的順序是c(Na+)>c(CH3COO—)>c(OH—)>c(H+),答案:c(Na+)>c(CH3COO—)>c(OH—)>c(H+)。
CH3COOH+OH―,水解后溶液呈堿性,所以溶液中各離子濃度由大到小的順序是c(Na+)>c(CH3COO—)>c(OH—)>c(H+),答案:c(Na+)>c(CH3COO—)>c(OH—)>c(H+)。
考點:元素及其化合物、電解質溶液中離子濃度大小比較


科目:高中化學 來源: 題型:填空題
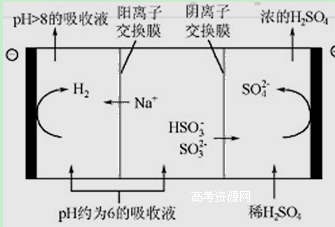
(8分)最近霧霾天氣又開始肆虐我國大部分地區。其中SO2是造成空氣污染的主要原因,利用鈉堿循環法可除去SO2。
(1)鈉堿循環法中,吸收液為Na2SO3溶液,該吸收反應的離子方程式是
(2)已知H2SO3的電離常數為 K1=1.54×10-2 , K2=1.02×10-7, H2CO3的電離常數為 K1=4.30×10-7, K2= 5.60×10-11,則下列微粒可以共存的是_____________。
A.CO32- HSO3- B.HCO3- HSO3-
C.SO32- HCO3- D.H2SO3 HCO3-
(3)吸收液吸收SO2的過程中,pH隨n(SO3²﹣):n(HSO3﹣)變化關系如下表:
| n(SO3²﹣):n(HSO3﹣) | 91 :9 | 1 :1 | 1 :91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)水的電離平衡曲線如圖所示,若A點表示25℃時水的電離達平衡時的離子濃度,B點表示100℃時水的電離達平衡時的離子濃度。則100℃時1 mol·L-1的NaOH溶液中,由水電離出的c(H+)=___________mol·L-1。25 ℃時,向水的電離平衡體系中加入少量NH4Cl固體,對水的電離平衡的影響是________(填“促進”、“抑制”或“不影響”)。
(2)電離平衡常數是衡量弱電解質電離程度強弱的量。已知如表數據。
| 化學式 | 電離平衡常數(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
從海水中提取鎂是世界各國獲得鎂的主要來源,以下是制取鎂的過程中涉及的幾種物質的溶度積,根據你所學的知識回答下列幾個問題:
| 物質 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| 溶度積 | 2.8×10–9 | 6.8×10–6 | 5.5×10–6 | 1.8×10–11 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫及其化合物有廣泛的應用,對SO2性質的研究是高中化學教學的一項重要內容。
I.對比研究是一種重要的研究方法。若將硫的單質及部分化合物按如下表所示分成3 組,則第2組中物質M的化學式是 。
| 第1組 | 第2組 | 第3組 |
| S (單質) | SO2、H2SO3、M、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |

| n(SO32—):n(HSO3—) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
| 序號 | 實驗方案 | 實驗現象 | 結論 |
| 方案① | 往第一份試液中加入KMnO4溶液溶液 | 紫紅色褪去 | SO2與Fe3+反應生成了Fe2+ |
| 方案② | 往第二份試液中加入 | | SO2與Fe3+反應生成了Fe2+ |
| 方案③ | 往第二份試液中加入 | | SO2與Fe3+反應生成了SO42— |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
常溫下,將某一元酸HA和NaOH溶液等體積混合,兩種溶液的濃度和混合后所得溶液的pH,如下表:
| 實驗編號 | HA物質的量濃度(mol·L-1) | NaOH物質的量濃度(mol·L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫酸是強酸,中學階段將硫酸在水溶液中看作完全電離。但事實是,硫酸在水中的第一步電離是完全的,第二步電離并不完全,其電離情況為:H2SO4=H++HSO4-,HSO4- H+ + S042-。
H+ + S042-。
請回答下列有關問題:
(1)Na2SO4溶液呈_(填“弱酸性”、“中性”或“弱堿性”),其理由是_
(用離子方程式表示)。
(2)H2SO4溶液與BaC12溶液反應的離子方程式為_ 。
(3)在0.l0mol·L-1的Na2SO4溶液中,下列離子濃度關系正確的是_ (填寫編號)。
| A.c(Na+)=c(SO42-)+c(HSO4一)+c(H2SO4) |
| B.c(OH-)="c(" HSO4-)+c(H+) |
| C.c( Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-) |
| D.c( Na+)=2c(SO42-)+2c(HSO4-) |
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
[14分]已知:I2+2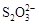

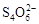 +2I―。相關物質的溶度積常數見下表:
+2I―。相關物質的溶度積常數見下表:
| 物質 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(12分)某學生用0.1000mol·L-1標準NaOH溶液滴定未知濃度的鹽酸,其操作可分解為以下幾步:
A移取25.00mL待測鹽酸溶液注入潔凈的錐形瓶中,并加入2~3滴酚酞溶液
B用標準NaOH溶液潤洗滴定管2~3次
C把盛有標準NaOH溶液的堿式滴定管固定好,擠壓玻璃珠,使滴定管尖嘴充滿溶液
D取標準NaOH溶液注入堿式滴定管到“0”刻度以上2~3cm
E.調節液面至“0”或“0”刻度以下,記下讀數
F.把錐形瓶放在滴定管的下面,用標準NaOH溶液滴定到終點,并記下滴定管液面的讀數
(1)下圖中屬于堿式滴定管的 (選填:“甲”、“乙”)。
(2)正確的操作順序是 (填字母序號)。
(3)上述B步操作的目的是 。
(4)判斷到達滴定終點的實驗現象是 。
(5)上述A步操作之前,若先用待測溶液潤洗錐形瓶,則對滴定結果的影響是 (填“偏大”或“偏小”或“無影響”)。
(6)若平行實驗三次,記錄的數據如下表
| 滴定次數 | 待測溶液的體積(/mL) | 標準NaOH溶液的體積 | |
| 滴定前讀數(/mL) | 滴定后讀數(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com