
硫酸是強酸,中學階段將硫酸在水溶液中看作完全電離。但事實是,硫酸在水中的第一步電離是完全的,第二步電離并不完全,其電離情況為:H2SO4=H++HSO4-,HSO4- H+ + S042-。
H+ + S042-。
請回答下列有關問題:
(1)Na2SO4溶液呈_(填“弱酸性”、“中性”或“弱堿性”),其理由是_
(用離子方程式表示)。
(2)H2SO4溶液與BaC12溶液反應的離子方程式為_ 。
(3)在0.l0mol·L-1的Na2SO4溶液中,下列離子濃度關系正確的是_ (填寫編號)。
| A.c(Na+)=c(SO42-)+c(HSO4一)+c(H2SO4) |
| B.c(OH-)="c(" HSO4-)+c(H+) |
| C.c( Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-) |
| D.c( Na+)=2c(SO42-)+2c(HSO4-) |
(1)弱堿性;SO42-+H2O HSO4-+OH-;
HSO4-+OH-;
(2)Ba2++HSO4-=BaSO4↓+H+
(3)BCD;
(4)<;H2SO4=HSO4-+H+,電離出的H+抑制HSO4-的電離;
(5)0.01
解析試題分析:(1)HSO4- H+ + SO42-存在電離平衡,SO42-要發生水解,溶液呈現弱堿性;(2)HSO4-為弱酸酸式酸根書寫離子方程式不拆寫;(3)B為質子守恒;C為電荷守恒;D為物料守恒;(4)略;(5)0.10 mol·L-1H2SO4溶液的pH=-lg0.11,則=0.11mol·L-1,硫酸一級電離出c(H+)為0.1mol·L-1,因此0.11-0.1=0.01,多電離出的H+為二級電離所得,即C(SO42-)=0.01mol·L-1。
H+ + SO42-存在電離平衡,SO42-要發生水解,溶液呈現弱堿性;(2)HSO4-為弱酸酸式酸根書寫離子方程式不拆寫;(3)B為質子守恒;C為電荷守恒;D為物料守恒;(4)略;(5)0.10 mol·L-1H2SO4溶液的pH=-lg0.11,則=0.11mol·L-1,硫酸一級電離出c(H+)為0.1mol·L-1,因此0.11-0.1=0.01,多電離出的H+為二級電離所得,即C(SO42-)=0.01mol·L-1。
考點:電離平衡的計算。


科目:高中化學 來源: 題型:填空題
(1)常溫下pH="5" HCl溶液和pH=5的AlCl3溶液中由水電離產生的c (H+) 之比等于 。
(2)寫出泡沫滅火器滅火時發生反應的離子方程式 。
(3)常溫下將0.01molCH3COONa和0.02mol鹽酸溶于水,配成0.5L混合溶液。溶液中共有 種微粒,各離子濃度從大到小的順序為 。
(4)常溫下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH溶液,圖中所示曲線表示混合溶液的pH變化情況(忽略溶液混合時的體積變化)。
回答下列問題:
①由圖中信息可知HA為_______酸(填“強”或“弱”) ② K點對應的溶液中c(M+)+c(MOH)= mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)25℃時,某NaCl溶液中c(Cl–)=1×10-4 mol·L–1,則該溶液中c(Na+)∶c(OH-)=
(2)25℃時,將0.1 mol·L–1NaOH溶液與0.06 mol·L–1的H2SO4溶液等體積混合(忽略混合后體積的變化),求所得溶液的pH= 。25℃時,pH值為8的NaOH溶液與pH值為10的NaOH溶液等體積混合后,溶液中氫離子濃度最接近 。
(3)25℃時,下列四種溶液中,①pH=0的鹽酸 ②0.1 mol·L–1的鹽酸 ③0.01 mol·L–1的NaOH溶液 ④pH=11的NaOH溶液,由水電離生成氫離子濃度之比①︰②︰③︰④是: (填字母)
| A.1︰10︰100︰1000 | B.0︰1︰12︰11 |
| C.14︰13︰12︰11 | D.14︰13︰2︰3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
有X、Y、Z、W四種物質的水溶液,它們分別是Na2CO3、NaOH、CH3COOH和NaCl中的一種。已知X、Y兩溶液中水的電離程度相同,X、Z兩溶液的pH相同,請回答下列問題:
(1)X是 ,Z是 ;
(2)Z、W兩溶液中水的電離程度由大到小的順序為 (用化學式表示);
(3)寫出Z溶液與過量Y溶液反應的離子方程式 ;
(4)X、Y兩溶液恰好完全反應后,溶液中各離子濃度由大到小的順序是
。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
膽礬是一種常見的化合物,工業上它也是一種制取其它含銅化合物的原料,現有廢銅(主要雜質為Fe)來制備膽礬。有人設計了如下流程:
pH值控制可參考下列數據
| 物質 | 開始沉淀時的pH值 | 完全沉淀時的pH值 |
| 氫氧化鐵 | 2.7 | 3.7 |
| 氫氧化亞鐵 | 7.6 | 9.6 |
| 氫氧化銅 | 5.2 | 6.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)大氣中SO2含量過高會導致雨水中含有(填化學式) 而危害植物和建筑物。工廠排放的SO2尾氣用飽和Na2SO3溶液吸收可得到重要化工原料NaHSO3,反應的化學方程式為 。
(2)已知NaHSO3的水溶液顯酸性,比較其中SO32-、HSO3-、H2SO3三種粒子的濃度: > > 。
(3)SO2是空氣質量報告的指標之一,可用SO2還原KIO3生成I2的反應測定空氣中SO2含量。每生成0.01mol I2,參加反應的SO2為 mol。
(4)已知25℃時,Ksp(BaSO4)=1.1×10-10,Ksp (BaCO3)=2.6×10-9。下列說法不正確的是
A.25℃時,向BaSO4懸濁液中加入大量水,Ksp(BaSO4)不變
B.25℃時,向BaSO4懸濁液中加入Na2CO3溶液后,BaSO4不可能轉化為BaCO3
C.向Na2SO4中加入過量BaCl2溶液后,溶液中c(SO42-)降低為零
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(17分)化學反應原理在科研和生產中有廣泛應用。
(1)一定條件下,模擬某礦石形成的反應aW+bQ→cN+dP+eR得到兩個圖像。
①該反應的△H 0(填“>”、“=”或“<”)。
②某溫度下,平衡常數表達式為K =c2(X),則由圖(2)判定X代表的物質為____。
(2)將E和F加入密閉容器中,在一定條件下發生反應:E(g)+F(s) 2G(g)。忽略
2G(g)。忽略
固體體積,平衡時G的體積分數(%)隨溫度和壓強的變化如下表所示:
則K(915℃)與K(810℃)的關系為K(915℃)____K(810℃)(填“大于”、“等于”或“小于”),a、b、f三者的大小關系為 ,1000℃、3.0 MPa時E的轉化率為____。(3)25℃時,H2CO3 HCO3-+H+的電離常數Ka=4×10—7 mo1·L-1,則該溫度下,NaHCO3的水解常數Kh= ,請用適當的試管實驗證明Na2CO3溶液中存在CO32-+H2O
HCO3-+H+的電離常數Ka=4×10—7 mo1·L-1,則該溫度下,NaHCO3的水解常數Kh= ,請用適當的試管實驗證明Na2CO3溶液中存在CO32-+H2O  HCO3-+OH-的事實 。
HCO3-+OH-的事實 。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
已知:Cu(OH)2是二元弱堿;亞磷酸(H3PO3)是二元弱酸,與NaOH溶液反應,生成Na2HPO3。
(1)在銅鹽溶液中Cu2+發生水解反應的離子方程式為____,該反應的平衡常數為____;(已知:25℃時,Ksp[Cu(OH)2]=2.0×10-20mol3/L3)
(2)根據H3PO3的性質可推測Na2HPO3稀溶液的pH______7(填“>”“<”或“=”)。常溫下,向10mL0.01mol/L H3PO3溶液中滴加10ml0.02mol/LNaOH溶液后,溶液中各種離子濃度由大到小的順序是_________;
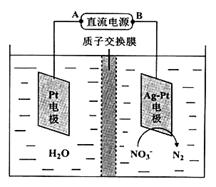
(3)電解Na2HPO3溶液可得到亞磷酸,裝置如圖(說明:陽膜只允許陽離子通過,陰膜只允許陰離子通過)
①陽極的電極反應式為____________________。
②產品室中反應的離子方程式為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
亞硝酸鈉(NaNO2)是重要的防腐劑。某化學興趣小組嘗試制備亞硝酸鈉,查閱資料:①HNO2為弱酸,在酸性溶液中,NO2-可將MnO4-還原為Mn2+且無氣體生成。
②NO不與堿反應,可被酸性KMnO4溶液氧化為硝酸
探究一 亞硝酸鈉固體的制備
以碳和濃硝酸為起始原料,設計如下裝置利用一氧化氮與過氧化鈉反應制備亞硝酸鈉。(反應方程式為2NO+Na2O2=2NaNO2,部分夾持裝置和A中加熱裝置已略)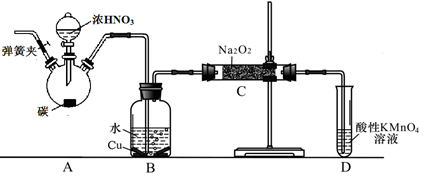
(1)寫出裝置A燒瓶中發生反應的化學方程式 。
(2)有同學認為裝置C中產物不僅有亞硝酸鈉,還有碳酸鈉和氫氧化鈉,為排除干擾應在B、C裝置間增加裝置E,E中盛放的試劑應是 (填字母)。
A.濃H2SO4 B.堿石灰 C.無水CaCl2
探究二 亞硝酸鈉固體含量的測定及性質驗證
稱取裝置C中反應后的固體4.000g溶于水配成250mL溶液,取25.00mL溶液于錐形瓶中,用0.1000
mol/L酸性KMnO4溶液進行滴定,實驗所得數據如下表所示:
| 滴定次數 | 1 | 2 | 3 | 4 |
| KMnO4溶液體積/mL | 20.60 | 20.02 | 20.00 | 19.98 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com