
【題目】向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的鹽酸,生成沉淀。溶度積為Ksp=c(Ag+)·c(Cl-)=1×10-10,試求(寫出簡單計算過程):
(1)沉淀生成后溶液中c(Ag+)為_____。
(2)沉淀生成后溶液的pH是___。
【答案】10-7mol·L-1 2
【解析】
(1)依據題干數據計算沉淀后溶液中氯離子濃度,結合Ksp計算溶液中銀離子濃度;
(2)計算沉淀后溶液中氫離子濃度,再計算pH。
(1)50ml 0.02mol/L的鹽酸中加入50ml 0.018mol/L AgNO3溶液加入后兩者濃度分別為c(Ag+)=![]() =0.009 mol/L,c(Cl-)=
=0.009 mol/L,c(Cl-)=![]() =0.01mol/L,由Ag++Cl-=AgCl↓可知,Cl-過量,過量濃度c(Cl-)=0.01-0.009=0.001mol/L,Ksp=c(Ag+)×C(Cl-)=1.8×10-10,則:c(Ag+)=
=0.01mol/L,由Ag++Cl-=AgCl↓可知,Cl-過量,過量濃度c(Cl-)=0.01-0.009=0.001mol/L,Ksp=c(Ag+)×C(Cl-)=1.8×10-10,則:c(Ag+)=![]() =1.8×10-7(mol/L);
=1.8×10-7(mol/L);
(2)溶液中氫離子濃度=![]() 0.01mol/L,溶液pH=-lg0.01=2;
0.01mol/L,溶液pH=-lg0.01=2;
答案:10-7mol·L-1 2


科目:高中化學 來源: 題型:
【題目】為了進行氨的催化氧化實驗:4NH3+5O2![]() 4NO+6H2O。請從下圖中選用所需的儀器(可重復使用)組成一套進行該反應的簡單裝置。現提供試劑:過氧化鈉、堿石灰、鉑粉、氯化鈣、濃硫酸、濃氨水和氫氧化鈉溶液。
4NO+6H2O。請從下圖中選用所需的儀器(可重復使用)組成一套進行該反應的簡單裝置。現提供試劑:過氧化鈉、堿石灰、鉑粉、氯化鈣、濃硫酸、濃氨水和氫氧化鈉溶液。
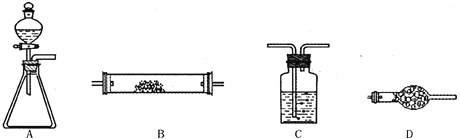
將所選的儀器按連接順序由上至下依次填入下表(可不填滿,也可以補充),并寫出該儀器中應加試劑的名稱及其作用。
選用的儀器(填字母) | 加入的試劑 | 作用 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所涉及的物質均為中學化學中的常見物質,其中C、D、E為單質,E為固體,F為有磁性的化合物。它們之間存在如下關系(反應中生成的水及次要產物均已略去):
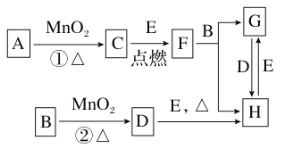
(1)寫出下列物質的化學式:B________,E________。
(2)指出MnO2在相關反應中的作用:反應①中是________劑,反應②中是________劑。
(3)若反應①是在加熱條件下進行,則A是________(填化學式);若反應①是在常溫條件下進行,則A是________(填化學式);如在上述兩種條件下得到等質量的C單質,反應中轉移的電子數之比為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科研團隊成功研究出高比能量、低成本的鈉離子二次電池,其工作原理示意圖如圖。已知電池反應:Na1-xMnO2+NaxCn![]() NaMnO2+nC。下列說法正確的是( )
NaMnO2+nC。下列說法正確的是( )
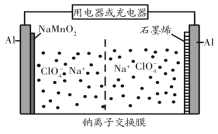
A.電池放電過程中,NaMnO2/Al上的電勢低于石墨烯/Al上的電勢
B.電池放電時,正極可發生反應Na1-xMnO2+xNa++xe-=NaMnO2
C.電池充電時,外接電源的負極連接NaMnO2/Al電極
D.電池充電時,Na+由NaMnO2/Al電極移向石墨烯/Al電極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】打印機使用的墨粉中含有Fe3O4。它的一種制備方法是:將FeSO4溶液、Fe2(SO4)3溶液按一定比例混合,再加入一定量的NaOH溶液,水浴加熱。反應如下:
反應a:![]()
下列分析不正確的是
A.Fe3O4具有磁性
B.反應a中,Fe2+ 是還原劑,Fe3+ 是氧化劑
C.從左至右,反應a各物質的系數依次為1、2、8、1、4
D.Fe3O4與鹽酸反應,生成鹽和水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】具有相同電子層數的![]() 、
、![]() 、
、![]() 三種元素,已知它們最高價氧化物的水化物的酸性強弱順序是
三種元素,已知它們最高價氧化物的水化物的酸性強弱順序是![]() ,則下列判斷正確的是( )
,則下列判斷正確的是( )
A.原子半徑:![]()
B.元素的非金屬性:![]()
C.氣體氫化物的穩定性:![]()
D.陰離子的還原性:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年諾貝爾化學獎頒給鋰離子電池領域,獲獎科學家的重要貢獻之一是研發出了電極材料——磷酸亞鐵鋰(LiFePO4)。LiFePO4的一種制備方法如下。

已知:H3PO4能電離出PO43-。
(1)Li在元素周期表中的位置是________。
(2)LiFePO4中,鐵元素的化合價為________價。
(3)將反應Ⅰ補充完整:____Fe2+ + 2H+ + ____H2O2 =____Fe3+ + 2H2O 。____
(4)反應Ⅲ的化學方程式是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將O2和NH3的混合氣體448mL通過加熱的三氧化二鉻(催化劑),充分反應后,再通過足量的水,最終收集到44.8mL O2。原混合氣體中O2的體積可能是(假設氨全部被氧化;氣體體積均已換算成標準狀況)( )
A. 134.4mL B. 313.6mL C. 287.5mL D. 268.8mL
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反應中。
(1)________元素被氧化,________是氧化劑。
(2)________是氧化產物,________發生氧化反應。
(3)在參加反應的鹽酸中,起還原劑(被氧化)作用的HCl與起酸性作用的HCl的質量比為_______。
(4)用雙線橋法標明電子轉移的方向和數目。____________________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com